ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Обоснование. Остеопороз — хроническое метаболическое заболевание скелета, характеризующееся высокой частотой низкотравматичных переломов вследствие снижения плотности костной ткани и нарушения ее микроархитектоники. Постменопаузальный остеопороз занимает около 80% в структуре остеопороза у женщин после 50 лет. Сахарный диабет (СД) не только является фактором риска низкотравматичных переломов, но и ухудшает репаративные процессы в костной ткани. Встречаемость и СД 2 типа, и остеопороза возрастает в период менопаузы, поэтому изучение костного обмена в условиях экспериментального СД и менопаузы без вмешательства внешних факторов представляется важным.
Цель. Изучение маркеров костного обмена и параметров гистоморфометрии костной ткани в условиях хирургической менопаузы и экспериментального СД.
Материалы и методы. В начале эксперимента половине самок крыс стока Wistar проводилась двусторонняя овариэктомия (ОЭ). Затем в течение 4 нед и далее на протяжении всего эксперимента животные находились на диете с повышенным содержанием насыщенных жиров. Для моделирования СД вводился раствор никотинамида и стрептозотоцина. Были сформированы следующие группы: «Контроль» (самки без каких-либо вмешательств, получавшие стандартный корм, n=5), «ОЭ» (самки после ОЭ, n=5), «CД» (самки с моделированным СД, n=4), «ОЭ+CД» (самки после ОЭ с СД, n=4). Период наблюдения составил 8 нед. В конце эксперимента производился забор крови с последующим определением маркеров костного ремоделирования и фосфорно-кальциевого обмена (остеокальцин, остеопротегерин (ОПГ), лиганд активатора рецептора ядерного фактора каппа-бета (RANKL), склеростин, фактор роста фибробластов-23 (ФРФ-23), кальций общий, фосфор неорганический). После эвтаназии проводилось гистоморфометрическое исследование костей.
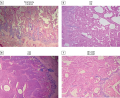
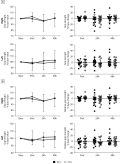
Результаты. Уровень фосфора был значимо ниже как в группе «ОЭ» (1,63 [1,58; 1,65] ммоль/л), так и в группе «СД» (2,81 [2,57; 2,83] ммоль/л) по сравнению с группой «Контроль» (3,12 [2,55; 3,24] ммоль/л), р<0,001. Данный показатель был значимо выше в группе «ОЭ+СД» (2,79 [2,46; 2,81] ммоль/л) по сравнению с группой «ОЭ» (2,79 [2,46; 2,81] ммоль/л), р=0,025. Уровень остеокальцина был достоверно ниже в группе «СД» (8,11 [7,84; 9,19] нг/мл) по сравнению с группой «Контроль» (16,97 [14,07; 17,07] нг/мл), р=0,005. Найдена слабая отрицательная корреляционная связь (r=-0,5; p<0,05 ) между уровнем глюкозы и уровнем остеокальцина. Выявлены более низкая концентрация RANKL в группе «ОЭ+СД» (278,1 [273,1; 289,7] пг/мл) по сравнению с группой «ОЭ» (400,6 [394,5; 415,1] пг/мл) и более высокое соотношение ОПГ/RANKL (0,03 [0,02; 0,04] и 0,01 [0,004; 0,014] соответственно), р=0,05. В группе «ОЭ» получен более низкий уровень ОПГ (5,1 [1,5; 5,6] пмоль/л) и соотношения ОПГ/RANKL (0,01 [0,003; 0,014]), чем в группе «Контроль» (12,3 [8,8; 14,2] пмоль/л и 0,34 [0,33; 0,4], р=0,025 и р=0,07 соответственно). Площадь костных балок в зоне эпифиза была наибольшей в группе «Контроль» (42 [39; 45]%), различия достоверны по сравнению с группой «ОЭ» (29 [25; 33]%, p=0,011) и группой «ОЭ+СД» (30 [23; 25]%, p=0,016). Площадь костных балок в зоне метаэпифиза также была наибольшей в группе «Контроль» (49 [46; 52]%) по сравнению с группами «ОЭ» (35 [25; 39]%), «СД» (31 [26; 34]%), «ОЭ+СД» (35 [33; 38]), p <0,001. В толщине костных балок различий между группами не было.
Заключение. СД может значимо угнетать костное ремоделирование у животных без хирургической менопаузы, что выражается в более низком уровне остеокальцина. Костный обмен при СД и менопаузе характеризуется более низким уровнем RANKL и более высоким соотношением ОПГ/RANKL, чем у животных без СД. Влияние ОЭ на костный обмен характеризуется большим снижением площади костных балок, чем при изолированном СД.
Обоснование. Как вегетативный дисбаланс контроля сердечного ритма, оцениваемый по вариабельности сердечного ритма (ВСР), так и признаки резистентности к инсулину достаточно распространены в выборке мужчин-северян. Однако до настоящего времени нет данных, связаны ли отклонения в ВСР в более старших возрастных группах жителей Севера с наличием инсулинорезистентности.
Цель. Проведение сравнительного анализа основных характеристик ВСР у мужчин зрелого возраста, проживающих в условиях Российского Севера, с учетом наличия или отсутствия метаболических признаков инсулинорезистентности.
Материалы и методы. Обследованы 73 мужчины зрелого возраста — постоянные жители Магаданской области из числа европеоидов. Анализируемая группа была дифференцирована на выборку без признаков (индекс HOMA-IR<2,5 усл. ед.) и с признаками инсулинорезистентности (индекс HOMA-IR>2,5 усл. ед.). В работе использовали иммунохемилюминесцентный и ферментативный методы, а также метод оценки ВСР c помощью прибора «Варикард» (Россия).
Результаты. Показано, что у 48% пациентов в анализируемой выборке были зафиксированы признаки инсулинорезистентности, что наблюдалось на фоне увеличения симпатической активности в регуляции сердечного ритма у представителей данной группы. Проведенный анализ основных характеристик кардиоритма у мужчин, различающихся по величине индекса HOMA-IR, позволил выявить ряд показателей, претерпевающих наиболее существенные изменения в зависимости от наличия или отсутствия признаков инсулинорезистентности: MxDMn, pNN50, SDNN, AMo50, SI, TP, HF, LF, масса тела.
Заключение. В целом полученные нами результаты свидетельствуют о достаточно высокой доле лиц с наличием признаков инсулинорезистентности в группе мужчин-северян зрелого возраста. Полученные результаты указывают на то, что обследуемые мужчины с признаками инсулинорезистентности характеризуются наличием вегетативного дисбаланса с относительным доминированием симпатической активности на фоне снижения активации парасимпатического звена вегетативной нервной системы и большими величинами массы тела. При этом взаимоотношения и причинно-следственные связи между признаками инсулинорезистентности, активации симпатического звена вегетативной нервной системы и избыточной массы тела во многом остаются невыясненными. По-видимому, все анализируемые признаки, скорее всего, взаимно дополняют, чем полностью исключают друг друга, при этом триада в виде ожирения, признаков инсулинорезистентности и активации симпатического звена вегетативной нервной системы является предпосылкой для значительных рисков нарушения здоровья. Необходимо отметить, что данное исследование направлено на расширение использования метода оценки вариабельности сердечного ритма с учетом наличия или отсутствия метаболических признаков инсулинорезистентности в выборке мужчин зрелого возраста.
BACKGROUND: Obesity, expressed as a high body mass index (BMI), is associated with a risk of decrease in functional capacity and muscle strength, in particular in weight-bearing joints, but so far, no study has been able to show a sufficiently strong relationship between these factors. two options in conclusion.
AIM: This study was conducted to quantify the effect of intense exercise on the functional capacity and muscle power of obese individuals and the risk of knee osteoarthritis.
MATERIALS AND METHODS: The present research project is characterized as a clinical trial, cross-sectional, and uncontrolled research. All participants had a body mass index from 30.6 kg/m² to 34.9 kg/m² and reported not working out in the last 3 months prior to this experiment. Before their involvement, all participants were informed during an initial interview about the experimental procedure, the nature of the research, and the test protocols. They gave their written and signed informed consent to voluntarily participate in this research and completed two questionnaires. Participants in our study were recruited from sports centers, social clubs, and word of mouth. A total of 78 participants responded to the call articipated in our training protocol which was composed of two main parts. The first one is the «Anthropometric measurements tests» and the second one is the «Functional capacity tests» that were done in a gym. The participants were divided randomly into two experimental. After the end of every phase of the experiment, some members of each group were moved randomly to the other group.
RESULTS: The final results of the intra-class correlation coefficient measurements for a set of tests showed strong reliability among members of each examined group. For the handgrip strength tests of the right and left hands, the results were 0.850 and 0.892, respectively. For the squat jump and countermovement jump tests, the results were 0.966 and 0.932, respectively. The results were 0.896 and 0.945 for walking 6 meters with or without double tasks. Finally, for the TUG and TUP-DT tests, the results were 0.520 and 0.663, respectively. After analyzing and interpreting the data for the functional capacity tests, the following results were obtained: For the 5 sit-stand test, the result was (F (3.87)=4.22; p=0.008, ηp2=0.127). For the Time up and go test, the result was (F (3.87)=4.56; p=0.019, ηp2=0.136), and for the 6 m walk, the result was (F (3.87)=3.81; p=0.013, ηp2=0.116). Finally, the 5X sit-to-stand test at 48 hours was lower than the base value (p=0.024), while the TUG immediately after the post was lower than the base value.
CONCLUSION: In conclusion, the results of this study demonstrate the positive impact of intense exercise on muscle power and functional capacity in obese individuals. These findings suggest that high-intensity physical activity may be an effective means of improving the health and quality of life of obese individuals. Therefore, it is recommended that obese individuals include high-intensity exercise in their regular exercise program to reap these health benefits. However, it is important to emphasize the importance of consulting a healthcare professional before starting a high-intensity exercise program to avoid the risk of injury or health complications.
Обоснование. У мужчин ожирение сопровождается комплексом метаболических и гормональных расстройств, что приводит к андрогенному дефициту и нарушению сперматогенеза. Для коррекции репродуктивных дисфункций могут быть использованы антидиабетические препараты, включая метформин (МФ), и агонисты рецептора лютеинизирующего гормона (ЛГР), активирующие тестикулярный стероидогенез. Однако при диета-индуцированном ожирении (ДИО) эффективность и механизмы их действия мало изучены.
Цель. Оценить восстанавливающий эффект МФ, хорионического гонадотропина человека (ХГЧ) и аллостерического ЛГР-агониста ТП03, различающихся по природе и механизмам действия, на уровни тестостерона, сперматогенез и морфологию семенных канальцев у самцов крыс с ДИО.
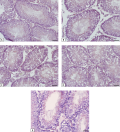
Материалы и методы. Ожирение у самцов крыс Wistar вызывали 23-недельной диетой, обогащенной насыщенными жирами. Обработку МФ проводили в течение 5 нед в дозе 120 мг/кг/сут (перорально), обработку ХГЧ и ТП03 — в течение 5 сут в суточных дозах 20 МЕ/крысу (п/к) и 15 мг/кг (в/б) соответственно. С помощью микроскопии и гистохимического анализа оценивали число и подвижность сперматозоидов (СП), число их дефектных форм и морфологию семенных канальцев, с помощью иммуноферментного анализа — уровни тестостерона и других гормонов в крови.
Результаты. МФ, ХГЧ и ТП03 в различной степени повышали сниженные у ДИО-крыс количество СП и долю их подвижных форм, в том числе с поступательным движением, нормализовали толщину эпителия семенных канальцев и количество в них сперматогониев и пахитеновых сперматоцитов, но не снижали повышенную при ДИО долю дефектных СП. В случае МФ это было ассоциировано с вызываемыми этим препаратом нормализацией массы тела, толерантности к глюкозе, уровней инсулина и лептина у ДИО-крыс. Положительное влияние ХГЧ и ТП03 на сперматогенез было обусловлено их стимулирующим эффектом на продукцию тестостерона.
Заключение. Применение длительной МФ-терапии и краткосрочных курсов ЛГР-агонистов нормализует нарушенный при ДИО сперматогенез, что указывает на перспективы их использования для улучшения мужской фертильности при ожирении, причем в случае МФ ключевое значение имеет нормализация метаболического и гормонального статуса, а в случае ЛГР-агонистов — их стероидогенный эффект.
Обоснование. Среди многочисленных причин ожирения особое место занимают генетические факторы. Очевидная роль среди них принадлежит генетическому полиморфизму ферментов метаболизма липидов, и в том числе параоксоназе-1 (РОN-1). До настоящего времени остается неясным характер взаимоотношения полиморфизма PON-1 и состояния эндокринной функции мезенхимальных тканей. Его изучение позволит пролить свет на тонкие механизмы развития ожирения в детском и подростковом возрасте.
Цель. Изучение взаимосвязи полиморфизма PON-1 (rs662) с характером сдвигов в содержании адипокинов, миокинов и показателей липидного обмена в крови у детей и подростков разного пола с ожирением.
Материалы и методы. У 100 здоровых детей и подростков разного пола и 89 их сверстников с ожирением было проведено генетическое исследование по оценке однонуклеотидного полиморфизма гена PON-1 (rs662). В сыворотке крови проводилось определение общего холестерола, холестерола липопротеинов высокой, низкой и очень низкой плотности, триацилглицеролов, глюкозы и активности аминотрансфераз (аланинаминотрансферазы и аспартатаминотрансферазы) фотометрическими методами, а также лептина, адипонектина, резистина, апелина, ирисина, адипсина, миостатина, FGF21, остеокрина, онкостатина и инсулина методом мультиплексного ИФА, аспросина — иммуноферментным методом.
Результаты. У гомозигот по аллели Arg192/Arg ограничивается развитие осложнений ожирения у мальчиков и предупреждается их возникновение у девочек. При других вариантах генотипа PON-1 (генотипы Gln192/Gln и Gln192/Arg) в организме девочек формируются защитные механизмы, направленные на предупреждение осложнений при ожирении и их выраженности. У мальчиков с генотипом Gln192/Gln при ожирении выявляются более выраженные сдвиги со стороны показателей липидного обмена, проявления альтерации и увеличение массы жировой ткани, а у детей и подростков с гетерозиготным генотипом Gln192/Arg, усиливаются процессы атерогенеза.
Заключение. Полиморфизм гена параоксоназы (rs662) вносит вклад в появление гендерных различий в изменении содержания в крови адипокинов и миокинов при ожирении в детском и подростковом возрасте.
ОБЗОР
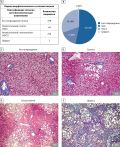
Неалкогольная жировая болезнь печени (НАЖБП) представляет собой заболевание печени с характерным накоплением жировых включений в гепатоцитах и включает спектр поражений печени от стеатоза до цирроза. Ввиду роста заболеваемости ожирением и связанной с ним НАЖБП проводится поиск оптимальных методов лечения. Авторами проведен анализ опубликованных клинических исследований по влиянию бариатрических операций на морфологические изменения в печени. Поиск литературы проводился по ключевым словам «неалкогольная жировая болезнь печени», «ожирение», «бариатрическая хирургия» в базах Pubmed и еLibrary.ru за период с 1990 по 2022 гг. Рассмотрены как положительные эффекты хирургического лечения ожирения в виде уменьшения степеней стеатоза и стеатогепатита, так и неблагоприятные последствия в виде усугубления цирроза у пациентов после перенесенной операции. Несмотря на очевидную эффективность бариатрических операций в отношении компонентов метаболического синдрома, связанных с ожирением, до сих пор не существует однозначного мнения об их эффективности в отношении НАЖБП.
Мезенхимальные стволовые клетки, полученные из жировой ткани, представляют собой взрослые стволовые клетки, наделенные мультипотентными способностями и иммуномодулирующими свойствами, как и мезенхимальные стволовые клетки другого происхождения. Многочисленные исследования показывают, что стволовые клетки жировой ткани участвуют в патологическом процессе могут проявлять провоспалительные свойства и привлекать воспалительные иммунные клетки по соседству. Впоследствии воспаление создает микросреду, приводящую к дисфункции жировой ткани. Примерами такого процесса являются ожирение и сахарный диабет 2 типа, при котором нарушается адипогенез и инициируется резистентность к инсулину. Цель этого обзора состоит в том, чтобы понять роль стволовых клеток жировой ткани в патогенезе ожирения и сахарного диабета 2 типа.
Одной из причин неопухолевой гиперпролактинемии является прием ряда лекарственных препаратов. С гиперпролактинемией как побочным эффектом медикаментозной терапии в своей практической деятельности встречаются врачи различных специальностей: кардиологи, гастроэнтерологи, эндокринологи, неврологи, но чаще всего она наблюдается в практике врача-психиатра при лечении пациентов психотропными препаратами. За последние несколько лет отмечается повышение частоты назначений антидепрессантов и нейролептиков в связи с постковидным синдромом, тревожностью и стрессом, вызванными пандемией новой коронавирусной инфекции. Также существует предрасположенность к развитию гиперпролактинемии на фоне приема нейролептиков из-за генетических особенностей пациентов. В настоящее время в мире не существует установленного общего алгоритма диагностики и лечения лекарственно-индуцированной гиперпролактинемии. В статье на основе обзора зарубежной и отечественной литературы подробно обсуждаются механизмы развития и различные подходы к коррекции ятрогенной (лекарственной) гиперпролактинемии, проводится оценка пролактогенной активности нейролептиков, предлагаются алгоритмы мониторинга пролактина и коррекции гиперпролактинемии с использованием агонистов дофамина. Часто тактику ведения таких пациентов необходимо обсуждать командой врачей-специалистов.
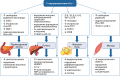
Железо оказывает влияние на формирование и клиническое течение таких хронических метаболических заболеваний, как ожирение, атеросклероз, неалкогольная жировая болезнь печени и сахарный диабет 2 типа. Высокая прооксидантная активность железа физиологически контролируется механизмами, регулирующими поступление, циркуляцию и потерю данного металла организмом. Эти механизмы включают взаимодействие железа с ферритином, трансферрином, гепсидином, инсулином, а также адипокинами и провоспалительными молекулами. Дисбаланс регулирующих обмен железа факторов приводит к развитию системного и паренхиматозного сидероза. Перегрузка железом обладает повреждающим эффектом в отношении основных тканей, участвующих в обмене липидов и глюкозы, — β-клеток поджелудочной железы, печени, мышечной и жировой тканей, а также в отношении органов, подверженных поражению в условиях хронической гипергликемии, — головного мозга, сетчатки и почек. Гиперферритинемия приводит к снижению секреции инсулина, формированию инсулинорезистентности и усилению глюконеогенеза в печени. Молекулярные механизмы данных эффектов железа разнообразны, и их изучение может способствовать ранней диагностике и профилактике нарушений углеводного обмена, а также расширению представлений о патогенезе других заболеваний, ассоциированных, как и сахарный диабет 2 типа, с питанием, старением и уровнем железа. В обзоре литературы приведены данные мировых исследований, посвященных взаимному влиянию метаболизма глюкозы и перегрузки железом, а также обсуждаются различия между наследственными и приобретенными нарушениями обмена железа с позиции их влияния на углеводный обмен.
КЛИНИЧЕСКИЙ СЛУЧАЙ
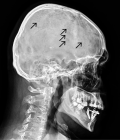
В данной статье представлен нестандартный клинический случай неочевидности причин вторичного остеопороза в рутинной практике врача-эндокринолога амбулаторного и стационарного профилей. В этой работе демонстрируется достаточно редкая ситуация, включающая в себя выявление у пациента нетипичных клинических проявлений остеопороза, а именно наличие у молодого мужчины жалоб на общую слабость, выраженный болевой синдром в позвоночнике, вынуждающий к ежедневному приему нестероидных противовоспалительных средств, снижение двигательной активности, и лабораторных показателей, таких как гиперкальциемия, гиперкальциурия на фоне референсных значений паратгормона, гиперпротеинемии и повышения СОЭ. С учетом описанной выше клинической картины неотъемлемой частью дальнейшего верного диагностического поиска является исключение эндокринных заболеваний, которые обусловливают снижение минеральной плотности костной ткани. Параллельно инициированное назначение патогенетически обоснованного лечения вторичного остеопороза является важным составляющим компонентом в рамках данного заболевания. Применение подобного многопрофильного подхода привело к своевременной верификации основного онкогематологического заболевания и маршрутизации пациента в специализированный стационар, позволило предотвратить необратимые изменения, ассоциированные с критическим снижением минеральной плотности костной ткани, и улучшить качество жизни пациента.

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).
ISSN 2306-5524 (Online)