Перейти к:
Особенности функционирования жировой ткани у мужчин на фоне андрогенного дефицита при сахарном диабете 2 типа
https://doi.org/10.14341/omet13223
Аннотация
Обоснование. Андрогенный дефицит, часто верифицируемый у пациентов с сахарным диабетом 2 типа (СД2), является одним из компонентов метаболического синдрома, которому сопутствует висцеральное ожирение. Патогенетические особенности функционирования жировой ткани пациентов при сочетании таких патологий, как СД2 и гипогонадизм, изучены чрезвычайно мало.
Цель. Оценить влияние андрогенного дефицита на параметры метаболизма и секрецию адипогормонов жировой тканью у мужчин, страдающих СД2.
Материалы и методы. Пациентам с СД2 и гипогонадизмом выполняли ряд общеклинических исследований, изучали степень нарушения обмена углеводов и жиров, в том числе индекс накопления липидов LAP, а также уровни общего тестостерона (Т), глобулина, связывающего половые гормоны, свободного Т, дегидроэпиандростерона, простатического специфического антигена и адипогормонов (адипонектина, резистина и лептина).
Результаты. В исследовании приняли участие 276 пациентов мужского пола с СД2 (в возрасте 54,0 (8,0) года) с сопоставимым стажем СД2 (длительностью 5,0 (6,0 лет), которые были разделены на 2 группы: 1 — больные с подтвержденным гипогонадизмом (n=124); 2 — эугонадные пациенты (n=152).
Наряду с более выраженными инсулинорезистентностью, гиперинсулинемией, дислипидемией и индексом LAP у мужчин, имеющих СД2 в сочетании с гипогонадизмом, нарушения секреторной активности адипозной ткани более значимы, чем у эугонадных пациентов: уменьшенный в 1,7 раза уровень адипонектина (р=0,006), увеличенная концентрация лептина на 18,4% (р=0,03) и резистина в 2 раза (р<0,001).
Заключение. Дефицит Т у мужчин с СД2 усугубляет нарушения обмена жиров и углеводов, а также дисфункцию жировой ткани, являющиеся патофизиологической основой для кардиометаболических заболеваний.
Ключевые слова
Для цитирования:
Хрипун И.А., Кузьменко Н.А., Алексеева Н.С., Иващенко С.О., Хрипун Н.А. Особенности функционирования жировой ткани у мужчин на фоне андрогенного дефицита при сахарном диабете 2 типа. Ожирение и метаболизм. 2025;22(4):319-325. https://doi.org/10.14341/omet13223
For citation:
Khripun I.A., Kuzmenko N.A., Alexeeva N.S., Ivaschenko S.O., Khripun N.A. Features of adipose tissue function against the background of androgen deficiency in men with type 2 diabetes mellitus. Obesity and metabolism. 2025;22(4):319-325. (In Russ.) https://doi.org/10.14341/omet13223
ОБОСНОВАНИЕ
Заболеваемость сахарным диабетом 2 типа (СД2) и ожирением продолжает стремительно увеличиваться в глобальных масштабах, превращая эти патологии в одну из наиболее острых и актуальных проблем современной медицины. Эти состояния, тесно взаимосвязанные между собой, не только снижают качество жизни миллионов людей, но и создают значительную нагрузку на системы здравоохранения по всему миру [1]. Особое беспокойство вызывает СД2, который часто сопровождается гипогонадизмом у мужчин. Согласно исследованиям, более чем у 33,7% мужчин с СД2 наблюдается дефицит тестостерона, что подчеркивает тесную связь между этими состояниями [2]. Ожирение, в свою очередь, выступает неизменным спутником СД2, и среди пациентов с этим диагнозом доля лиц, страдающих предожирением или ожирением, достигает внушительных 90%. Это тревожное сочетание не только усугубляет течение заболевания, но и создает дополнительные риски для здоровья, подчеркивая необходимость комплексного подхода к лечению и профилактике [3][5]. По данным за 2022 г., около 13% взрослого населения страдают ожирением, и прогнозы неутешительны: к 2025 г. каждый 5‑й взрослый может столкнуться с этой проблемой [4].
Многочисленные исследования свидетельствуют о наличии обратной зависимости между уровнем тестостерона у мужчин и риском развития СД2 [6]. У пациентов, страдающих гипогонадизмом, вероятность возникновения данного заболевания существенно возрастает, особенно на фоне декомпенсации углеводного обмена. Так, при уровне гликированного гемоглобина, превышающем 10%, риск развития гипогонадизма становится особенно выраженным [7]. Андрогенный дефицит и нарушения углеводного обмена взаимно усиливают друг друга, создавая порочный круг, который приводит к более тяжелому течению СД2 и его осложнений. Это подчеркивает необходимость комплексного подхода к диагностике и лечению данных состояний для улучшения прогноза и качества жизни пациентов [2][8].
Андрогенный дефицит оказывается тесно связанным не только с СД2, но также с множеством других метаболических и сердечно-сосудистых заболеваний. К числу этих патологий относятся висцеральное ожирение, артериальная гипертензия, ишемическая болезнь сердца и неалкогольная жировая болезнь печени [9]. Каждое из этих состояний в значительной мере негативно сказывается на качестве жизни пациентов, повышая вероятность развития серьезных осложнений и риск преждевременной смерти. Исследования показывают, что смертность среди пациентов, страдающих СД2 в сочетании с дефицитом тестостерона, значительно превышает таковую у людей, у которых уровень этого гормона находится в пределах нормы [10]. Таким образом, серьезные последствия, связанные с дефицитом тестостерона, подчеркивают важность его мониторинга и корректировки в клинической практике для сохранения здоровья и улучшения качества жизни мужчин.
Жировая ткань на сегодняшний день рассматривается не только как энергетическое депо, но и как активный эндокринный орган, синтезирующий гормоны и биологически активные вещества. Ее роль выходит далеко за пределы хранения энергии, влияя на множество метаболических процессов и способствуя сложным взаимодействиям в организме. Одним из ключевых ферментов, участвующих в метаболизме жировой ткани, является ароматаза, которая превращает андрогены в эстрогены, и при увеличении массы жировой ткани активность данного фермента неуклонно растет. Таким образом, происходит нарушение гипоталамо-гипофизарной регуляции синтеза тестостерона клетками Лейдига вследствие увеличения секреции эстрогенов в организме мужчин, страдающих ожирением, что подавляет выработку лютеинизирующего гормона (ЛГ) и усиливает секрецию пролактина [4]. Высокий уровень эстрогенов, кроме того, стимулирует гиперплазию адипоцитов, скорость которой превышает темпы неоангиогенеза для адекватного снабжения новых клеток кислородом, и которая является одним из механизмов, провоцирующих нарушения функциональной активности жировой ткани, на фоне нарастающей гипоксии, наряду с хроническим воспалением, ремоделированием экстрацеллюлярного матрикса и секрецией адипокинов [4][12]. Этот процесс усугубляет метаболические нарушения и повышает риск развития СД2. Дисфункция жировой ткани является ключевым звеном между гипогонадизмом и нарушениями углеводного обмена.
В условиях современного мира, когда проблемы с избыточным весом и метаболическими нарушениями приобретают угрожающие масштабы, понимание роли тестостерона в регуляции функций жировой ткани становится особенно актуальным и важным для разработки эффективных методов профилактики и лечения данных состояний.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Оценить влияние андрогенного дефицита на параметры метаболизма и секрецию адипогормонов жировой тканью у мужчин, страдающих СД2.
МАТЕРИАЛЫ И МЕТОДЫ
Место и время проведения исследования
Место проведения. Исследование было проведено на базе отделения эндокринологии клиники ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России.
Время исследования. Включение участников в исследование осуществлялось в период с 2014 по 2018 гг.
Изучаемые популяции
В исследовании приняли участие мужчины с СД2. Ключевым фактором, определяющим распределение участников по двум группам, стало наличие или отсутствие гипогонадизма.
Критерии включения: мужской пол, возраст пациента не менее 40 лет, длительность СД2 более 12 месяцев, сахароснижающая терапия включала только пероральные лекарственные препараты.
Критерии исключения: установленный ранее первичный или вторичный гипогонадизм (классические формы), гиперпролактинемический синдром, установленный прием андрогенсодержащих препаратов или анаболических стероидов, нарушения функции щитовидной железы, онкологические заболевания, тяжелые формы почечной или печеночной недостаточности.
Способ формирования выборки из изучаемой популяции
В исследовании была использована выборка пациентов с СД2 и гипогонадизмом, сформированная методом сплошного включения наблюдений. Группа сравнения состояла из эугонадных пациентов с СД2, сопоставимых по полу, возрасту, антропометрическим данным и длительности сахарного диабета. Формирование этой группы осуществлялось случайным образом.
Дизайн исследования
Исследование было одноцентровым, одномоментным, проспективным и сравнительным.
Описание медицинского вмешательства
В рамках исследования осуществляли тщательный анализ анамнеза жизни и истории болезни каждого пациента, фиксировали текущие жалобы, проводили измерения ключевых антропометрических параметров (масса тела, рост, окружность бедер и окружность талии (ОТ), а также рассчитывали индекс массы тела (ИМТ). У всех участников натощак производили забор венозной крови в объеме 10 мл. Свежую сыворотку использовали для биохимического анализа, а замороженную (-20 °C) — для иммуноферментных исследований. Биохимический анализ включал определение следующих показателей: уровня иммунореактивного инсулина, глюкозы крови, индекса инсулинорезистентности HOMA, а также гликированного гемоглобина (HbA1c) и показателей липидограммы, включая общий холестерин (ОХС), триглицериды (ТГ) и липопротеиды низкой плотности (ЛПНП). Кроме того, исследовали концентрации следующих гормонов: общего тестостерона (Т), глобулина, связывающего половые гормоны (ГСПГ), расчетного свободного Т, дегидроэпиандростерона (ДГЭА), простатического специфического антигена (ПСА). Помимо этого, определяли содержание резистина, лептина и адипонектина, которые служат ключевыми маркерами секреторной функции жировой ткани.
Методы
Участники исследования с СД2, включенные в данное исследование, были разделены на две группы в зависимости от наличия гипогонадизма: пациенты с гипогонадизмом составили 1-ю группу, а мужчины с эугонадизмом — 2-ю.
Анализатор «Bayer ADVIA 1650» использовали для проведения оценки параметров гликемии и липидного профиля, в то время как анализатор «Siemens Healthcare Diagnostics DCA 2000+» был использован для определения НbА1с. Для оценки выраженности инсулинорезистентности проводили расчет коэффициента НОМА.
Индекс накопления липидов LAP (Lipid Accumulation Product) применяли для комплексной оценки метаболического и кардиоваскулярного рисков, вычисляя его по установленной формуле: [ ОТ (см) – 65] х [ТГ (ммоль/л)] [13][14].
В процессе исследования использовали фотометр «Zenyth 340» для проведения иммуноферментного анализа. Для определения концентрации гормона ДГЭА и ПСА применяли наборы реагентов «Алкор-Био» (Россия). Уровень ГСПГ определяли с помощью тест-системы «DRG Elisa» (Германия). Содержание лептина, резистина и адипонектина определяли с помощью наборов «Mediagnost» (Германия), «Биовендер Лаборатори» (Чешская Республика) и «eBioscience» (Австрия) соответственно.
Этическая экспертиза
Проведение исследования и получение информированного согласия от пациентов были одобрены локальным независимым этическим комитетом Ростовского государственного медицинского университета (протокол №13/14 от 11.09.2014). Все пациенты до начала участия в исследовании подписали документы информированного согласия, подтверждая тем самым свое добровольное согласие.
Статистический анализ
Методы статистического анализа данных: для статистической обработки данных использовалось программное обеспечение Statistica 10.0 (StatSoft Inc., США). Нормальность распределения переменных была проверена с помощью критерия Колмогорова-Смирнова. Данные представлены в виде медиан и интерквартильного размаха. Для сопоставления групп по качественным признакам был использован непараметрический метод χ² с поправкой Йетса, а для сравнения количественных признаков был применен U-тест Манна-Уитни. Различие при значении р<0,05 считалось статистически значимым.
Основные исходы исследования
За основные показатели исследования были приняты уровни содержания гормонов жировой ткани в крови — резистина, адипонектина и лептина.
Дополнительно были изучены значения показателей метаболизма жиров и углеводов, индекс LAP, а также антропометрические данные.
РЕЗУЛЬТАТЫ
В ходе исследования, охватившего 276 мужчин с типом 2 сахарного диабета (СД2), средний стаж заболевания составил 5,0 (6,0) года, а медианный возраст участников — 54,0 (8,0) года. Пациенты были разделены на две группы в соответствии с диагностическими критериями гипогонадизма, установленными Европейской ассоциацией урологов (2014) и Российской ассоциацией эндокринологов (2017). Первую группу составили пациенты с выявленными признаками гипогонадизма (n=124), вторую — пациенты без таких признаков (n=152). Обе группы были сопоставимы по продолжительности СД2, возрасту и основным антропометрическим показателям (табл. 1).
Таблица 1. Антропометрические параметры
|
Параметр |
группа 1 |
группа 2 |
p |
|
Возраст, лет |
54,0 (8,0) |
53,0 (8,5) |
0,661 |
|
Длительность СД2, лет |
5,0 (6,0) |
5,0 (8,0) |
0,414 |
|
ОТ, см |
112 (17,0) |
112 (11,0) |
0,162 |
|
ОБ, см |
110 (12,0) |
108 (11,0) |
0,128 |
|
Масса тела, кг |
103 (20,0) |
101,0 (13,0) |
0,143 |
|
ИМТ, кг/м² |
32,8 (5,5) |
32,7 (3,6) |
0,130 |
Примечания: ОТ — окружность талии, ОБ — окружность бедер, ИМТ — индекс массы тела.
Различие между группами по данным антропометрическим параметрам не являлось статистически значимым (р>0,05).
Основные результаты исследования
В соответствии с критериями, по которым производилось деление больных на две группы, их значения заметно отличались друг от друга концентрацией общего Т и свободного Т (р<0,001). Помимо этого, у мужчин второй группы уровень ГСПГ значимо выше, чем в первой (р=0,002) (табл. 2).
Таблица 2. Сывороточные уровни половых гормонов
|
Параметр |
группа 1 |
группа 2 |
р |
|
Т общий, нмоль/л |
10,1 (3,7) |
17,3 (5,8) |
<0,001 |
|
Т свободный, нмоль/мл |
212 (90,0) |
362 (156,0) |
<0,001 |
|
ГСПГ, нмоль/л |
26,1 (19,7) |
31,0 (24,5) |
0,002 |
|
ДГЭА, мкг/мл |
2,0 (2,7) |
2,0 (1,8) |
0,523 |
Примечания: Т — тестостерон, ГСПГ — глобулин, связывающий половые гормоны, ДГЭА — дегидроэпиандростерон.
Показатели ПСА в каждой из групп пациентов были сопоставимы и находились в диапазоне референсных значений: 0,9 (1,2) нг/мл в группе 1 и 0,9 (1,1) нг/мл в группе 2 (р=0,766).
С результатами анализа состояния липидного обмена можно ознакомиться на рисунке 1.

Рисунок 1. Результаты анализа состояния липидного обмена.
У пациентов, входящих в группу 1, обнаружено статистически значимое повышение концентрации ОХС на 11,3% (р=0,048), а также ТГ на 28% (р<0,001). Одновременно у пациентов 1‑й группы относительно 2‑й наблюдалось повышение следующих показателей: ЛПНП — на 9,5% (р=0,02) и липопротеидов очень низкой плотности (ЛПОНП) — в 1,4 раза (р<0,001). Содержание липопротеидов высокой плотности (ЛПВП) в обеих группах пациентов было сопоставимо (р=0,74). Медиана индекса атерогенности в группе 1 составила 2,9 (0,7), что на 9,5% больше, чем в группе 2, — 2,6 (0,5) (р=0,007).
Значение комбинированного показателя метаболического риска (индекса LAP) у мужчин с гипогонадизмом составило 103 (85,8) единицы и было в 1,5 раза больше по сравнению с эугонадными пациентами, у которых индекс LAP составил 71 (44,3) единицу (р<0,001).
С содержанием адипогормонов можно ознакомиться на рисунке 2.
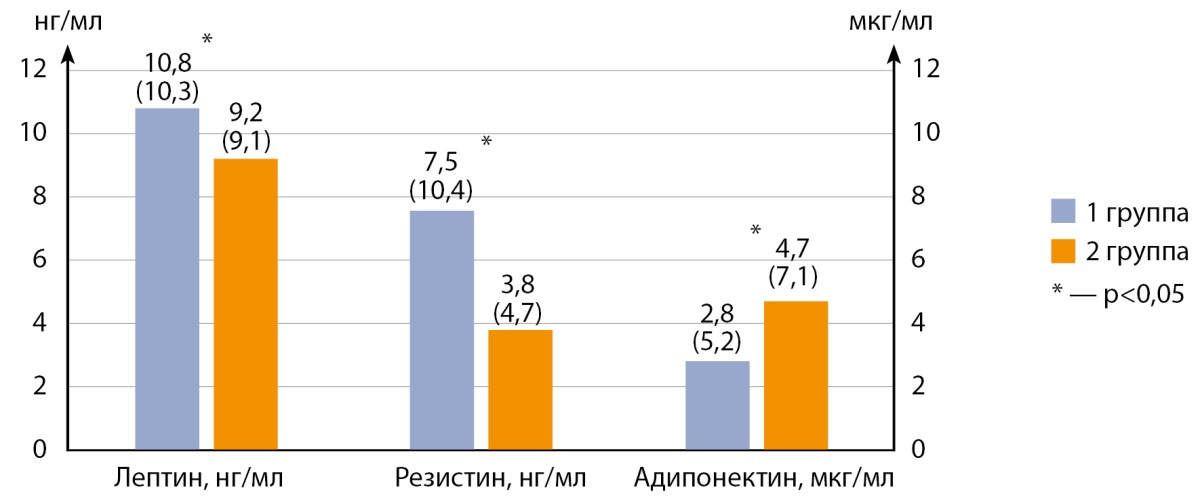
Рисунок 2. Содержание адипогормонов.
У пациентов с гипогонадизмом уровень адипонектина был меньше в 1,7 раза (р=0,006), концентрации лептина и резистина — больше на 18,4% (р=0,03) и в 2 раза (р<0,001) соответственно по сравнению с эугонадными мужчинами.
Дополнительные результаты исследования
Углеводный обмен в каждой группе оценивали путем анализа уровней следующих показателей: глюкозы натощак (ммоль/л), гликированнго гемоглобина (HbA1c, %), иммунореактивного инсулина (ИРИ, мкМЕ/мл) и индекса HOMA (ед.).
Уровень гликемии натощак в обеих группах не имел значимых отличий (группа 1 — 7,8 (4,2) ммоль/л, группа 2 — 7,9 (3,2) ммоль/л, p=0,661), показатели HbA1c в каждой группе также оказались сопоставимы (группа 1 — 7,9 (3,5)%, группа 2 — 7,7 (2,5) %, p=0,198), хотя медиана и интерквартильный размах уровня HbA1c в группе 1 имеют более высокие значения. Значения ИРИ в 1 и 2 группе составили: 1 — 6,2 (7,2) мкМЕ/мл и 2 — 12,7 (12,6) мкМЕ/мл соответственно. Различие в показателях выраженности гиперинсулинемии между группой 1 и группой 2 составило 27,6% (p=0,002). Индекс HOMA в 1 группе — 6,2 (7,2) ед., во 2 группе — 4,6 (4,2) ед., p<0,001. У пациентов с гипогонадизмом наблюдается статистически значимое увеличение в 1,3 раза индекса HOMA (р<0,001).
Нежелательные явления
В данном научном исследовании нежелательных реакций и явлений зарегистрировано не было.
ОБСУЖДЕНИЕ
Проведен анализ данных 276 пациентах мужского пола, имеющих в анамнезе СД2. В ходе исследования удалось установить взаимосвязь между наличием гипогонадизма и нарушением функции жировой ткани. При комплектовании групп исследования особое внимание уделялось антропометрическим параметрам участников, что позволило обеспечить их сопоставимость. Тем не менее полученные результаты исследования свидетельствуют о том, что у пациентов с сахарным диабетом 2 типа и гипогонадизмом наблюдаются более неблагоприятные показатели липидного профиля по сравнению с мужчинами, не имеющими нарушений продукции тестостерона. Эти данные подчеркивают важность учета гормональных факторов при оценке метаболических рисков у данной категории пациентов. Данная тенденция проявляется в повышенном уровне общего холестерина, триглицеридов и липопротеинов низкой плотности. Важно отметить, что индекс LAP у пациентов с гипогонадизмом был в 1,5 раза выше по сравнению с пациентами с нормальным уровнем Т. Ранее проведенные исследования уже продемонстрировали тесную связь данного индекса с показателями ИМТ и концентрацией лептина в крови [13][14], тогда как его связь с гипогонадизмом у мужчин вне зависимости от выраженности висцерального ожирения продемонстрирована впервые. Поскольку индекс LAP выступает не только в роли предиктора метаболических нарушений, но и является важным фактором риска сердечно-сосудистых заболеваний, таких как артериальная гипертензия и ишемическая болезнь сердца, его значение нельзя недооценивать [15]. Учитывая его доступность, экономичность и простоту расчета при высокой прогностической значимости, более активное внедрение данного индекса в клиническую практику представляется крайне важным и целесообразным шагом.
Анализ углеводного обмена у пациентов с СД2 выявил следующую закономерность: несмотря на схожие показатели уровня гликемии и HbA1c в исследуемых группах, у мужчин с гипогонадизмом отмечалось выраженное усиление инсулинорезистентности и развитие гиперинсулинемии. Это находит подтверждение в результатах других исследований, которые подчеркивают, что дефицит тестостерона оказывает значительное влияние на развитие и ухудшение инсулинорезистентности у мужчин с СД2. С другой стороны, эти данные указывают на то, что данная проблема продолжает оставаться незамеченной в рамках клинических наблюдений, основанных только на стандартных исследованиях углеводного обмена, таких как уровень гликемии и HbA1c. Подчеркивается необходимость определения уровня иммунореактивного инсулина и индекса HOMA у этой категории больных. Такое воздействие гипогонадизма нарушает компенсаторные механизмы углеводного обмена и выступает в роли важного звена патогенеза, способствующего развитию коморбидных состояний.
Известно, что нарушение функции жировой ткани является непосредственным триггером в развитии инсулинорезистентности [17]. В ходе исследования было выявлено, что при схожей степени выраженности висцерального ожирения в исследуемых группах наблюдались существенные различия в концентрации адипокинов, что подчеркивает их ключевую роль в метаболических процессах. Иными словами, в данном случае гипогонадизм у пациентов мужского пола провоцирует дисфункциональные нарушения секреторной активности адипоцитов, о чем свидетельствует повышение содержания лептина и резистина в сыворотке крови. Недавние исследования показали, что гиперрезистинемия не только приводит к усугублению имеющейся инсулинорезистентности, увеличивая метаболические риски, но и снижает подвижность и жизнеспособность сперматозоидов, что ухудшает фертильность мужчины [18].
Вместе с тем выявлено одновременное уменьшение в 1,7 раза концентрации адипонектина, который, в свою очередь, по результатам последних исследований, существенно влияет на экспрессию генов стероидогенеза в клетках Лейдига [19]. Такое соотношение адипокинов может подавлять синтез Т клетками Лейдига и приводить к усугублению его дефицита в организме. Кроме того, гипоадипонектинемия сопровождается у мужчин с ожирением не только инсулинорезистентностью, но и резистентностью к адипонектину [18], что парадоксально повышает риски кардиоваскулярных заболеваний у данной категории больных [20].
Таким образом, дисбаланс в синтезе гормонов жировой ткани играет важнейшую роль не только в развитии инсулинорезистентности, но и в регуляции выработки половых гормонов, что подчеркивает их взаимосвязь в поддержании метаболического и репродуктивного здоровья.
Результаты нашего исследования доказывают, что у мужчины с СД2 и гипогонадизмом по сравнению с мужчиной без такового, при одинаковом количестве висцерального жира, из-за более выраженной дисфункции жировой ткани будет наблюдаться худший кардиометаболический прогноз.
Ограничения исследования
Данное исследование проводилось на пациентах с уже диагностированным СД2, в связи с чем существует ограничение в невозможности переноса в полной мере полученных результатов на более широкую группу пациентов мужского пола с гипогонадизмом, который не связан с нарушениями углеводного обмена.
Направления дальнейших исследований
Научный интерес представляет дальнейшее изучение эффективности и безопасности заместительной гормональной терапии Т в уменьшении кардиометаболических рисков с учетом нормализации функции жировой ткани у мужчин с гипогонадизмом.
ЗАКЛЮЧЕНИЕ
Недостаток тестостерона является важным фактором, который значительно влияет на здоровье мужчин, страдающих сахарным диабетом 2 типа. Необходимо подчеркнуть, насколько критична его роль в формировании различных метаболических расстройств, включая инсулинорезистентность, гиперинсулинемию и дислипидемию, несмотря на сопоставимый объем висцеральной жировой ткани по сравнению с эугонадными пациентами. С другой стороны, гипогонадизм у этих пациентов становится причиной возникновения дисфункциональных нарушений в секреторной активности адипоцитов. Это проявляется, в частности, в более значительном увеличении уровня лептина и резистина в сыворотке крови, что наглядно демонстрирует сложные взаимодействия между гормональным фоном и метаболизмом жировой ткани. Эти изменения подчеркивают негативное влияние дефицита тестостерона, вызывая серьезные отклонения в регуляции обмена веществ и усугубляя существующие проблемы, связанные с сахарным диабетом. В совокупности данные факты указывает на ключевую роль дефицита Т в развитии метаболических расстройств и нарушении функции жировой ткани у мужчин при СД2.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источник финансирования. Грант № 14-25-00052 Российского научного фонда (РНФ).
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Хрипун И.А. — концепция и разработка исследования, подбор участников, анализ полученных данных, а также составление текста. Кузьменко Н.А. — набор пациентов в исследование, коррекция текста. Алексеева Н.С. — статистический анализ данных, коррекция текста. Иващенко С.О. — анализ полученных данных, написание текста. Хрипун Н.А. — статистический анализ данных, написание текста.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Magliano DJ, Boyko EJ; IDF Diabetes Atlas 10th edition scientific committee. IDF DIABETES ATLAS [Internet]. 10th ed. Brussels: International Diabetes Federation; 2021
2. Мельниченко Г.А., Шестакова М.В., Роживанов Р.В. Распространенность синдрома гипогонадизма у мужчин с сахарным диабетом типа 2 в условиях рутинной клинической практики // Сахарный диабет. — 2019. — Т. 22. — №2. — С. 127-130. doi: https://doi.org/10.14341/DM9944
3. Giagulli VA, Castellana M, Murro I, Pelusi C, Guastamacchia E, Triggiani V, De Pergola G. The Role of Diet and Weight Loss in Improving Secondary Hypogonadism in Men with Obesity with or without Type 2 Diabetes Mellitus. Nutrients. 2019;11(12):2975. doi: https://doi.org/10.3390/nu11122975
4. Genchi VA, Rossi E, Lauriola C, D'Oria R, Palma G, et al. Adipose Tissue Dysfunction and Obesity-Related Male Hypogonadism. Int J Mol Sci. 2022;23(15):8194. doi: https://doi.org/10.3390/ijms23158194
5. Bays HE, Bindlish S, Clayton TL. Obesity, diabetes mellitus, and cardiometabolic risk: An Obesity Medicine Association (OMA) Clinical Practice Statement (CPS) 2023. Obes Pillars. 2023;5:100056. doi: https://doi.org/10.1016/j.obpill.2023.100056
6. Chen XJ. Analysis of Sex Hormones, Insulin Dosage, and Risk Factors Associated With Male Diabetic Patients. Am J Mens Health. 2024;18(2):15579883241235062. doi: https://doi.org/10.1177/15579883241235062
7. Хрипун И.А. Риск развития дефицита тестостерона у мужчин с сахарным диабетом 2 типа в зависимости от уровня гликированного гемоглобина аналитические обзоры / И.А. Хрипун, Н.А. Кузьменко, А.С. Ахмедова // Эндокринология. Новости. Мнения. Обучение. — 2023. — Т. 12. — № 4(45). — С. 50-54. doi: https://doi.org/10.33029/2304-9529-2023-12-4-50-54
8. Caretta N, Facondo P, Mereu S, Delbarba A, Crepaldi MC, Vedovato M, Avogaro A, Ferlin A. Cardiometabolic indices predict hypogonadism in male patients with type 2 diabetes. J Endocrinol Invest. 2023;46(3):599-608. doi: https://doi.org/10.1007/s40618-022-01941-0
9. Хрипун И.А. Дефицит тестостерона и неалкогольная жировая болезнь печени у мужчин с сахарным диабетом 2 типа / И.А. Хрипун, С.В. Воробьев, Я.С. Аллахвердиева // Сахарный диабет. — 2019. — Т. 22. — № 6. – С. 542-549. doi: https://doi.org/10.14341/DM10232
10. Hackett G, Kirby M, Rees RW, Jones TH, Muneer A, et al. The British Society for Sexual Medicine Guidelines on Male Adult Testosterone Deficiency, with Statements for Practice. World J Mens Health. 2023;41(3):508-537. doi: https://doi.org/10.5534/wjmh.221027
11. Alemany M. The Metabolic Syndrome, a Human Disease. Int J Mol Sci. 2024;25(4):2251. doi: https://doi.org/10.3390/ijms25042251
12. Funcke JB, Scherer PE. Beyond adiponectin and leptin: adipose tissue-derived mediators of inter-organ communication. J Lipid Res. 2019;60(10):1648-1684. doi: https://doi.org/10.1194/jlr.R094060
13. Ayundini G, Astrella C, Tahapary D, Soewondo P. A Systematic Review on the Association between Lipid Accumulation Product Index and Type 2 Diabetes Mellitus. J ASEAN Fed Endocr Soc. 2019;34(1):16-20. doi: https://doi.org/10.15605/jafes.034.01.04
14. Хрипун И.А. Новый маркер метаболических нарушений у мужчин с сахарным диабетом 2 типа / И.А. Хрипун, С.В. Воробьев, М.И. Коган // Медицинский вестник Юга России. — 2016. — №1. — С. 84-86. doi: https://doi.org/10.21886/2219-8075-2016-1-84-86.
15. Yuan W, Shao Y, Zhao D, Zhang B. Correlation analysis of lipid accumulation index, triglyceride-glucose index and H-type hypertension and coronary artery disease. PeerJ. 2023;11:e16069. doi: https://doi.org/10.7717/peerj.16069
16. Wittert G, Grossmann M. Obesity, type 2 diabetes, and testosterone in ageing men. Rev Endocr Metab Disord. 2022;23(6):1233-1242. doi: 10.1007/s11154-022-09746-5
17. Liu W. Serum leptin, resistin, and adiponectin levels in obese and non-obese patients with newly diagnosed type 2 diabetes mellitus: A population-based study / W. Liu, X. Zhou, Y. Li [et al.] // Medicine (Baltimore). 2020;99(6):e19052
18. George BT, Jhancy M, Dube R, Kar SS, Annamma LM. The Molecular Basis of Male Infertility in Obesity: A Literature Review. Int J Mol Sci. 2023;25(1):179. doi: https://doi.org/10.3390/ijms25010179
19. Nguyen HT, Martin LJ. Transcriptomic analysis of MA-10 tumor Leydig cells treated with adipose derived hormones adiponectin and resistin. Reprod Biol. 2022;22(1):100598. doi: https://doi.org/10.1016/j.repbio.2021.100598
20. Zhao S, Kusminski CM, Scherer PE. Adiponectin, Leptin and Cardiovascular Disorders. Circ Res. 2021;128(1):136-149. doi: https://doi.org/10.1161/CIRCRESAHA.120.314458
Об авторах
И. А. ХрипунРоссия
Хрипун Ирина Алексеевна, д.м.н., доцент, профессор кафедры эндокринологии (с курсом детской эндокринологии)
344022, г. Ростов-на-Дону, пер. Нахичеванский, 29
Scopus ID: 56603164700
Researcher ID: AAF-8950-2019
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Н. А. Кузьменко
Россия
Кузьменко Наталия Александровна, к.м.н., доцент кафедры эндокринологии (с курсом детской эндокринологии)
Ростов-на-Дону
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Н. С. Алексеева
Россия
Алексеева Наталья Сергеевна, к.м.н., доцент кафедры нормальной физиологии
Ростов-на-Дону
Scopus ID: 56677461800
Researcher ID: AEV-9993-2022
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
С. О. Иващенко
Россия
Иващенко Софья Олеговна, студентка
Ростов-на-Дону
Researcher ID: PEV-1601-2025
eLibrary SPIN: 3163-3137
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Н. А. Хрипун
Россия
Хрипун Никита Алексеевич, студент
Ростов-на-Дону
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Дополнительные файлы
|
|
1. Рисунок 1. Результаты анализа состояния липидного обмена. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(223KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Содержание адипогормонов. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(210KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Хрипун И.А., Кузьменко Н.А., Алексеева Н.С., Иващенко С.О., Хрипун Н.А. Особенности функционирования жировой ткани у мужчин на фоне андрогенного дефицита при сахарном диабете 2 типа. Ожирение и метаболизм. 2025;22(4):319-325. https://doi.org/10.14341/omet13223
For citation:
Khripun I.A., Kuzmenko N.A., Alexeeva N.S., Ivaschenko S.O., Khripun N.A. Features of adipose tissue function against the background of androgen deficiency in men with type 2 diabetes mellitus. Obesity and metabolism. 2025;22(4):319-325. (In Russ.) https://doi.org/10.14341/omet13223
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).









































