Перейти к:
Эффективность лираглутида в комплексной терапии больных псориазом в сочетании с метаболическими нарушениями: метаанализ наблюдательных и контролируемых исследований
https://doi.org/10.14341/omet13204
Аннотация
Обоснование. Псориаз характеризуются высокой частотой сопутствующих метаболических нарушений, включая ожирение и сахарный диабет 2 типа (СД2). Имеются ограниченные данные об эффективности агониста рецептора глюкагоноподобного пептида-1 для лечения метаболических нарушений у пациентов с псориазом.
Цель. Анализ эффективности лираглутида в комплексной терапии больных псориазом в сочетании с метаболическими нарушениями.
Материалы и методы. В базе PubMed проведен поиск исследований по ключевым словам: «psoriasis» и «liraglutide». Найдено 23 публикации, в окончательный анализ вошли 5 исследований с общим размером выборки 52 пациента с псориазом в сочетании с метаболическими нарушениями (СД2 и ожирение). Оценивали влияние лираглутида на распространенность и тяжесть псориаза по динамике индекса площади поражения и тяжести псориаза (PASI), качество жизни по опроснику DLQI и уровень глюкозы плазмы крови натощак, гликированного гемоглобина, индекса массы тела (ИМТ). Результаты представлены в виде средневзвешенной разницы (WMD) и 95% доверительного интервала (ДИ).
Результаты. Длительность терапии лираглутидом составила от 8 до 16 нед. Доза лираглутида титровалась от 0,6 мг/сут до 3,0 мг/сут. Показана значимая динамика WMD индексов PASI (-6,95 [95% ДИ -11,59; -2,32]) и DLQI (-6,95 [95% ДИ -11,59; -2,32]), а также ИМТ (-2,97 [95% ДИ -3,58; -2,37]) на фоне терапии лираглутидом. Значимой разницы в уровне глюкозы и гликированного гемоглобина выявлено не было.
Заключение. Результаты метаанализа демонстрируют, что использование лираглутида в комплексной терапии псориаза способствует снижению ИМТ, распространенности и тяжести псориаза, а также улучшению качества жизни больных.
Для цитирования:
Коротаева Т.В., Трошина Е.А., Лила А.М., Паневин Т.С., Насонов Е.Л., Корсакова Ю.Л., Глухова С.И. Эффективность лираглутида в комплексной терапии больных псориазом в сочетании с метаболическими нарушениями: метаанализ наблюдательных и контролируемых исследований. Ожирение и метаболизм. 2025;22(2):70-76. https://doi.org/10.14341/omet13204
For citation:
Korotaeva T.V., Troshina E.A., Lila A.M., Panevin T.S., Nasonov E.L., Korsakova Yu.L., Glukhova S.I. Efficacy of liraglutide in combination therapy of patients with psoriasis combined with metabolic disorders: a meta-analysis of observational and controlled studies. Obesity and metabolism. 2025;22(2):70-76. (In Russ.) https://doi.org/10.14341/omet13204
Обоснование
Псориаз и псориатический артрит характеризуются высокой частотой сопутствующих метаболических нарушений. В частности, риск развития ожирения у пациентов с псориазом увеличен на 50% [1]. Кроме того, тяжелое течение псориаза ассоциировано с более высоким шансом развития ожирения [2]. И наоборот, у пациентов с ожирением риск развития псориаза почти в 2 раза выше в сравнении с больными, имеющими нормальную массу тела. Более того, сам по себе процесс набора веса может увеличивать риск псориаза [3]. Отмечено, что сахарный диабет 2 типа (СД2), важным фактором развития которого является ожирение, также встречается значимо чаще при псориатической болезни в сравнении с пациентами без него, в среднем у 6–20% пациентов [4]. Предрасполагающими факторами, способствующими развитию СД2 при псориатической болезни, могут быть большее число болезненных суставов и показатель СОЭ [5].
Негативное влияние ожирения на течение псориатической болезни может быть обусловлено изменением уровня адипокинов в условиях избытка жировой ткани, в частности снижения уровня адипонектина, ингибирующего выработку ИЛ-6 и ФНО-α, а также «воспалительную» поляризацию макрофагов и Th1- и Th17-опосредованный иммунный ответ [6]. Уровень других цитокинов (химерина, лептина, резистина и висфатина), в отличие от адипонектина оказывающих провоспалительный эффект, при ожирении, наоборот, увеличивается [7].
Ожирение может ухудшать эффективность генно-инженерной биологической терапии [8], а также является фактором, увеличивающим дозу вводимого генно-инженерного препарата [9]. Кроме того, ожирение — фактор риска развития неблагоприятных эффектов базисной противовоспалительной терапии, а в частности, гепатотоксичности метотрексата, что связано с высокой частотой неалкогольной жировой болезни печени при ожирении [10].
Снижение массы тела может приводить к улучшению течения псориатической болезни. Потеря массы тела более чем на 5% от исходной за 6 мес на фоне диеты с ограничением калорийности может сопровождаться более выраженным ответом на применение ингибиторов ФНО-α, а также значимо увеличивает вероятность достижения минимальной активности псориатического артрита [11][12]. Данные исследований влияния бариатрической хирургии у пациентов с морбидным ожирением на течение псориатической болезни также показали положительные результаты [13][14].
Актуальность изучения влияния медикаментозной терапии ожирения в последнее десятилетие возросла, что связано с появлением новой группы препаратов для лечения СД2 и ожирения — агонистов рецепторов глюкагоноподобного пептида 1 (АрГПП-1), которые, с одной стороны, имеют высокую эффективность снижения массы тела, а с другой — могут иметь потенциальные экстрапанкреатические механизмы влияния на воспаление [15]. В настоящий момент основные исследования по влиянию АрГПП-1 на псориатическую болезнь опубликованы по дираглутиду и только в отношении псориаза [16].
ЦЕЛЬ ИССЛЕДОВАНИЯ
Анализ эффективности лираглутида в комплексной терапии больных псориазом в сочетании с метаболическими нарушениями.
МАТЕРИАЛЫ И МЕТОДЫ
В метаанализ были включены исследования оценки эффективности лираглутида у пациентов с псориазом как с наличием, так и с отсутствием сопутствующего СД2. Систематический поиск исследований проводился в базе данных PubMed. В поиске использовались термины «psoriasis» и «liraglutide». Для улучшения чувствительности использовался оператор «AND». Поиск включал работы, опубликованные до 15 августа 2024 г. без нижнего предела даты (рис. 1).
Из каждого исследования были извлечены данные о дизайне исследования, размерах выборки, преобладании пола, среднем возрасте, наличии нарушений углеводного обмена, продолжительности лечения и режиме дозирования лираглутида, индекса площади поражения и тяжести псориаза PASI и дерматологического индекса качества DLQI, показатели индекса массы тела (ИМТ), глюкозы крови натощак и гликированного гемоглобина (HbA1c) до назначения и через некоторое время после терапии лираглутидом (табл. 1). Во всех исследованиях, кроме работы M. Buysschaert и соавт. [18], указано отсутствие какой-либо локальной/системной терапии псориаза на протяжении как минимум 2 мес до включения и на всем протяжении исследования.
Статистическая обработка данных осуществлялась с помощью программы для проведения метаанализов MetaXL 5.3 (Австралия). Результаты представлены в виде средневзвешенной разницы (WMD) и 95% доверительного интервала (ДИ). Гетерогенность между различными публикациями оценивалась при помощи Cochrane’s Q-критерия и критерия I2. При р<0,05 и I2>40% гетерогенность результатов считалась значительной.
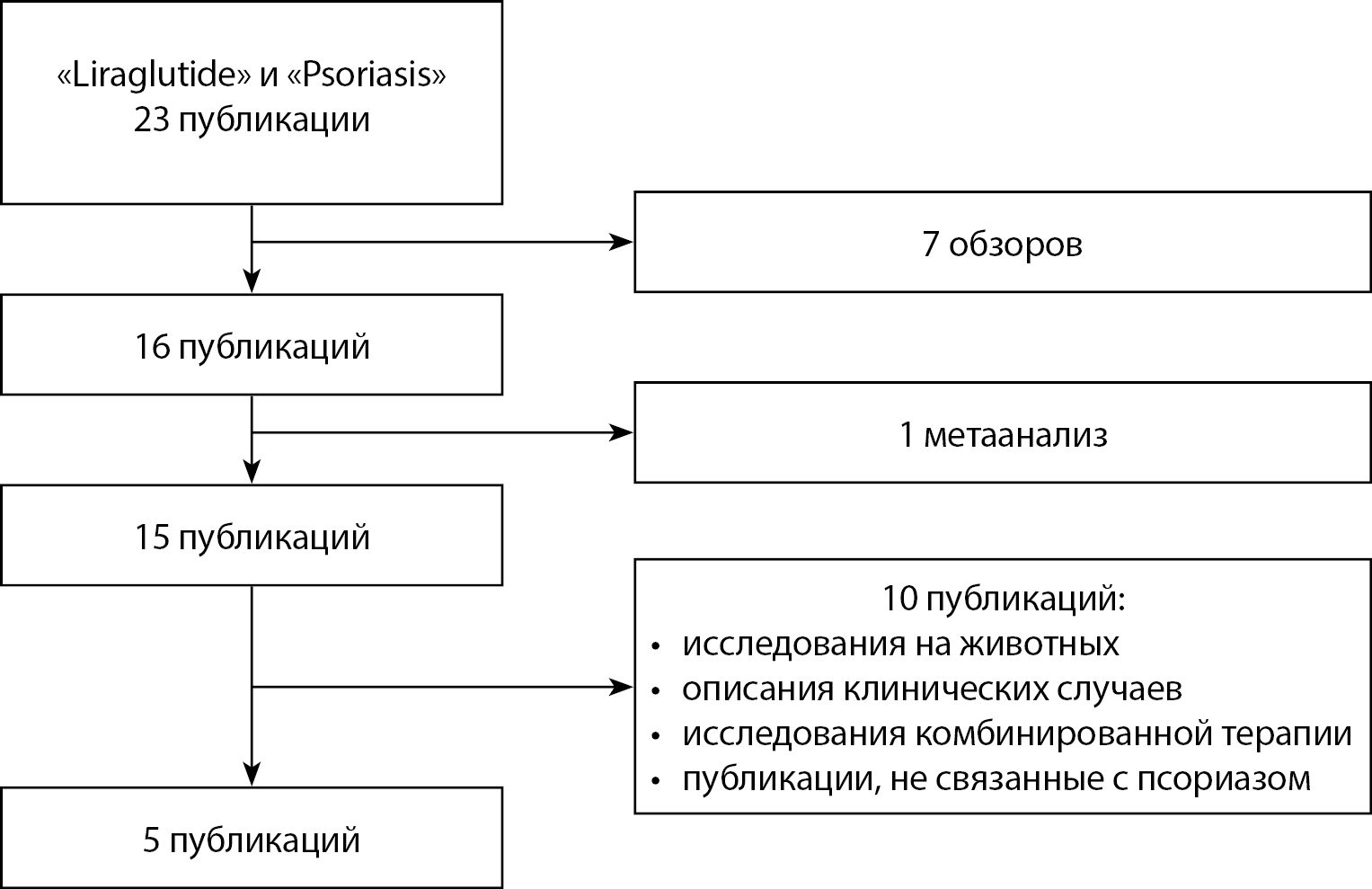
Рисунок 1. Критерии отбора публикаций.
Таблица 1. Характеристика исследований, включенных в метаанализ
|
Исследование |
Ahern T. |
Buysschaert M. и соавт., 2014 [18] |
Faurschou A. и соавт., 2015 [19] |
Xu X. |
Nicolau J. и соавт., 2023 [21] |
|
Тип исследования |
Проспективное когортное |
Проспективное (серия случаев) |
Рандомизированное контролируемое |
Проспективное когортное |
Проспективное когортное |
|
Число пациентов |
7 |
7 |
11 |
7 |
20 |
|
Пол (М/Ж) |
5/2 |
5/2 |
7/4 |
6/1 |
9/11 |
|
Средний возраст (лет) |
45±11 |
56±8 |
54±14 |
60±8 |
45±10 |
|
Сахарный диабет |
+ |
+ |
НТГ |
+ |
- |
|
Продолжительность наблюдения (нед.) |
10 |
16 |
8 |
12 |
12 |
|
Дозирование лираглутида (подкожное введение) |
0,6 мг/сут первые 2 недели, далее — 1,2 мг/сут |
0,6 мг/сут первую неделю, далее — 1,2 мг/сут |
0,6 мг/сут первую неделю, далее — 1,2 мг/сут вторую неделю, далее — 1,8 мг/сут |
0,6 мг/сут первую неделю, далее — 1,2 мг/сут вторую неделю, далее — 1,8 мг/сут |
0,6 мг/сут первую неделю, далее — повышение дозы +0,6 мг каждую неделю до 3,0 мг/сут |
|
PASI (балл) |
Исходно 8,74±9,22 После 4,88±4,25 |
Исходно 12,0±5,9 После 9,2±6,4 |
Исходно 14,5±7,2 После 11,9±4,65 |
Исходно 15,7±11,8 После 2,2±3,0 |
Исходно 10,0±8,4 После 5,1±6,0 |
|
DLQI (балл) |
Исходно 5,7±3,9 После 3,3±3,0 |
- - |
Исходно 8,7±6,1 После 6,2±5,25 |
Исходно 21,8±6,0 После 4,1±3,9 |
Исходно 12,7±7,0 После 6,4±5,6 |
|
ИМТ (кг/м2) |
Исходно 45,67±14,39 После 43,78±5,53 |
Исходно 32,0±10,1 После 30,6±9,1 |
Исходно 37,0±8,2 После 32,3±8,2 |
Исходно 23,0±4,0 После 21,0±3,0 |
Исходно 38,9±5,8 После 36,4±5,6 |
|
Гликированный гемоглобин (%) |
- - |
Исходно 7,5±1,2 После 6,5±0,8 |
Исходно 5,4±0,2 После 5,25±0,19 |
Исходно 8,1±2,3 После 6,4±0,8 |
Исходно 5,5±0,3 После 5,4±0,4 |
|
Глюкоза плазмы натощак (ммоль/л) |
Исходно 6,1±0,74 После 5,8±0,82 |
- - |
Исходно 5,9±0,5 После 5,58±0,43 |
Исходно 6,2±1,6 После 5,5±0,8 |
Исходно 5,14±0,67 После 5,06±0,78 |
Результаты
Индекс площади поражения и тяжести псориаза (PASI)
По результатам проведенного анализа на основе всех 5 исследований на фоне терапии лираглутидом показано значимое снижение средневзвешенной разницы по индексу PASI (-4,85 [ 95% ДИ -7,08; -4,02]) при незначительной гетерогенности (I2=25%, p=0,26) (рис. 2).
Индекс качества жизни в дерматологии (DLQI)
Из включенных 5 исследований динамика DLQI не была описана только в исследовании Buysschaert M. и соавт. [18]. По результатам анализа 4 остальных исследований на фоне терапии лираглутидом показано значимое снижение средневзвешенной разницы по индексу DLQI (-6,95 [ 95% ДИ -11,59; -2,32]) при значительной гетерогенности данных (I2=86%, p=<0,001) (рис. 3).
Глюкоза плазмы натощак
Из включенных 5 исследований динамика уровня глюкозы плазмы натощак также не была описана только в исследовании Buysschaert M. и соавт. [18]. По результатам анализа 4 остальных исследований на фоне терапии лираглутидом не отмечено значимого снижения средневзвешенной разницы глюкозы плазмы натощак (-0,26 [ 95% ДИ -0,54; 0,03]) при незначительной гетерогенности данных (I2=32%, p=0,21) (рис. 4).
Гликированный гемоглобин (HbA1c)
По результатам проведенного анализа на основе всех 5 исследований на фоне терапии лираглутидом не отмечено значимого снижения средневзвешенной разницы уровня гликированного гемоглобина (-0,20 [ 95% ДИ -0,41; 0,02]) при незначительной гетерогенности (I2=32%, p=0,21) (рис. 5).
Индекс массы тела (ИМТ)
По результатам проведенного анализа на основе всех 5 исследований на фоне терапии лираглутидом показано значимое снижение средневзвешенной разницы по индексу массы тела (-2,97 [ 95% ДИ -3,58; -2,37]) при незначительной гетерогенности (I2=0%, p=0,94) (рис. 6).
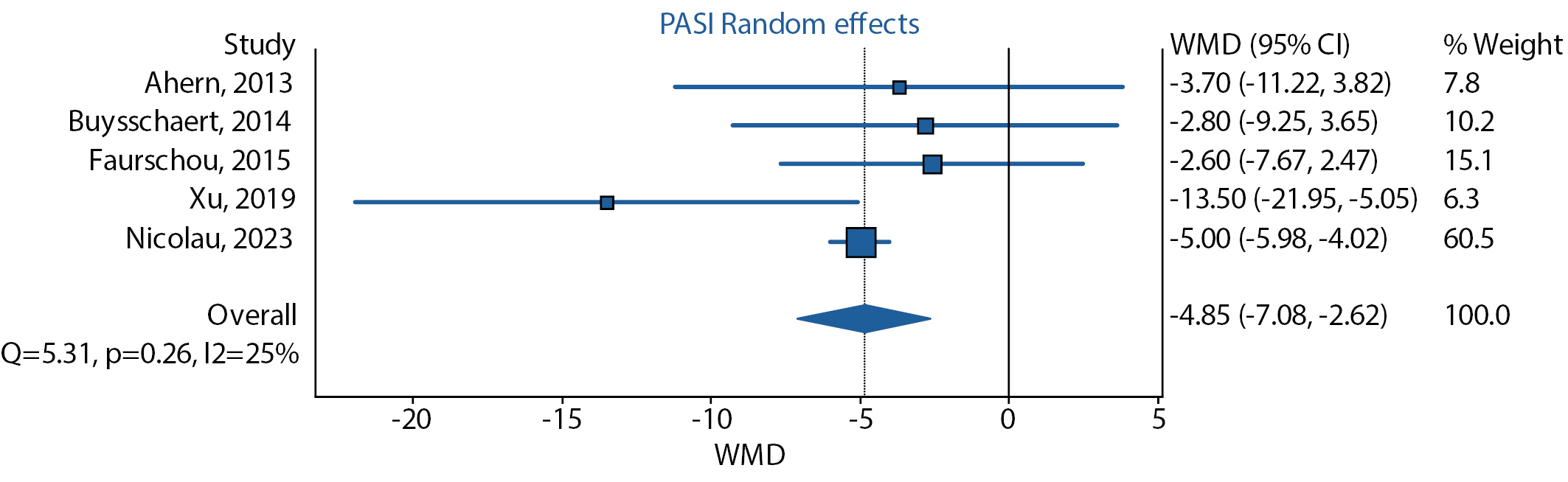
Рисунок 2. Динамика индекса PASI на фоне терапии лираглутидом.
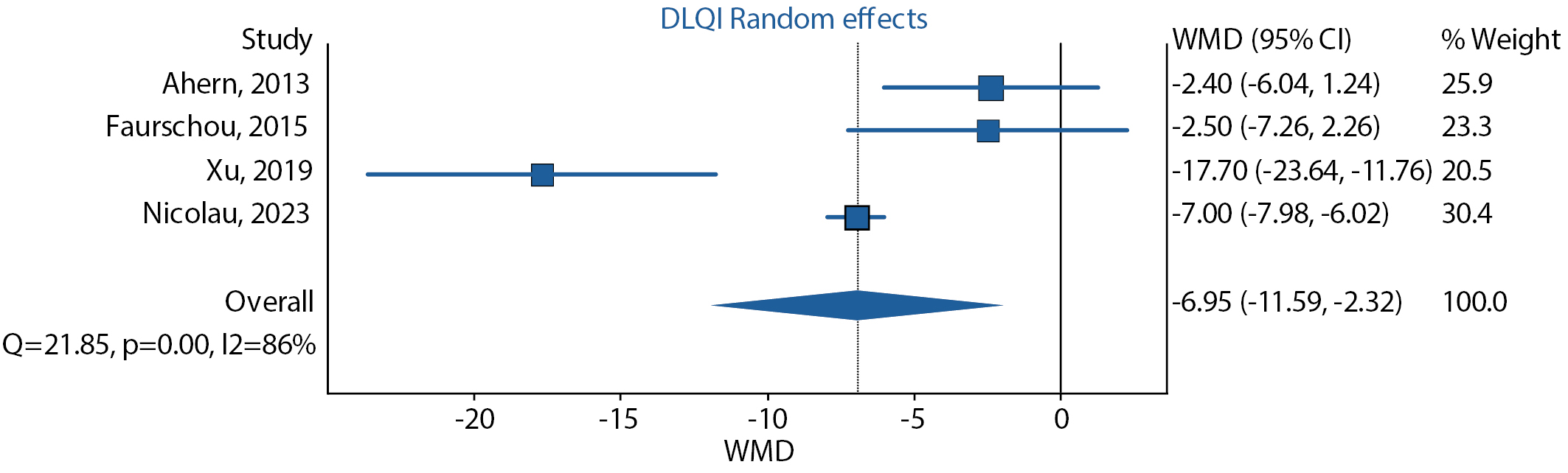
Рисунок 3. Динамика индекса DLQI на фоне терапии лираглутидом.
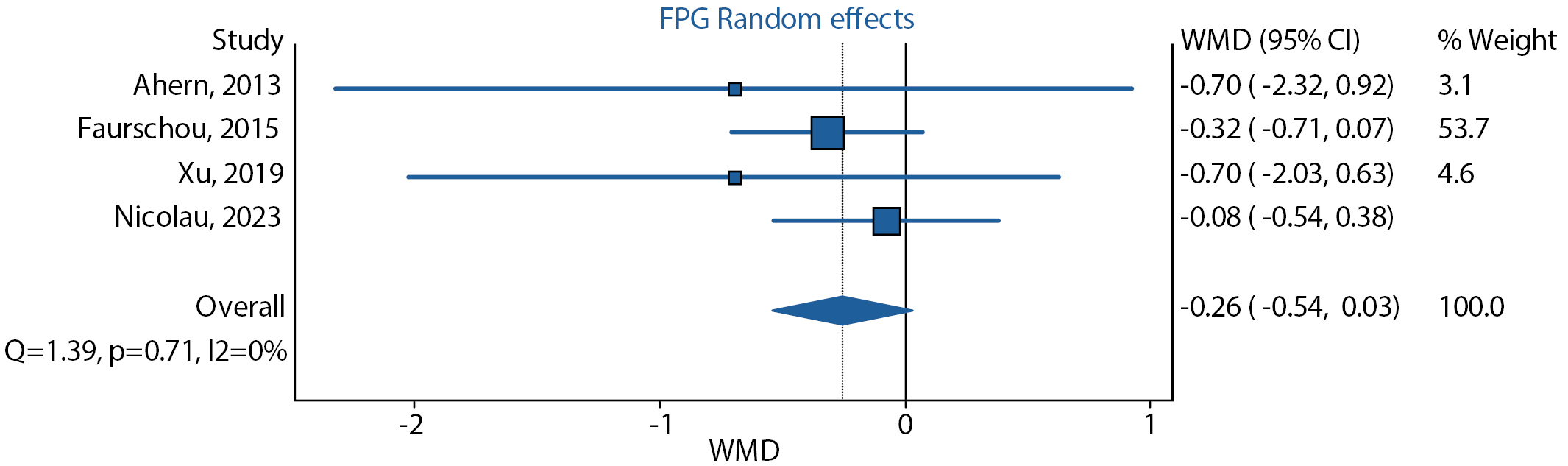
Рисунок 4. Динамика уровня глюкозы плазмы натощак на фоне терапии лираглутидом.
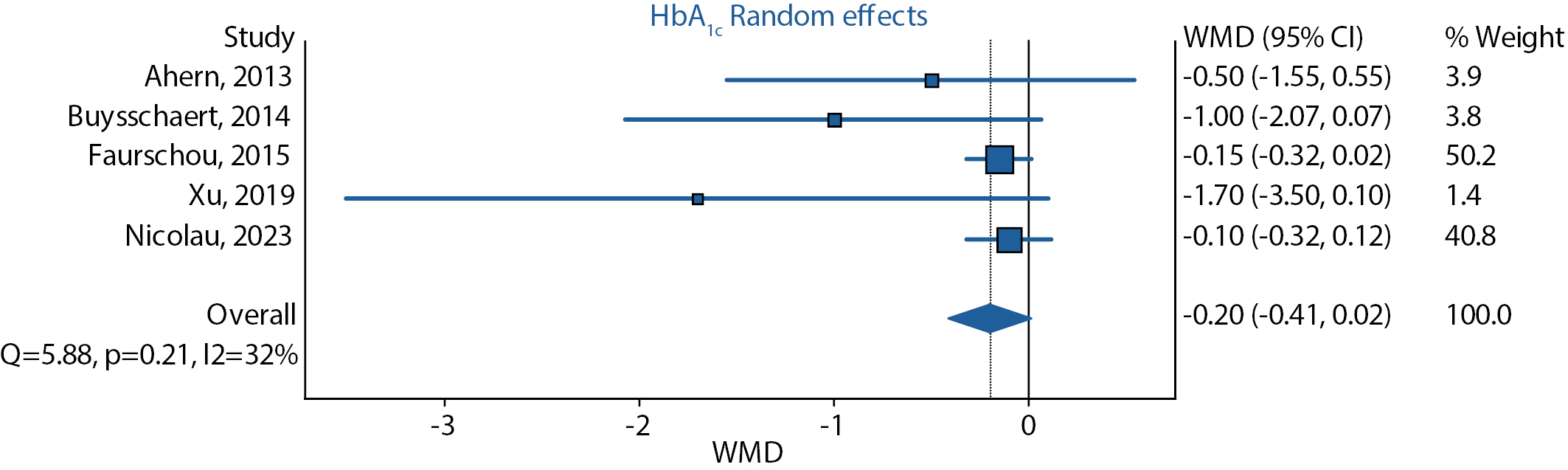
Рисунок 5. Динамика уровня гликированного гемоглобина на фоне терапии лираглутидом.
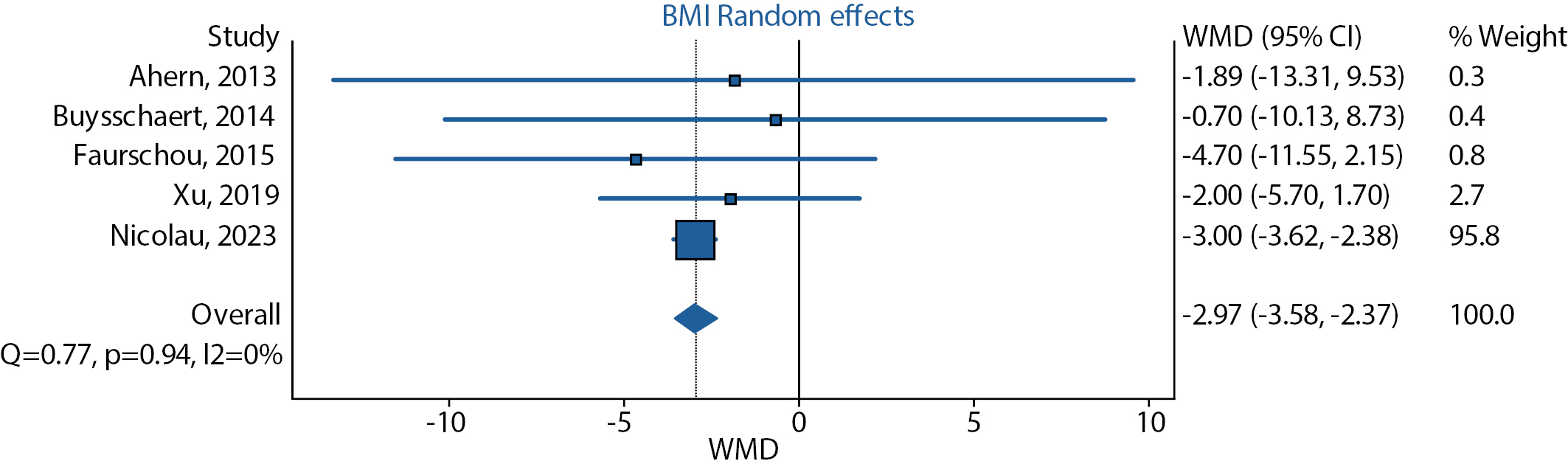
Рисунок 6. Динамика индекса массы тела на фоне терапии лираглутидом.
Обсуждение
Глюкагоноподобный пептид-1 (ГПП-1) относится к гормонам желудочно-кишечного тракта инкретинам, состоит из 30–31 аминокислот и продуцируется L-клетками кишечника в ответ на пищевые и воспалительные стимулы. Кроме того, ГПП-1 вырабатывается в нейронах ядра одиночного тракта ствола мозга. Рецепторы к ГПП-1 экспрессируются в β-клетках островков поджелудочной железы, эпителиальных клетках легких, кардиомиоцитах предсердий, афферентных нейронах блуждающего нерва, нейронах ряда областей головного мозга, а также клетках, составляющих слизистые оболочки желудка и тонкого кишечника. Эффекты ГПП-1 при взаимодействии с мембранным рецептором реализуются через систему G-белка с увеличением образования цАМФ, а также высвобождением кальция, что приводит к активации путей передачи сигналов PKA, Epac-2, фосфолипазы C и ERK1/2 [22]. Гипогликемическая активность ГПП-1 связана со стимуляцией глюкозозависимой секреции инсулина, ингибированием продукции глюкагона и регуляцией пролиферации, дифференцировки и выживания островковых клеток поджелудочной железы [23].
Потенциальные экстрапанкреатические механизмы влияния АрГПП-1 на воспаление, как предполагается, могут быть связаны, с активацией AMPK, NF-kB, влиянием на T-клеточное звено, в частности инвариантных натуральных Т-киллеров, а также влиянием на продукцию ИЛ-17 [15].
В одном из включенных в метаанализ исследований (Buysschaert M. и соавт.) при применении лираглутида отмечено также снижение числа Т-клеток в коже и экспрессии ИЛ-17 в псориатических бляшках [18]. В исследовании Ahern T. и соавт., где помимо включенных в метаанализ показателей, оценивались иммуннологические показатели, отмечено увеличение доли циркулирующих инвариантных натуральных Т-киллеров среди всей популяции Т-лифомцитов с 0,13 до 0,4% (p=0,03) [17]. Интересно также, что экспрессия рецептора к ГПП-1 была выявлена в клетках псориатических бляшек у человека, но не в культуре здоровых кератиноцитов [24].
Ранее в 2022 г. уже проводился метаанализ 4 исследований, суммарно включавших 32 пациента, получавших лираглутид (от 8 до 16 недель), страдавших СД2 или нарушением толерантности к глюкозе. Было показано значимое снижение индекса PASI (-4,3, 95% ДИ от -7,6 до -1,05, p=0,01) и глюкозы натощак (-0,34, 95% ДИ от -0,68 до -0,01, p=0,048) после проведения лечения, однако не было получено значимых различий по ИМТ, индексу DLQI и уровню гликированного гемоглобина [16]. В наш метаанализ добавлено исследование Nicolau J. и соавт., опубликованное в 2023 г. [21]. Особенностью данного исследования является наибольшая выборка пациентов (n=20) в сравнении с другими работами, отсутствие нарушений углеводного обмена у них, а также более высокая максимальная доза применяемого лираглутида (до 3,0 мг/сут). Учитывая высокий вклад исследования Nicolau J. и соавт. [21] в результаты проведенного нами метаанализа, были получены отличные от предыдущего метаанализа результаты. Так, помимо значимого изменения индекса PASI, получена значимая разница по индексу DLQI и ИМТ, в то время как для показателей углеводного обмена значимой разницы не отмечалось, что может быть объяснено высокой долей лиц без нарушений углеводного обмена из исследования Nicolau J. и соавт. [21]. Различия в результатах двух метаанализов могут быть обусловлены изменением размеров выборки с включением значительной доли пациентов без нарушений углеводного обмена, что обуславливает отсутствие серьезных колебаний уровня глюкозы натощак и гликированного гемоглобина. С другой стороны, пациенты из исследования Nicolau J. и соавт. характеризовались высоким исходным ИМТ, а также значимой динамикой его снижения, что и внесло вклад в появление значимой динамики по данному показателю в нашем метаанализе.
Исследования влияния других АрГПП-1 при псориазе к настоящему времени представлены лишь единичными описаниями клинических случаев, где отмечался положительный эффект [25][26].
Ограничением настоящего исследования, как и ранее проведенного метаанализа, по-прежнему остается небольшое количество исследований, общее число пациентов и длительность наблюдения. Однако результаты настоящего метаанализа учитывают и пациентов без СД2, а также применение лираглутида и в максимально зарегистрированной суточной дозе 3,0 мг.
Заключение
Представленные данные позволяют говорить о возможности наличии влияния АрГПП-1 на активность псориаза. Необходимы дальнейшие контролируемые исследования с большим объемом выборок, а также отдельные исследования влияния данной группы препаратов для пациентов с псориатическим артритом.
Дополнительная информация
Источники финансирования. Работа выполнена в рамках фундаментальной научной тематики ФГБНУ НИИР им. В.А. Насоновой №125020501435-8 «Эволюция аксиальных спондилоартритов на основе комплексного динамического изучения молекулярно-биологических, молекулярно-генетических, клинико-визуализационных факторов прогрессирования заболевания, качества жизни, коморбидности и таргетной инновационной терапии».
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Коротаева Т.В. — концепция исследования, интерпретация результатов, внесение существенной правки; Трошина Е.А. — концепция исследования, внесение в рукопись существенной правки; Лила А.М. — концепция исследования, внесение в рукопись существенной правки; Паневин Т.С. — концепция и дизайн исследования, написание статьи; Насонов Е.Л. — концепция исследования, внесение в рукопись существенной правки; Корсакова Ю.Л. — дизайн исследования, внесение в рукопись существенной правки; Глухова С.И. — дизайн исследования, получение, анализ данных, написание статьи. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Armstrong AW, Harskamp CT, Armstrong EJ. The association between psoriasis and obesity: a systematic review and meta-analysis of observational studies. Nutr Diabetes. 2012;2(12):e54. doi: https://doi.org/10.1038/nutd.2012.26
2. Neimann AL, Shin DB, Wang X, Margolis DJ, Troxel AB, Gelfand JM. Prevalence of cardiovascular risk factors in patients with psoriasis. J Am Acad Dermatol. 2006;55(5):829-835. doi: https://doi.org/10.1016/j.jaad.2006.08.040
3. Snekvik I, Smith CH, Nilsen TIL, et al. Obesity, Waist Circumference, Weight Change, and Risk of Incident Psoriasis: Prospective Data from the HUNT Study. J Invest Dermatol. 2017;137(12):2484-2490. doi: https://doi.org/10.1016/j.jid.2017.07.822
4. Dal Bello G, Gisondi P, Idolazzi L, Girolomoni G. Psoriatic Arthritis and Diabetes Mellitus: A Narrative Review. Rheumatol Ther. 2020;7(2):271-285. doi: https://doi.org/10.1007/s40744-020-00206-7
5. Eder L, Chandran V, Cook R, Gladman DD. The Risk of Developing Diabetes Mellitus in Patients with Psoriatic Arthritis: A Cohort Study. J Rheumatol. 2017;44(3):286-291. doi: https://doi.org/10.3899/jrheum.160861
6. Takahashi H, Honma M, Ishida-Yamamoto A, Iizuka H. Adiponectin and leptin modulate cell proliferation and cytokine secretion of normal human keratinocytes and T lymphocytes. J Dermatol Sci. 2010;59(2):143-145. doi: https://doi.org/10.1016/j.jdermsci.2010.06.004
7. Xue K, Liu H, Jian Q, et al. Leptin induces secretion of pro-inflammatory cytokines by human keratinocytes in vitro--a possible reason for increased severity of psoriasis in patients with a high body mass index. Exp Dermatol. 2013;22(6):406-410. doi: https://doi.org/10.1111/exd.12162
8. Dalamaga M, Papadavid E. Can we better strategize our choice of pharmacotherapy for patients with comorbid psoriasis and obesity?. Expert Opin Pharmacother. 2019;20(11):1303-1308. doi: https://doi.org/10.1080/14656566.2019.1603294
9. Gisondi P, Conti A, Galdo G, Piaserico S, De Simone C, Girolomoni G. Ustekinumab does not increase body mass index in patients with chronic plaque psoriasis: a prospective cohort study. Br J Dermatol. 2013;168(5):1124-1127. doi: https://doi.org/10.1111/bjd.12235
10. Chiricozzi A, Gisondi P, Girolomoni G. The pharmacological management of patients with comorbid psoriasis and obesity. Expert Opin Pharmacother. 2019;20(7):863-872. doi: https://doi.org/10.1080/14656566.2019.1583207
11. Di Minno MN, Peluso R, Iervolino S, et al. Weight loss and achievement of minimal disease activity in patients with psoriatic arthritis starting treatment with tumour necrosis factor α blockers. Ann Rheum Dis. 2014;73(6):1157-1162. doi: https://doi.org/10.1136/annrheumdis-2012-202812
12. Klingberg E, Björkman S, Eliasson B, Larsson I, Bilberg A. Weight loss is associated with sustained improvement of disease activity and cardiovascular risk factors in patients with psoriatic arthritis and obesity: a prospective intervention study with two years of follow-up. Arthritis Res Ther. 2020;22(1):254. doi: https://doi.org/10.1186/s13075-020-02350-5
13. Maglio C, Peltonen M, Rudin A, Carlsson LMS. Bariatric surgery and the incidence of psoriasis and psoriatic arthritis in the Swedish obese subjects study. Obesity (Silver Spring). 2017;25(12):2068-2073. doi: https://doi.org/10.1002/oby.21955
14. Egeberg A, Sørensen JA, Gislason GH, et al. Incidence and prognosis of psoriasis and psoriatic arthritis in patients undergoing bariatric surgery [published correction appears in JAMA Surg. 2018;153(7):692]. JAMA Surg. 2017;152(4):344-349. doi: https://doi.org/10.1001/jamasurg.2016.4610
15. Насонов Е.Л., Паневин Т.С., Трошина Е.А. Агонисты рецепторов глюкагоноподобного пептида-1: перспективы применения в ревматологии. // Научно-практическая ревматология. — 2024. — Т.62. — №2. — С.135–144 doi: https://doi.org/10.47360/1995-4484-2024-135-144
16. Chang G, Chen B, Zhang L. Efficacy of GLP-1rA, liraglutide, in plaque psoriasis treatment with type 2 diabetes: a systematic review and meta-analysis of prospective cohort and before-after studies. J Dermatolog Treat. 2022;33(3):1299-1305. doi: https://doi.org/10.1080/09546634.2021.1882658
17. Ahern T, Tobin AM, Corrigan M, et al. Glucagon-like peptide-1 analogue therapy for psoriasis patients with obesity and type 2 diabetes: a prospective cohort study. J Eur Acad Dermatol Venereol. 2013;27(11):1440-1443. doi: https://doi.org/10.1111/j.1468-3083.2012.04609.x
18. Buysschaert M, Baeck M, Preumont V, et al. Improvement of psoriasis during glucagon-like peptide-1 analogue therapy in type 2 diabetes is associated with decreasing dermal γδ T-cell number: a prospective case-series study. Br J Dermatol. 2014;171(1):155-161. doi: https://doi.org/10.1111/bjd.12886
19. Faurschou A, Gyldenløve M, Rohde U, et al. Lack of effect of the glucagon-like peptide-1 receptor agonist liraglutide on psoriasis in glucose-tolerant patients--a randomized placebo-controlled trial. J Eur Acad Dermatol Venereol. 2015;29(3):555-559. doi: https://doi.org/10.1111/jdv.12629
20. Xu X, Lin L, Chen P, et al. Treatment with liraglutide, a glucagon-like peptide-1 analogue, improves effectively the skin lesions of psoriasis patients with type 2 diabetes: A prospective cohort study. Diabetes Res Clin Pract. 2019;150:167-173. doi: https://doi.org/10.1016/j.diabres.2019.03.002
21. Nicolau J, Nadal A, Sanchís P, Pujol A, Nadal C, Masmiquel L. Effects of liraglutide among patients living with psoriasis and obesity. Med Clin (Barc). 2023;161(7):293-296. doi: https://doi.org/10.1016/j.medcli.2023.05.021
22. Mehdi SF, Pusapati S, Anwar MS, et al. Glucagon-like peptide-1: a multi-faceted anti-inflammatory agent. Front Immunol. 2023;14:1148209. doi: https://doi.org/10.3389/fimmu.2023.1148209
23. Kim W, Egan JM. The role of incretins in glucose homeostasis and diabetes treatment. Pharmacol Rev. 2008;60(4):470-512. doi: https://doi.org/10.1124/pr.108.000604
24. Faurschou A, Pedersen J, Gyldenløve M, et al. Increased expression of glucagon-like peptide-1 receptors in psoriasis plaques. Exp Dermatol. 2013;22(2):150-152. doi: https://doi.org/10.1111/exd.12081
25. Costanzo G, Curatolo S, Busà B, Belfiore A, Gullo D. Two birds one stone: semaglutide is highly effective against severe psoriasis in a type 2 diabetic patient. Endocrinol Diabetes Metab Case. doi: https://doi.org/10.1530/EDM-21-0007
26. Malavazos AE, Meregalli C, Sorrentino F, et al. Semaglutide therapy decreases epicardial fat inflammation and improves psoriasis severity in patients affected by abdominal obesity and type-2 diabetes. Endocrinol Diabetes Metab Case Rep. 2023;2023(3):23-0017. doi: https://doi.org/10.1530/EDM-23-0017
Об авторах
Т. В. КоротаеваРоссия
Коротаева Татьяна Викторовна - д.м.н.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Е. А. Трошина
Россия
Трошина Екатерина Анатольевна - д.м.н., чл.-корр. РАН.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
А. М. Лила
Россия
Лила Александр Михайлович - д.м.н., член-корр. РАН
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Т. С. Паневин
Россия
Паневин Тарас Сергеевич - к.м.н.
115522, Москва, Каширское шоссе, 34А
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Е. Л. Насонов
Россия
Насонов Евгений Львович - д.м.н., акад. РАН.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Ю. Л. Корсакова
Россия
Юлия Леонидовна Корсакова - к.м.н.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
С. И. Глухова
Россия
Глухова Светлана Ивановна - к.ф-м.н.
Москва
Конфликт интересов:
Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи
Дополнительные файлы
|
|
1. Рисунок 1. Критерии отбора публикаций. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(258KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Динамика индекса PASI на фоне терапии лираглутидом. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(279KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Динамика индекса DLQI на фоне терапии лираглутидом. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(245KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Динамика уровня глюкозы плазмы натощак на фоне терапии лираглутидом. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(254KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Динамика уровня гликированного гемоглобина на фоне терапии лираглутидом. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(256KB)
|
Метаданные ▾ | |
|
|
6. Рисунок 6. Динамика индекса массы тела на фоне терапии лираглутидом. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(264KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Коротаева Т.В., Трошина Е.А., Лила А.М., Паневин Т.С., Насонов Е.Л., Корсакова Ю.Л., Глухова С.И. Эффективность лираглутида в комплексной терапии больных псориазом в сочетании с метаболическими нарушениями: метаанализ наблюдательных и контролируемых исследований. Ожирение и метаболизм. 2025;22(2):70-76. https://doi.org/10.14341/omet13204
For citation:
Korotaeva T.V., Troshina E.A., Lila A.M., Panevin T.S., Nasonov E.L., Korsakova Yu.L., Glukhova S.I. Efficacy of liraglutide in combination therapy of patients with psoriasis combined with metabolic disorders: a meta-analysis of observational and controlled studies. Obesity and metabolism. 2025;22(2):70-76. (In Russ.) https://doi.org/10.14341/omet13204

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).










































