Перейти к:
Лимфатическая система и жировая ткань: коммуникации в норме и патологии
https://doi.org/10.14341/omet12776
Аннотация
Лимфатическая система (ЛС) — одна из основных интегративных систем организма, обеспечивающая защитную и транспортную функции. В последние годы особый интерес вызывают взаимодействия между ЛС и жировой тканью (ЖТ). Лимфатические сосуды играют важную роль в обеспечении метаболической и регуляторной функции ЖТ, являясь коллектором продуктов липолиза и адипокинов. В свою очередь, гормоны и адипоцитокины, продуцируемые в адипоцитах (в их числе лептин, адипонектин, IL-6, TNF-α и др.), влияют на функцию лимфатических эндотелиальных клеток и контролируют рост лимфатических сосудов. Кооперации между ЛС и ЖТ становятся патогенетически и клинически важными при лимфедеме и ожирении. Известно, что как первичная, так и вторичная лимфедемы характеризуются усиленной аккумуляцией жира, которая ассоциирована с выраженностью лимфостаза и воспаления. Сходным образом при ожирении нарушается дренажная функция ЛС, что сопровождается перилимфатической мононуклеарной инфильтрацией ЖТ. Развитию этих изменений способствуют эндокринная дисфункция адипоцитов и нарушение продукции адипоцитокинов. Увеличение продукции воспалительных медиаторов и нарушение трафика воспалительных клеток вызывают дальнейшее ухудшение оттока интерстициальной жидкости и усугубляют воспаление ЖТ, формируя тем самым порочный круг. Роль лимфангиогенеза в ремоделировании ЖТ при ожирении нуждается в дальнейших исследованиях. Другим перспективным направлением исследований является изучение роли интестинальной ЛС в развитии ожирения и связанных с ним расстройств. Показано, что транспорт хиломикронов из кишечника зависит от экспрессии целого ряда молекулярных медиаторов в эндотелиоцитах интестинальных лимфатических сосудов (VEGF-C, DLL-4, нейропилин-1, VEGFR-1, CD36/FAT), а также функционирования «кнопочных» и «молниеобразных» контактов между эндотелиоцитами. Экспериментально обоснован новый подход к лечению ожирения, основанный на блокаде лимфатического транспорта хиломикронов. Дальнейшая идентификация молекулярных механизмов и сигнальных путей, определяющих ремоделирование ЖТ при лимфедеме и ожирении, вероятно, позволит найти новые подходы к лечению этих заболеваний.
Для цитирования:
Климонтов В.В., Булумбаева Д.М. Лимфатическая система и жировая ткань: коммуникации в норме и патологии. Ожирение и метаболизм. 2021;18(3):336-344. https://doi.org/10.14341/omet12776
For citation:
Klimontov V.V., Bulumbaeva D.M. Lymphatic system and adipose tissue: Crosstalk in health and disease. Obesity and metabolism. 2021;18(3):336-344. (In Russ.) https://doi.org/10.14341/omet12776
ВВЕДЕНИЕ
Лимфатическая система (ЛС) — одна из основных интегративных систем организма, обеспечивающая защитную и транспортную функции. Первая из них реализуется органами и клетками ЛС, вторая — ее сосудистым компонентом. Будучи тесно связанной с иммунной, кровеносной системой и системой соединительной ткани, ЛС принимает участие в многочисленных межклеточных кооперациях, клеточно-матриксных взаимодействиях, иммунном ответе, репарации, обмене липидов и других физиологических процессах, играя важнейшую роль в обеспечении постоянства внутренней среды [1]. В последние годы особый интерес вызывают взаимодействия между ЛС и жировой тканью (ЖТ). Обсуждается роль этих взаимодействий в развитии ожирения, иммуновоспалительных заболеваний, а также патологии самой ЛС [2–4].
В данном обзоре мы обобщили сведения об участии ЛС в обеспечении метаболической и регуляторной функции ЖТ, а также данные о роли взаимодействий между ЛС и ЖТ в патогенезе лимфедемы и ожирения. Автоматический поиск литературных источников проведен по комбинациям ключевых слов “lymphatic”, “adipose tissue”, “lymphedema”, “obesity”, “lymphangiogenesis” и их русскоязычных эквивалентов в реферативных базах данных PubMed/Medline, Scopus, eLibrary. Дополнительный анализ проводился в ручном режиме по спискам цитируемой литературы в релевантных статьях.
МОРФОФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА ЛИМФАТИЧЕСКОЙ СЕТИ ЖИРОВОЙ ТКАНИ
По современным представлениям, ЖТ — орган с высочайшим уровнем метаболических процессов и эндокринной функцией, который синтезирует не менее 50 регуляторных молекул (гормонов, адипокинов), участвующих в регуляции самых различных функций организма [5]. ЖТ характеризуется высокой пластичностью, способностью к ремоделированию при избытке или недостатке питательных веществ. Указанные свойства ЖТ реализуются в тесном взаимодействии с сетью кровеносных и лимфатических сосудов.
Лимфатические сосуды в ЖТ, как правило, располагаются в прослойках междольковой рыхлой волокнистой соединительной ткани, по ходу кровеносных сосудов (рис. 1). Корнями ЛС являются слепо начинающиеся лимфатические капилляры. Эти высокопроницаемые сосуды состоят из одного слоя эндотелиальных клеток, не имеют базальной мембраны и характеризуются прерывистыми, «пуговичными» межклеточными соединениями. Градиенты гидростатического давления, действующие через лимфатическую стенку, облегчают открытие или закрытие этих соединений, функционирующих как первичная клапанная система [6]. Во время лимфообразования интерстициальная жидкость, содержащая воду, растворенные вещества и иммунные клетки, первоначально транспортируется в просвет лимфатических капилляров. Лимфа, образующаяся в капиллярах, затем пассивно транспортируется в собирательные сосуды, которые разделяются внутрипросветными двустворчатыми клапанами. Эти области собирательных сосудов дополнительно покрыты базальной мембраной и лимфатическими мышечными клетками. В отличие от лимфатических капилляров, эндотелиоциты в собирательных сосудах образуют непрерывные «молниеобразные» межклеточные соединения, предотвращающие утечку лимфы во время транспортировки. Регулирование открытия и закрытия внутрипросветных клапанов поддерживает однонаправленный транспорт лимфы и предотвращает обратный отток [1].
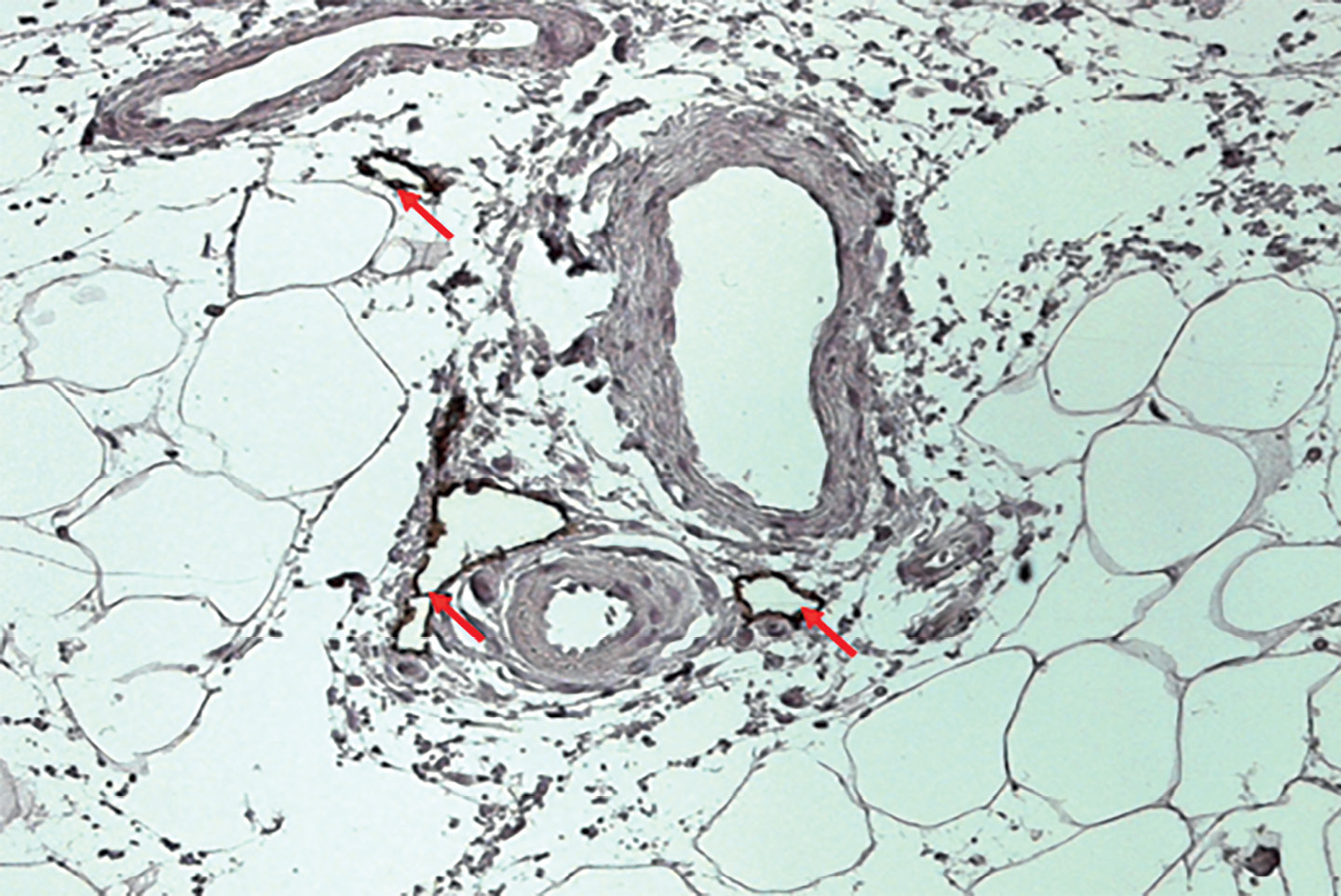
Рисунок 1. Визуализация лимфатических сосудов в подкожной жировой ткани у человека.
Стрелками показаны лимфатические сосуды в междольковой рыхлой волокнистой соединительной ткани. Иммуногистохимическое окрашивание на подопланин. Ув. х100.
Об особенностях корней ЛС в подкожной и висцеральной ЖТ известно немного. В недавнем исследовании Redondo P. et al., использовав для иммуногистохимического типирования молекулярные маркеры лимфатических эндотелиоцитов: VEGFR-3 (Vascular endothelial growth factor receptor-3), Prox-1 (Prospero-related homeobox protein-1), LYVE-1 (Lymphatic vessel endothelial hyaluronan receptor-1) и подопланин, конфокальную микроскопию и трехмерную визуализацию, показали наличие лимфатических сосудов малого и среднего калибра вокруг и внутри долек висцеральной ЖТ человека. В подкожной ЖТ лимфатические сосуды встречались реже и обнаруживались в подкожных сосудистых сплетениях (на границе с дермой) и в фиброзных перегородках между дольками ЖТ. При морфометрическом анализе оказалось, что плотность сети лимфатических сосудов в подкожной ЖТ в 5 раз меньше по сравнению с висцеральной. Лимфатические капилляры были типированы в висцеральной ЖТ, где они располагались внутри паренхимы, прилегая к отдельным адипоцитам. В подкожной ЖТ лимфатические капилляры выявить не удалось [7]. Эти данные согласуются с результатами более раннего изотопного исследования с коллоидным технецием, показавшими слабый лимфатический дренаж в подкожной ЖТ [8].
Происхождение лимфатических сосудов на протяжении длительного времени оставалось предметом дискуссий. В 1902 г. F.R. Sabin предложила модель развития лимфатических сосудов из эмбриональных вен. Немногим позже, в 1908 г. G.S. Huntington и С.F. McClure была выдвинута альтернативная гипотеза локального образования лимфатических сосудов в мезенхиме [1]. На протяжении столетия эти две теории являлись конкурирующими. Данные, накопленные в последние годы, подтверждают возможность образования лимфатических сосудов как из эмбриональных вен, так и из локальных лимфангиобластов. Образование новых лимфатических сосудов может наблюдаться и в постнатальном периоде, в частности, при воспалении и опухолевом росте. Как и в эмбриональный период, новообразование лимфатических сосудов при этом может осуществляться как из уже существующих сосудов (лимфангиогенез), так и de novo из ангиобластов (лимфоваскулогенез) [9]. В последние годы заметно расширились представления о молекулярно-генетических аспектах формирования лимфатических сосудов. Установлено, что в их развитии важную роль играют факторы роста сосудистого эндотелия VEGF-C и VEGF-D, их рецепторы (VEGFR-3), транскрипционные факторы (Prox-1, FOXC2, Sox 18, Nr2f2 и др.), внутриклеточные сигнальные пути (BMP/Smad, Wnt, Notch, AKT/ERK), микро РНК [9–11]. Основные регуляторы лимфангиогенеза представлены в табл. 1. Особенности эмбрионального и постнатального развития лимфатических сосудов висцеральной и подкожной ЖТ, а также механизмы, контролирующие этот процесс, не изучены.
Таблица 1. Активаторы и ингибиторы лимфангиогенеза [1, 11–13]
Активаторы | Ингибиторы |
•Факторы роста эндотелия сосудов С и D (VEGF-С, VEGF-D) •Адипонектин •Ангиопоэтин-1, ангиопоэтин-2 •Фактор некроза опухоли-α (TNF-α) •Эпидермальный фактор роста (EGF) •Фактор роста фибробластов (FGF2) •Фактор роста гепатоцитов (HGF) •Инсулиноподобный фактор-1 (IGF-1) •Тромбоцитарный фактор роста-BB (PDGF-BB) •Тромбоцитарный фактор роста •(TGF-α) •Интерлейкины: IL-1, IL-12, IL-18 •Коллаген I типа (у мышей) •Фибронектин (in vitro) | •Лептин •Матриксные металлопротеиназы: MMP-1, MMP-2, MMP-9 •Интерлейкины: IL-4, IL-5, IL-10, IL-13 |
Вместе с тем накапливаются данные о вовлечении ЛС в обеспечение метаболической и регуляторной функции ЖT. Как известно, ЛС играют важную роль в транспорте пищевых липидов из тонкой кишки в кровоток. Абсорбированные липиды, преимущественно в виде хиломикронов, поступают в специализированные интестинальные лимфатические капилляры («млечные сосуды») через открытые «пуговичные» контакты между эндотелиоцитами [14]. С током лимфы хиломикроны достигают подключичной вены и далее транспортируются в печень, где подвергаются метаболизму. Образующиеся при этом жирные кислоты поступают в ЖТ. От самой ЖТ через лимфу переносятся продукты липолиза. Показано, что лимфа, оттекающая от ЖТ, содержит в 2 раза меньше неэстерифицированных жирных кислот и в 20 раз меньше триглицеридов по сравнению с плазмой венозной крови. При этом концентрация глицерина выше в лимфе, что, очевидно, связано с процессами липолиза в адипоцитах [15].
Показано, что проницаемость собирательных лимфатических сосудов обеспечивает контакт антигенов, транспортирующихся лимфой, с макрофагами и дендритными клетками в окружающей лимфатические сосуды ЖТ. Эндоцитоз антигенов данными клетками важен для формирования Т-клеточного иммунного ответа ЖТ, а также для миграции антиген-презентирующих дендритных клеток в близлежащие лимфатические узлы. Таким образом, собирательные лимфатические сосуды координируют воспалительные и иммунные реакции в жировых депо [16].
Установлено, что многие адипокины переносятся из интерстициальной жидкости в кровоток через ЛС. Miller N.E. сравнил концентрации гормонов ЖТ и адипоцитокинов в плазме венозной крови и афферентной (пренодальной) лимфе, оттекающей от подкожной ЖТ, у 12 здоровых мужчин. Концентрации лептина и фактора некроза опухолей-α (TNF-α) в лимфе превышали соответствующие показатели в плазме крови в 5 раз, концентрация моноцитарного хемоаттрактантного протеина-1 (МСР-1) — в 4 раза, интерлейкина-1β (IL-1β) — в 3 раза, интерлейкина-6 (IL-6) — в 25 раз (все P≤0,003). Уровень адипонектина, напротив, оказался достоверно более высоким в крови [15]. Известно, что проницаемость кровеносных капилляров для макромолекул отличается большей селективностью по сравнению с проницаемостью терминальных лимфатических сосудов. При условии отсутствия специфических механизмов переноса, размер молекул, по-видимому, является основным фактором, определяющим транспортный маршрут адипокина. Вопрос о транспортировке различных секреторных продуктов ЖТ заслуживает, на наш взгляд, дальнейших исследований.
Данные, накопленные к настоящему времени, свидетельствуют о тесных межклеточных взаимодействиях между эндотелиальными клетками лимфатических сосудов и адипоцитами. Транскриптом эндотелиоцитов лимфатических сосудов насчитывает около 1600 генов [17]. Синтетическая функция этих клеток меняется при изменении потока интерстициальной жидкости, гипоксии и других «событиях», происходящих в тканевом микрорайоне [18]. Таким образом, эндотелиоциты обеспечивают пластичность лимфатических сосудов и оказывают влияние на микроокружение. Ряд гормонов и адипоцитокинов, продуцируемых в адипоцитах (в их числе лептин, адипонектин, IL-6, TNF-α и др.), влияют на функцию лимфатических эндотелиальных клеток и контролируют рост лимфатических сосудов [1]. Стволовые клетки ЖТ также могут активировать лимфангиогенез за счет секреции ангиогенных ростовых факторов [19], стимуляции пролиферации и миграции эндотелиоцитов [20], а также трансформации в клетки лимфатического эндотелия [21]. Кооперации между ЛС и ЖТ становятся патогенетически и клинически значимыми при лимфедеме и ожирении.
РЕМОДЕЛИРОВАНИЕ ЖИРОВОЙ ТКАНИ ПРИ ЛИМФЕДЕМЕ
Лимфедема — хроническое прогрессирующее заболевание, характеризующееся патологическим накоплением межклеточной жидкости с крупномолекулярными белками в интерстициальном пространстве вследствие дефекта лимфатического дренажа. Первичная лимфедема возникает в результате генетических дефектов, нарушающих развитие ЛС. Вторичная лимфедема — наиболее распространенная форма заболевания, вызывается повреждением путей лимфотока при хирургических вмешательствах, лучевой терапии, инфекциях или травмах [1][10]. Лимфедема является довольно распространенным заболеванием: в США им страдают не менее 5 млн человек [22].
Патогенез лимфедемы включает отек и фиброз тканей, повышение восприимчивости к инфекциям, а также интенсификацию адипогенеза [4]. Показано, что у мышей с гетерозиготным дефектом гена PROX1 лимфатические мальформации сочетаются с отложением жира вокруг мезентериальных лимфатических сосудов [23]. Усиленное депонирование жира наблюдается у больных с лимфедемой, при которой оно может быть выявлено с помощью ультразвукового исследования, магнитно-резонансной или компьютерной томографии, а также двухэнергетической рентгеновской абсорбциометрии [4]. Последняя позволяет количественно оценить массу мягких тканей, включая массу подкожного жира, на пораженной и непораженной конечностях (рис. 2). Недавнее исследование с применением магнитно-резонансной томографии показало, что отложение жира при лимфедеме может не ограничиваться подкожной жировой клетчаткой и затрагивать также мышечную ткань [24].
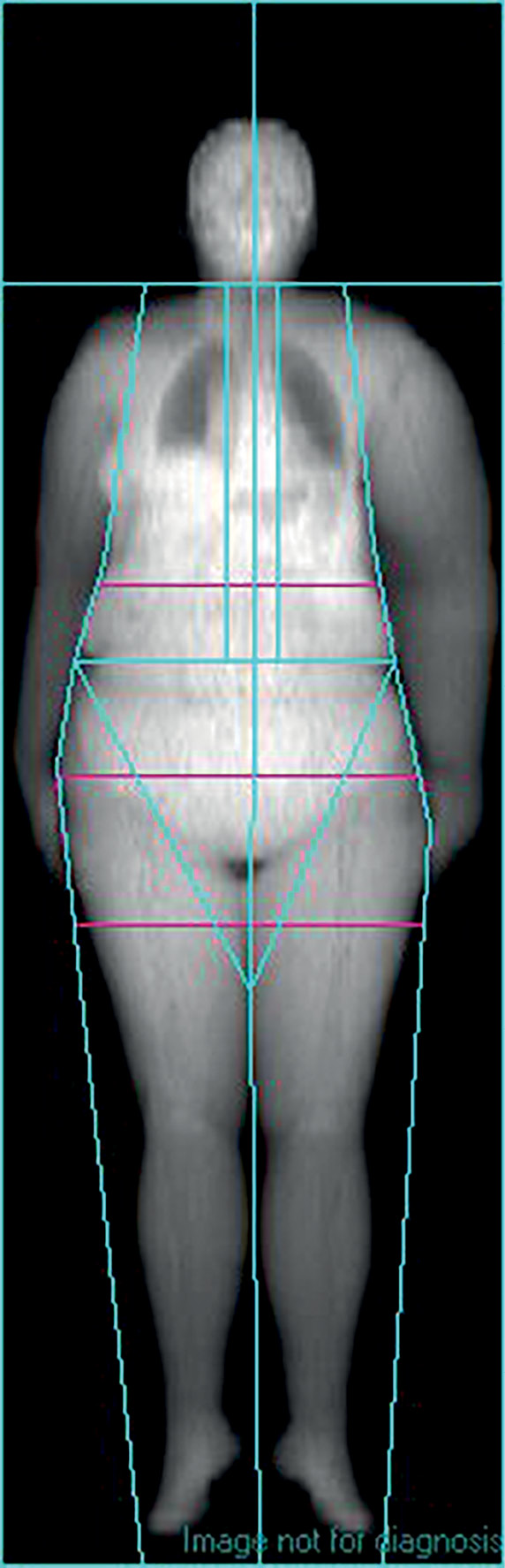
Рисунок 2. Вторичная лимфедема левой верхней конечности после оперативного лечения рака молочной железы.
Ч., 72 года. Оперативное лечение по поводу рака молочной железы в анамнезе (7 лет назад). Масса мягких тканей на правой руке 3,8 кг, на левой — 6,8 кг, масса жировой ткани — 1,7 и 3 кг соответственно. Двухэнергетическая рентгеновская абсорбциометрия на аппарате Lunar Prodigy (GE, США).
Механизмы активации адипогенеза при лимфедеме изучены недостаточно. Известно, что отложение ЖТ при лимфедеме связано с выраженностью лимфостаза и воспаления [25]. По экспериментальным данным, активация экспрессии провоспалительных генов при лимфедеме предшествует аккумуляции жира; блокада воспаления дексаметазоном препятствует адипогенезу [26]. Недавнее исследование ЖТ в зоне вторичной лимфедемы у женщин, оперированных по поводу рака молочной железы, показало усиление липолиза, лимфангиогенеза, повышение количества активированных CD4+ Т-лимфоцитов и секреции провоспалительных цитокинов [27]. В другом исследовании у больных с вторичной лимфедемой и в модели лимфедемы у мышей обнаружено повышение экспрессии провоспалительного цитокина IL-6, которое коррелировало с аккумуляцией ЖТ. Однако ингибирование IL-6 вызвало дальнейшее увеличение жироотложения, что указывает на то, что повышенный уровень данного цитокина являлся не причиной, а следствием активации адипогенеза [28]. Показано, что жидкость из лимфедематозной ЖТ стимулирует дифференцировку преадипоцитов in vitro [27]. Транскриптомный анализ мезенхимальных стволовых клеток ЖТ из областей вторичной лимфедемы выявил повышение экспрессии генов, связанных с клеточной пролиферацией и делением, а также усиленную дифференцировку этих клеток в адипоциты [29]. В экспериментах с удалением лимфоузлов у мышей показано, что повреждение ЛС и лимфостаз быстро активируют адипоциты и усиливают гены дифференцировки ЖТ, включая CCAAT/энхансер-связывающий белок α, а также рецептор, активируемый пролифератором пероксисом γ (PPARγ) [30, 31]. Расшифровка молекулярных механизмов адипогенеза при лимфедеме — задача дальнейших исследований.
ВЗАИМОДЕЙСТВИЯ МЕЖДУ ЛИМФАТИЧЕСКОЙ СИСТЕМОЙ И ЖИРОВОЙ ТКАНЬЮ ПРИ ОЖИРЕНИИ
Взаимодействия между ЛС и ЖТ, наблюдаемые при лимфедеме, в определенной степени реализуются и при ожирении. Более полувека назад ожирение было идентифицировано как фактор риска развития вторичной лимфедемы у онкологических больных [32]. На моделях заболевания у грызунов показано, что ожирение характеризуется замедлением транспорта интерстициальной жидкости, нарушением насосной функции лимфатических коллекторов и перестройками архитектуры лимфатических узлов [33–35].У мышей с ожирением и сахарным диабетом 2 типа, имеющих дефект гена рецептора лептина (db/db), выявлено резкое увеличение проницаемости собирательных лимфатических сосудов [36]. Эти наблюдения согласуются с результатами клинических наблюдений, зафиксировавших снижение клиренса макромолекул из подкожной жировой клетчатки у лиц с ожирением. Интересно, что пероральная нагрузка глюкозой сопровождалась увеличением лимфатического дренажа ЖТ у лиц с нормальной массой тела; данный эффект отсутствовал у тучных пациентов [37]. В недавнем исследовании с лимфосцинтиграфией и забором интерстициальной жидкости показано, что ухудшение лимфатического дренажа подкожной ЖТ у женщин в пременопаузе ассоциировано со снижением чувствительности подкожных адипоцитов к адренергическим стимулам и со снижением липолиза [38]. Ультраструктурные изменения эндотелиоцитов лимфатических сосудов подкожной ЖТ, косвенно свидетельствующие о нарушении микроциркуляции и лимфатического дренажа, выявлены у лиц с ожирением и сахарным диабетом 2 типа [39].
Снижение дренажно-транспортной функции ЛС при ожирении может возникать вследствие изменения состава межклеточной жидкости. Увеличение концентрации длинноцепочечных жирных кислот приводит к снижению экспрессии VEGFR-3 в лимфатических эндотелиальных клетках и активирует их апоптоз [35]. Другим эффектом жирных кислот является повышение проницаемости лимфатических эндотелиальных клеток [40]. Изменение продукции адипокинов также может влиять на ЛС. Один из наиболее характерных признаков дисфункции ЖТ при ожирении — снижение продукции адипонектина. Известно, что адипонектин повышает продукцию оксида азота в эндотелии кровеносных сосудов путем AMPK-зависимой активации эндотелиальной NO-cинтазы [41]. Сходный эффект адипонектина описан и в эндотелии лимфатических сосудов. В модели лимфедемы у мышей с нокаутированным геном адипонектина показано, что данный гормон регулирует дифференцировку и повышает выживаемость эндотелиоцитов; дефицит адипонектина снижает лимфангиогенез и усиливает развитие лимфедемы [42].
В настоящее время установлено, что нарушение лимфатического дренажа при ожирении тесно связано с развитием латентного (низкоинтенсивного) воспаления ЖТ. Корреляция между массой ЖТ с уровнем циркулирующих маркеров воспаления была показана в общепопуляционных исследованиях [43][44], а также у больных сахарным диабетом 2 типа [45][46]. В настоящее время хроническое воспаление ЖТ рассматривается как важный механизм в развитии инсулинорезистентности. Морфологическим признаком воспаления ЖТ является аккумуляция мононуклеарных лейкоцитов (макрофагов и Т-лимфоцитов) в интерстиции [47][48]. Показано, что воспалительная инфильтрация ЖТ при ожирении развивается вокруг лимфатических сосудов и сопровождается изменением экспрессии генов рецепторов воспалительных медиаторов в лимфатических эндотелиальных клетках [35][49]. Стимулом к провоспалительной активации эндотелиоцитов может быть стаз лимфы и/или изменение синтетической функции адипоцитов. Так, показано, что высокие концентрации лептина увеличивают синтез IL-6 в лимфатических эндотелиоцитах [50]. Показано, что провоспалительные цитокины (TNF-α, IL-6, IL-1β, особенно интерферон-γ) повышают проницаемость эндотелия лимфатических сосудов [51]. Последняя, как уже отмечалось, играет важную роль в обеспечении иммунорегуляторной функции ЖТ [16].
Увеличение продукции воспалительных медиаторов и нарушение трафика воспалительных клеток в условиях воспаления ЖТ могут вызывать дальнейшее нарушение дренажно-насосной функции ЛС. В экспериментах на мышах с алиментарным ожирением уменьшение перилимфатической воспалительной инфильтрации на фоне введения mTOR-ингибитора такролимуса сопровождалось повышением плотности и увеличением насосной функции лимфатических сосудов в ЖТ, а также улучшением клиренса интерстициальной жидкости [49]. Представленные данные свидетельствуют о тесных взаимосвязях между нарушениями метаболической и регуляторной функций адипоцитов и дренажно-транспортной функции ЛС при ожирении, который можно представить как порочный круг (рис. 3). Одним из механизмов, способных «разорвать» этот круг, могла бы стать активация лимфангиогенеза. Как уже отмечалось, новообразование лимфатических сосудов сопровождает многие воспалительные и репаративные процессы. Имеются данные, что численная и объемная плотность лимфатических сосудов в подкожной ЖТ у больных сахарным диабетом 2 типа и ожирением повышена в сравнении с лицами без диабета и ожирения [39], что не исключает активацию лимфангиогенеза. Можно предполагать, что стимулятором новообразования лимфатических сосудов при ожирении являются макрофаги и Т-лимфоциты, аккумулирующиеся в ЖТ. Иммунные клетки способны индуцировать лимфангиогенез посредством секреции ангиогенных факторов роста и провоспалительных цитокинов (VEGF-C, VEGF-D, TNF-α, ангиопоэтин-2, IL-1β, IL-18 и др.) [52]. Известно, что стимуляция лимфангиогенеза может как стимулировать, так и тормозить воспалительный ответ [53]. В связи с этим представляют несомненный интерес результаты недавних исследований, выполненных на мышах с изолированной гиперэкспрессией лимфотропного фактора VEGF-D в ЖТ. Развитие ожирения у этих животных сопровождалось формированием новых лимфатических сосудов, уменьшением макрофагальной инфильтрации ЖТ и улучшением метаболизма глюкозы [54][55].

Рисунок 3. Взаимосвязи между адипоцитами, лимфатическими сосудами и интерстицием жировой ткани при ожирении.
Перспективным направлением исследований является изучение роли мезентериальной ЛС в развитии ожирения и связанных с ним расстройств. Уменьшение диаметра и нарушение сократимости мезентериальных собирающих лимфатических сосудов наблюдалось в модели метаболического синдрома у крыс, вызванного диетой с высоким содержанием фруктозы [56]. В экспериментах на мышах установлено, что нарушение формирования «млечных» лимфатических сосудов, осуществляющих транспорт хиломикронов из кишечника, с помощью «выключения» генов VEGF-C или дельта-подобного Notch лиганда-4 (DLL-4) препятствует всасыванию жиров и развитию алиментарного ожирения [57][58]. Другими таргетными молекулами оказались нейропилин-1 и VEGFR-1 — рецепторы VEGF-A. Нокаутирование генов этих молекул нарушало функцию «молниеобразных» контактов между эндотелиоцитами лимфатических сосудов, что также приводило к мальабсорбции хиломикронов и «защищало» животных от ожирения [12]. В свою очередь, делеция гена-транспортера жирных кислот CD36/FAT дестабилизировала «пуговичные» межклеточные соединения между эндотелиоцитами, тормозила окисление жирных кислот, сигналинг VEGF-C и лимфангиогенез. В условиях in vivo это повышало проницаемость «млечных» сосудов, отходящих от кишечника, что вызывало «утечку» богатой хиломикронами лимфы, воспаление висцеральной ЖТ и развитие ожирения [59].
Предполагают, что иммунные клетки мезентериальной ЖТ могут играть важную роль в иммунном ответе на антигены, поступающие с лимфой от кишечника [16]. Как известно, одним из источников таких антигенов является кишечный микробиом. В последние годы накапливается все больше данных о том, что иммунометаболизм и метавоспаление при ожирении связаны с особенностями кишечной микробиоты [47][48]. Роль взаимодействий между мезентериальной ЛС и ЖТ в реализации эффектов кишечной микробиоты при ожирении — перспективное направление для будущих исследований.
Мезентериальная ЛС может играть важную роль в осложненном течении новой коронавирусной инфекции (COVID-19) у лиц с ожирением. Выдвинута гипотеза «лимфатико-легочной оси», согласно которой вызванное SARS-CoV2 увеличение кишечной проницаемости с повышенной транслокацией кишечной микробиоты и связанных с ней молекул (microbial-associated molecular patterns) у лиц с висцеральным ожирением приводит к резкому усилению воспалительного ответа мезентериальной ЖТ. В адипоцитах и макрофагах при этом синтезируется большое количество провоспалительных цитокинов (IL-6, TNF-α и др.), которые, поступая через ЛС в общую циркуляцию и достигая легких, включаются в формирование «цитокинового шторма» и респираторного дистресс-синдрома [60].
ЗАКЛЮЧЕНИЕ
Изучение взаимосвязей между ЛС и ЖТ можно считать новым и перспективным научным направлением. Накопленные к настоящему времени данные свидетельствуют, что ЛС участвует в реализации метаболической, эндокринной и иммунорегуляторной функции ЖТ. С другой стороны, адипоциты, а также стволовые клетки ЖТ вовлечены в регуляцию ремоделирования сети лимфатических сосудов. Кооперации между адипоцитами и эндотелиоцитами лимфатических сосудов играют важную роль при лимфедеме и ожирении. Данные патологические состояния, будучи изначально различными по своей этиологии, имеют много общего в патогенезе. Выраженные стадии лимфедемы характеризуются аккумуляцией ЖТ, а ожирение — нарушением функций ЛС. Связующим патогенетическим звеном в обоих случаях выступает воспаление. В будущих исследованиях предстоит определить особенности строения и функции лимфатического русла в висцеральной и подкожной, белой, бурой и бежевой ЖТ, выявить ключевые молекулы в межклеточных кооперациях между адипоцитами и лимфатическим эндотелием. Среди актуальных задач — идентификация молекулярных механизмов и сигнальных путей, определяющих ремоделирование ЖТ и ее лимфатической сети при лимфедеме и ожирении. Углубление знаний о взаимодействиях между ЛС и ЖТ, вероятно, позволит найти новые подходы к лечению этих социально значимых заболеваний.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена за счет средств государственного задания НИИКЭЛ — филиала ИЦиГ СО РАН.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Климонтов В.В. — концепция и дизайн исследования, поиск и анализ литературных данных, написание текста; Булумбаева Д.М. — поиск и анализ литературных данных, написание текста. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Благодарности. Авторы выражают признательность к.м.н., ст.н.с. НИИКЭЛ — филиал ИЦиГ СО РАН О.Н. Фазуллиной за предоставление данных двухэнергетической денситометрии.
Этические принципы. Проведение морфологических исследований жировой ткани было одобрено локальным этическим комитетом НИИКЭЛ — филиал ИЦиГ СО РАН (протокол № 88 от 22.11.2012). Пациенты добровольно подписали информированное согласие на публикацию персональной медицинской информации в обезличенной форме.
Список литературы
1. Коненков В.И., Бородин Ю.И., Любарский М.С. Лимфология. — Новосибирск: Манускрипт; 2012.
2. Escobedo N, Oliver G. The Lymphatic Vasculature: Its Role in Adipose Metabolism and Obesity. Cell Metab. 2017;3;26(4):598-609. doi: https://doi.org/10.1016/j.cmet.2017.07.020.
3. Bernier-Latmani, J, Petrova TV. Intestinal lymphatic vasculature: structure, mechanisms and functions. Nat Rev Gastroenterol Hepatol. 2017;14(9):510-526.
4. Azhar SH, Lim HY, Tan BK, Angeli V. The Unresolved Pathophysiology of Lymphedema. Front Physiol. 2020;11:137. doi: https://doi.org/10.3389/fphys.2020.00137.
5. Болезни жировой ткани / Под ред. И.И. Дедова. — М.: ГЭOTAP-Медиа; 2020.
6. Baluk P, Fuxe J, Hashizume H, et al. Functionally specialized junctions between endothelial cells of lymphatic vessels. J Exp Med. 2007;204:2349-2362. doi: https://doi.org/10.1084/jem.20062596.
7. Redondo, P, Gubert, F, Zaverucha-do-Valle C, et al. Lymphatic vessels in human adipose tissue. Cell Tissue Res. 2020;379:511-520. doi: https://doi.org/10.1007/s00441-019-03108-5.
8. Mortimer PS, Simmonds R, Rezvani M, et al. The measurement of skin lymph flow by isotope clearance--reliability, reproducibility, injection dynamics, and the effect of massage. J Invest Dermatol. 1990;95(6):677-682. doi: https://doi.org/10.1111/1523-1747.ep12514347.
9. Semo J, Nicenboim J, Yaniv K. Development of the lymphatic system: new questions and paradigms. Development. 2016;143(6):924-935. doi: https://doi.org/10.1242/dev.132431.
10. Choi I, Lee S, Hong YK. The new era of the lymphatic system: no longer secondary to the blood vascular system. Cold Spring Harb Perspect Med. 2012;2(4):a006445. doi: https://doi.org/10.1101/cshperspect.a006445.
11. Abouelkheir GR, Upchurch BD, Rutkowski JM. Lymphangiogenesis: fuel, smoke, or extinguisher of inflammation’s fire? Exp Biol Med (Maywood). 2017;242(8):884-895. doi: https://doi.org/10.1177/1535370217697385.
12. Sáinz-Jaspeado M, Claesson-Welsh L. Cytokines regulating lymphangiogenesis. Curr Opin Immunol. 2018;53:58-63. doi: https://doi.org/10.1016/j.coi.2018.04.003.
13. Vaahtomeri K, Karaman S, Mäkinen T, Alitalo K. Lymphangiogenesis guidance by paracrine and pericellular factors. Genes Dev. 2017;31(16):1615-1634. doi: https://doi.org/10.1101/gad.303776.117.
14. Zhang F, Zarkada G, Han J, et al. Lacteal junction zippering protects against diet-induced obesity. Science. 2018;361(6402):599-603. doi: https://doi.org/10.1126/science.aap9331.
15. Miller NE, Michel CC, Nanjee MN, et al. Secretion of adipokines by human adipose tissue in vivo: partitioning between capillary and lymphatic transport. Am J Physiol Endocrinol Metab. 2011;301(4):659-667. doi: https://doi.org/10.1152/ajpendo.00058.2011.
16. Kuan EL, Ivanov S, Bridenbaugh EA, et al. Collecting lymphatic vessel permeability facilitates adipose tissue inflammation and distribution of antigen to lymph node-homing adipose tissue dendritic cells. J Immunol. 2015;194(11):5200-5210. doi: https://doi.org/10.4049/jimmunol.1500221.
17. Becker J, Schwoch S, Zelent C, et al. Transcriptome Analysis of Hypoxic Lymphatic Endothelial Cells Indicates Their Potential to Contribute to Extracellular Matrix Rearrangement. Cells. 2021;10(5):1008. doi: https://doi.org/10.3390/cells10051008.
18. Wang Y, Simons M. Flow-regulated lymphatic vasculature development and signaling. Vasc Cell. 2014;6:14. doi: https://doi.org/10.1186/2045-824X-6-14.
19. Saijo H, Suzuki K, Yoshimoto H, et al. Paracrine Effects of Adipose-Derived Stem Cells Promote Lymphangiogenesis in Irradiated Lymphatic Endothelial Cells. Plast Reconstr Surg. 2019;143(6):1189e-1200e. doi: https://doi.org/10.1097/PRS.0000000000005669.
20. Strassburg S, Torio-Padron N, Finkenzeller G, et al. Adipose-Derived Stem Cells Support Lymphangiogenic Parameters In Vitro. J Cell Biochem. 2016;117(11):2620-2629. doi: https://doi.org/10.1002/jcb.25557.
21. Sun Y, Lu B, Deng J, et al. IL-7 enhances the differentiation of adipose-derived stem cells toward lymphatic endothelial cells through AKT signaling. Cell Biol Int. 2019;43(4):394-401. doi: https://doi.org/10.1002/cbin.11093.
22. Brayton KM, Hirsch AT, O Brien PJ, et al. Lymphedema prevalence and treatment benefits in cancer: impact of a therapeutic intervention on health outcomes and costs. PLoS One. 2014;9(12):e114597. doi: https://doi.org/10.1371/journal.pone.0114597.
23. Harvey NL, Srinivasan RS, Dillard ME, et al. Lymphatic vascular defects promoted by Prox1 haploinsufficiency cause adult-onset obesity. Nat Genet. 2005;37(10):1072-81. doi: https://doi.org/10.1038/ng1642.
24. Hoffner M, Peterson P, Månsson S, Brorson H. Lymphedema Leads to Fat Deposition in Muscle and Decreased Muscle/Water Volume After Liposuction: A Magnetic Resonance Imaging Study. Lymphat Res Biol. 2018;16(2):174-181. doi: https://doi.org/10.1089/lrb.2017.0042.
25. Avraham T, Zampell JC, Yan A. Th2 differentiation is necessary for soft tissue fibrosis and lymphatic dysfunction resulting from lymphedema. FASEB J. 2013;27(3):1114-1126. doi: https://doi.org/10.1096/fj.12-222695.
26. Cuadrado GA, de Andrade MFC, Ariga SK, et al. Inflammation Precedes Fat Deposition in an Experimental Model of Lymphedema. Lymphat Res Biol. 2021;19(2):116-125. doi: https://doi.org/10.1089/lrb.2020.0061.
27. Koc M, Wald M, Varaliová Z, et al. Lymphedema alters lipolytic, lipogenic, immune and angiogenic properties of adipose tissue: a hypothesis-generating study in breast cancer survivors. Sci Rep. 2021;11(1):8171. doi: https://doi.org/10.1038/s41598-021-87494-3.
28. Cuzzone DA, Weitman ES, Albano NJ. IL-6 regulates adipose deposition and homeostasis in lymphedema. Am J Physiol Heart Circ Physiol. 2014;306(10):1426-H1434. doi: https://doi.org/10.1152/ajpheart.01019.2013.
29. Xiang Q, Xu F, Li Y, et al. Transcriptome analysis and functional identification of adipose-derived mesenchymal stem cells in secondary lymphedema. Gland Surg. 2020;9(2):558-574. doi: https://doi.org/10.21037/gs.2020.02.09.
30. Zampell JC, Aschen S, Weitman ES, et al. Regulation of adipogenesis by lymphatic fluid stasis: part I. Adipogenesis, fibrosis, and inflammation. Plast Reconstr Surg, 2012;129(4):825-834. doi: https://doi.org/10.1097/PRS.0b013e3182450b2d.
31. Aschen S, Zampell JC, Elhadad S, et al. Regulation of adipogenesis by lymphatic fluid stasis: part II. Expression of adipose differentiation genes. Plast Reconstr Surg. 2012;129(4):838-847. doi: https://doi.org/10.1097/PRS.0b013e3182450b47.
32. Treves N. An evaluation of the etiological factors of lymphedema following radical mastectomy; an analysis of 1,007 cases. Cancer. 1957;10(3):444-59. doi: https://doi.org/10.1002/1097-0142(195705/06)10:3<444::aid-cncr2820100306>3.0.co;2-7.
33. Weitman ES, Aschen SZ, Farias-Eisner G, et al. Obesity impairs lymphatic fluid transport and dendritic cell migration to lymph nodes. PLoS One. 2013;8(8):e70703. doi: https://doi.org/10.1371/journal.pone.0070703.
34. Blum KS, Karaman S, Proulx ST. Chronic high-fat diet impairs collecting lymphatic vessel function in mice. PLoS One. 2014;9(4):94713. doi: https://doi.org/10.1371/journal.pone.0094713.
35. García Nores, GD, Cuzzone DA, Albano NJ, et al. Obesity but no thigh-fat diet impairs lymphatic function. Int J Obes (Lond). 2016;40(10):1582-1590. doi: 10.1038/ijo.2016.96.
36. Scallan JP, Hill MA, Davis MJ. Lymphatic vascular integrity is disrupted in type 2 diabetes due to impaired nitric oxide signalling. Cardiovasc Res. 2015;107(1):89-97. doi: https://doi.org/10.1093/cvr/cvv117.
37. Arngrim N, Simonsen L, Holst JJ, Bülow J. Reduced adipose tissue lymphatic drainage of macromolecules in obese subjects: a possible link between obesity and local tissue inflammation? Int J Obes (Lond). 2013;37(5):748-750. doi: https://doi.org/10.1038/ijo.2012.98.
38. Varaliova Z, Vlasak R, Cízkova T, et al. Lymphatic drainage affects lipolytic activity of femoral adipose tissue in women. Int J Obes (Lond). 2020;44(9):1974-1978. doi: https://doi.org/10.1038/s41366-020-0559-x.
39. Климонтов В.В., Булумбаева Д.М., Бгатова Н.П., и др. Концентрации адипокинов в сыворотке крови у пациентов с сахарным диабетом 2 типа: взаимосвязи с распределением, гипертрофией и васкуляризацией подкожной жировой ткани // Сахарный диабет. — 2019. — Т. 22. — №4. — С. 336-347.
40. Sawane M, Kajiya K, Kidoya H, et al. Apelin inhibits diet-induced obesity by enhancing lymphatic and blood vessel integrity. Diabetes. 2013;62(6):1970-1980. doi: https://doi.org/10.2337/db12-0604.
41. Achari AE, Jain SK. Adiponectin, a Therapeutic Target for Obesity, Diabetes, and Endothelial Dysfunction. Int J Mol Sci. 2017;18(6):1321. doi: https://doi.org/10.3390/ijms18061321.
42. Shimizu Y, Shibata R, Ishii M. Adiponectin-mediated modulation of lymphatic vessel formation and lymphedema. J Am Heart Assoc. 2013;2(5):e000438. doi: https://doi.org/10.1161/JAHA.113.000438.
43. Pettersson-Pablo P, Nilsson TK, Breimer LH, Hurtig-Wennlöf A. Body fat percentage is more strongly associated with biomarkers of low-grade inflammation than traditional cardiometabolic risk factors in healthy young adults — the Lifestyle, Biomarkers, and Atherosclerosis study. Scand J Clin Lab Invest. 2019;79(3):182-187. doi: https://doi.org/10.1080/00365513.2019.1576219.
44. Klevebro S, Björkander S, Ekström S, et al. Inflammation-related plasma protein levels and association with adiposity measurements in young adults. Sci Rep. 2021;31;11(1):11391. doi: https://doi.org/10.1038/s41598-021-90843-x.
45. Климонтов В.В., Тян Н.В., Фазуллина О.Н., и др. Белки острой фазы и адипоцитокины в сыворотке крови у женщин с сахарным диабетом 2 типа: взаимосвязи с композитным составом тела и колебаниями гликемии // Терапевтический архив. — 2016. — Т. 88. — №10. — С. 35-41.
46. Klimontov VV, Bulumbaeva DM, Fazullina ON, et al. Circulating Wnt1-inducible signaling pathway protein-1 (WISP-1/CCN4) is a novel biomarker of adiposity in subjects with type 2 diabetes. J Cell Commun. Signal. 2020;14(1):101-109. doi: https://doi.org/10.1007/s12079-019-00536-4.
47. Романцова Т.И., Сыч Ю.П. Иммунометаболизм и метавоспаление при ожирении // Ожирение и метаболизм. — 2019. — Т. 16. — №4. — С. 3-17.
48. Воротников А.В., Стафеев Ю.С., Меньшиков М.Ю., Шестакова М.В., Парфенова Е.В. Латентное воспаление и нарушение обновления жировых депо как механизм развития резистентности к инсулину при ожирении (Обзор) // Биохимия. — 2019. — T. 84. — №11. — С. 1649-1667.
49. Torrisi JS, Hespe GE, Cuzzone DA. Inhibition of Inflammation and iNOS Improves Lymphatic Function in Obesity. Sci Rep. 2016;6:19817. doi: https://doi.org/10.1038/srep19817.
50. Sato A, Kamekura R, Kawata K, et al. Novel mechanisms of compromised lymphatic endothelial cell homeostasis in obesity: the role of leptin in lymphatic endothelial cell tube formation and proliferation. PLoS One. 2016;11:e0158408. doi: https://doi.org/10.1371/journal.pone.0158408.
51. Cromer WE, Zawieja SD, Tharakan B, et al. The effects of inflammatory cytokines on lymphatic endothelial barrier function. Angiogenesis. 2014;17(2):395-406. doi: https://doi.org/10.1007/s10456-013-9393-2.
52. Corliss BA, Azimi MS, Munson JM, et al. Macrophages: An Inflammatory Link Between Angiogenesis and Lymphangiogenesis. Microcirculation. 2016;23(2):95-121. doi: https://doi.org/10.1111/micc.12259.
53. Kim H, Kataru RP, Koh GY. Inflammation-associated lymphangiogenesis: a double-edged sword? J Clin Invest. 2014;124(3):936-942. doi: https://doi.org/10.1172/JCI71607.
54. Chakraborty A, Barajas S, Lammoglia GM, et al. Vascular Endothelial Growth Factor-D (VEGF-D) Overexpression and Lymphatic Expansion in Murine Adipose Tissue Improves Metabolism in Obesity. Am J Pathol. 2019;189(4):924-939. doi: https://doi.org/10.1016/j.ajpath.2018.12.008.
55. Chakraborty A, Scogin CK, Rizwan KK, et al. Characterizing Lymphangiogenesis and Concurrent Inflammation in Adipose Tissue in Response to VEGF-D. Front Physiol. 2020;11:363. doi: https://doi.org/10.3389/fphys.2020.00363.
56. Zawieja SD, Wang W, Wu X, et al. Impairments in the intrinsic contractility of mesenteric collecting lymphatics in a rat model of metabolic syndrome. Am J Physiol Heart Circ Physiol. 2012;302(3):H643-H653. doi: https://doi.org/10.1152/ajpheart.00606.2011.
57. Nurmi H, Saharinen P, Zarkada G, et al. VEGF-C is required for intestinal lymphatic vessel maintenance and lipid absorption. EMBO Mol Med. 2015;7(11):1418-1425. doi: https://doi.org/10.15252/emmm.201505731.
58. Bernier-Latmani J, Cisarovsky C, Demir CS, et al. DLL4 promotes continuous adult intestinal lacteal regeneration and dietary fat transport. J Clin Invest. 2015;125(12):4572-4586. doi: https://doi.org/10.1172/JCI82045.
59. Cifarelli V, Appak-Baskoy S, Peche VS, et al. Visceral obesity and insulin resistance associate with CD36 deletion in lymphatic endothelial cells. Nat Commun. 2021;12(1):3350. doi: https://doi.org/10.1038/s41467-021-23808-3.
60. Uzzan M, Corcos O, Martin JC, et al. Why is SARS-CoV-2 infection more severe in obese men? The gut lymphatics — Lung axis hypothesis. Med Hypotheses. 2020;144:110023. doi: https://doi.org/10.1016/j.mehy.2020.110023.
Об авторах
В. В. КлимонтовРоссия
Климонтов Вадим Валерьевич, д.м.н., профессор; eLibrary SPIN: 1734-4030
Россия, 630060, Новосибирск, ул. Тимакова, д. 2
Д. М. Булумбаева
Россия
Булумбаева Динара Мухтаровна; eLibrary SPIN: 1153-7622
Дополнительные файлы
|
|
1. Рисунок 1. Визуализация лимфатических сосудов в подкожной жировой ткани у человека. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(333KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Вторичная лимфедема левой верхней конечности после оперативного лечения рака молочной железы. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(156KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Взаимосвязи между адипоцитами, лимфатическими сосудами и интерстицием жировой ткани при ожирении. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(383KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Климонтов В.В., Булумбаева Д.М. Лимфатическая система и жировая ткань: коммуникации в норме и патологии. Ожирение и метаболизм. 2021;18(3):336-344. https://doi.org/10.14341/omet12776
For citation:
Klimontov V.V., Bulumbaeva D.M. Lymphatic system and adipose tissue: Crosstalk in health and disease. Obesity and metabolism. 2021;18(3):336-344. (In Russ.) https://doi.org/10.14341/omet12776
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).










































