Перейти к:
Жировая ткань: цвета, депо и функции
https://doi.org/10.14341/omet12748
Аннотация
Ожирение — хроническое заболевание, характеризующееся избыточным накоплением жировой ткани. Распространенность ожирения и ассоциированных заболеваний побудила исследователей расширить исследования в области биологии жировой ткани. Благодаря новым технологиям в настоящее время существенно расширились представления о механизмах адипогенеза, особенностях метаболизма липидов и глюкозы, паракринной и эндокринной функции жировой ткани. Жировая ткань — сложный, гетерогенный эндокринный орган. Целый ряд оттенков адипоцитов отражает их морфологическую и функциональную гетерогенность. Основной функцией белой жировой ткани является запасание энергии. Бурые и белые адипоциты выполняют преимущественно термогенную функцию. Костномозговая (желтая) жировая ткань регулирует процессы костного ремоделирования и гемопоэза. Розовые адипоциты формируются во время беременности и обеспечивают энергетические потребности потомства. Изучение биологии жировой ткани играет важнейшую роль в понимании патофизиологии ожирения и определении его молекулярных взаимосвязей с сахарным диабетом 2 типа, сердечно-сосудистыми и онкологическими заболеваниями. В обзоре представлены современные данные литературы о происхождении, особенностях адипогенеза, функциональных свойствах жировой ткани в зависимости от ее клеточного состава и локализации. Изложены сведения о характере изменений жировой ткани при ожирении. Освещены вопросы клинической значимости и терапевтического потенциала различных депо жировой ткани.
Для цитирования:
Романцова Т.И. Жировая ткань: цвета, депо и функции. Ожирение и метаболизм. 2021;18(3):282-301. https://doi.org/10.14341/omet12748
For citation:
Romantsova T.I. Adipose tissue: colors, depots and functions. Obesity and metabolism. 2021;18(3):282-301. (In Russ.) https://doi.org/10.14341/omet12748
ВВЕДЕНИЕ
Ожирение — хроническое заболевание, характеризующееся избыточным накоплением жировой ткани, представляющим угрозу здоровью, и являющееся основным фактором риска других хронических заболеваний, включая сахарный диабет 2 типа (СД2) и сердечно-сосудистые заболевания [1]. По мере смены исторических эпох отношение общества к ожирению претерпело кардинальные изменения: от отчетливых ассоциаций с материальным достатком во времена античности и Средневековья, восторженных прославлений рубенсовских форм тела в период Ренессанса до крайней стигматизации в современном Голливуде. Несмотря на устоявшееся в последние годы негативное отношение к ожирению, темпы его распространения повсеместно возрастают. Эпидемия ожирения и ассоциированных заболеваний предопределила необходимость существенно расширить объем исследований в области физиологии и патофизиологии жировой ткани (ЖТ). Основными объектами изучения являются её развитие (органогенез, адипогенез), функции при гомеостазе, реакции в ответ на внешние факторы (дефицит или избыток нутриентов, изменения температурного режима, физические нагрузки и др.) [2].
У человека на долю ЖТ приходится от 3% (у профессиональных спортсменов) до 70% (при морбидном ожирении) массы тела [3]. ЖТ осуществляет множество жизненно важных функций. Она является основным энергетическим банком организма, служит ключевым связующим звеном в метаболических коммуникациях, регулирует процесс репродукции, координирует функцию иммунной системы, контролирует чувствительность тканей к инсулину, сосудистый тонус, костный метаболизм и гемопоэз; обеспечивает терморегуляцию. Функции ЖТ определяются происхождением входящих в ее состав клеток, особенностями их цвета (структуры) и локализации [4][5]. В зависимости от оттенков в настоящее время выделяют 5 типов адипоцитов. Белые адипоциты — доминирующие жировые клетки, которые располагаются в подкожных и висцеральных депо и ответственны за их экспансию при ожирении. Бурые адипоциты в виде небольших скоплений локализованы преимущественно в верхних отделах грудной клетки. Бежевые адипоциты сосредоточены в подкожной белой жировой ткани. Желтые адипоциты присутствуют в костном мозге длинных костей и позвоночника. Розовые адипоциты формируются в ткани молочной железы в период беременности и лактации (рис. 1) [6][7].

Рисунок 1. Фенотипические и функциональные свойства белых, бурых, бежевых, желтых, розовых адипоцитов (адаптировано из работы J. Zinngrebe и соавт., 2020) [7].
БЕЛАЯ ЖИРОВАЯ ТКАНЬ
Структура
Белая ЖТ на 55–80% состоит из зрелых адипоцитов (количество определяется спецификой конкретного депо), оставшаяся часть представлена клетками стромально-сосудистого комплекса, включающего мультипотентные мезенхимальные стромальные клетки, преадипоциты, фибробласты, клетки эндотелия и гладкой мускулатуры, клетки иммунной системы. Внеклеточный матрикс (ВКМ), поддерживающий клетки по типу гамака, состоит из структурных белков: протеогликанов, полисахаридов, различных видов коллагена, эластина, фибронектина и ламинина. ВКМ не только обеспечивает характерную архитектонику жировой ткани, он содержит целый ряд ростовых факторов и принимает непосредственное участие в адипогенезе и ангиогенезе [4]. ВКМ постоянно адаптируется к динамическим изменениям объема адипоцитов. Макрофаги-резиденты (М2-фенотип) вносят важный вклад в модификацию компонентов ВКМ, предопределяющих его эластичность. Учитывая доминирующую роль в процессе запасания и обеспечения организма энергией, ЖТ нуждается в гарантированной доставке должного количества кислорода и нутриентов. Соответственно, сохранность ее функций напрямую зависит от состояния сосудов. Развитое сосудистое русло является также источником мезенхимальных стволовых клеток, которые рекрутируются ЖТ для преобразования их в преадипоциты.
Зрелый адипоцит имеет сферическую форму, диаметр варьирует от 25 до 200 мкм. На долю единственной цитоплазматической вакуоли — жировой капли, содержащей триглицериды и, в небольшом количестве, эфиры холестерина, — приходится до 90% объема клетки (унилокулярный адипоцит). Бледная окраска наиболее крупной органеллы предопределяет белый цвет клетки при микроскопии. В оставшемся объеме адипоцита располагается ядро серповидной формы (как результат сдавливания липидной каплей) и цитоплазма, окружающая тонкой каймой центральную вакуоль. В цитоплазме содержится небольшое количество митохондрий продолговатой формы с хаотично расположенными криптами, гладкий эндоплазматический ретикулум, гранулярный эндоплазматический ретикулум, комплекс Гольджи, лизосомы, пероксисомы и пиноцитозные везикулы. Каждый белый адипоцит окружен базальной мембраной, состоящей преимущественно из коллагена IV типа. Внутренняя поверхность базальной мембраны представлена тонкой сетью микрофибрилл, внешняя поверхность — коллагеновыми волокнами [6].
Локализация
Основными депо белой ЖТ являются подкожное и висцеральное. Свыше 80% объема жировой ткани сосредоточено подкожно. В подкожном депо выделяют поверхностный и глубокий слои, абдоминальный (верхний) и глютеофеморальный (нижний) регионы. Висцеральное депо включает брыжеечный, сальниковый и ретроперитонеальный жир. Эктопический висцеральный жир располагается в средостении (интраторакальный, или паракардиальный, жир) и вокруг внутренних органов — сердца (эпикардиальный жир), желудка (эпигастральный жир), кровеносных сосудов (периваскулярный жир). В небольших количествах эктопический висцеральный жир пенетрирует в мышцы, печень, сердце, поджелудочную железу, почки [8]. На долю висцеральных депо приходится до 10–20% жировой ткани у мужчин, до 5–10% — у женщин. Каждое анатомическое депо имеет существенные отличия по генезу, клеточному составу, метаболизму, продукции адипокинов. Так, например, установлено, что источником висцеральных (но не подкожных) адипоцитов являются мезотелиальные клетки, содержащие маркер Wilms tumor 1 (WT1) [6]. Для подкожной ЖТ характерно высокое содержание зрелых адипоцитов (более 70% от клеточного состава), эпикардиальный и перикардиальный жир по сравнению с другими депо содержит наибольшее количество иммунных клеток (свыше 20%) [3]. При сопоставимых показателях индекса массы тела количество ЖТ у женщин в среднем на 10% выше, чем у мужчин. У женщин характерно отложение жира в области ягодиц и бедер, у мужчин — в области живота, что предопределяется генетическими особенностями и содержанием половых гормонов. В период менопаузы отмечается накопление жировой ткани преимущественно в висцеральных отделах. У грызунов трансплантация подкожной ЖТ улучшает метаболизм глюкозы, что свидетельствует о клеточно-автономной специфике данного депо, а не просто об особенностях анатомической локализации. Подкожные преадипоциты обладают высокой скоростью пролиферации и накопления липидов, в то время как висцеральные адипоциты характеризуются ускоренными темпами липолиза и повышенной склонностью к апоптозу [9]. Экспрессия генов, вовлеченных в процессы адипогенеза, ангиогенеза, метаболизма и воспаления, в различных жировых депо имеет свои характерные особенности. Ярким примером региональной гетерогенности ЖТ является разная степень ее потери при различных видах липодистрофии. Например, при 1-м типе врожденной генерализованной липодистрофии (синдром Берардинелли–Сейпа) жировая ткань практически полностью отсутствует, за исключением ладоней, стоп, ретро-орбитальных и пери-артикулярных зон. При семейной парциальной липодистрофии (синдром Даннигана–Кобберлинга) подкожная ЖТ исчезает на туловище и конечностях, при этом отмечается увеличение количества жира на лице, шее и в брюшной полости [10]. Учитывая выраженную клеточную и функциональную гетерогенность, в настоящее время каждое жировое депо рассматривается как отдельный мини-орган, экспрессирующий индивидуальную молекулярную программу [4].
Развитие, адипогенез
В эмбриональном периоде адипоциты образуются из мезенхимальных клеток, источником которых является латеральный слой мезодермы. Адипоциты краниофациальной локализации берут начало от клеток нейроэктодермы. У плода развитие белой ЖТ начинается во II триместре эмбриогенеза. В области головы и шеи накопление липидов в клетках наблюдается на 14-й неделе внутриутробной жизни, отдельные жировые дольки прослеживаются на 17-й неделе. Идентификация белых адипоцитов в области живота возможна к 14-й неделе, на стенках грудной клетки — к 15-й неделе, вдоль аорты и параренальной фасции — после 21-й недели. Конечности приобретают ЖТ после 23-й недели. На первом году жизни ЖТ продолжает свою экспансию путем гипертрофии (увеличение объема клеток) и гиперплазии (формирование новых адипоцитов). У взрослого человека обновление адипоцитов происходит со скоростью 10% в год. Характер экспансии ЖТ предопределяет метаболическое здоровье. Разрастание преимущественно подкожного депо, а также экспансия путем гиперплазии ассоциированы с кардиометаболической протекцией. Экспансия висцерального жира, равно как и увеличение количества ЖТ путем гипертрофии, сопряжены с развитием инсулинорезистентности и СД2 [2][11].
Адипогенез — сложный, многокомпонентно контролируемый процесс, во время которого мезенхимальные стволовые клетки дифференцируются в зрелые адипоциты. Адипогенез включает 2 этапа: детерминация и терминальная дифференцировка. В фазу детерминации происходит преобразование плюрипотентных стволовых клеток в унипотентные преадипоциты. Морфологически преадипоциты идентичны стволовым клеткам-предшественникам, однако потенциал дифференцировки в клетки других линий уже потерян. В фазу терминальной дифференцировки преадипоциты приобретают фенотип и функциональные характеристики зрелых адипоцитов. Мезенхимальные стволовые клетки стромально-сосудистого комплекса являются мультипотентными и могут дифференцироваться в остеогенные, хондрогенные, миогенные, адипогенные линии. Долгое время предполагалось, что все виды адипоцитов происходят от единой линии мезенхимальных клеток. Это представление изменилось благодаря развитию новых исследовательских технологий, в том числе генной инженерии, флуоресцентного сортинга. Идентификация популяции клеток, обладающих наиболее высоким адипогенным потенциалом, осуществляется на основе специфических поверхностных клеточных маркеров. Адипогенные клетки не имеют эндотелиального либо гематопоэтического происхождения: CD31-, CD45- (cluster of differentiation), экспрессируя при этом классические поверхностные маркеры мезенхимальных стволовых клеток Sca-1 (spinocerebellar ataxia type 1), CD24, CD34, CD29. В последующем из этого пула выделяют субпопуляцию клеток, экспрессирующих CD24. В 2008 г. были идентифицировали две различные популяции клеток-предшественников адипоцитов. Как клетки с панелью клеточных маркеров CD31-, CD45-, Sca-1+, CD34+, CD29+, CD24- (далее — CD24- клетки), так и предшественники с фенотипом CD31-, CD45-, Sca-1+, CD34+, CD29+, CD24+ (далее — CD24+клетки) индуцируют дифференциацию адипоцитов in vitro, однако их адипогенный потенциал в условиях in vivo имеет существенные отличия. Например, лишь CD24+клетки (но не CD24-клетки) способны воссоздать функционирующую ЖТ при их трансплантации в область резидуальных гонадных депо у мышей с липодистрофией. И напротив, лишь CD24-клетки при их внедрении в зоны, лишенные естественного микроокружения жировой ткани, активируют адипогенез. На основании этих данных был сделан вывод, что CD24-клетки представляют собой более поздние прогениторы, в то время как CD24+клетки являются примитивными клетками-предшественниками [2][12]. Сортинг предшественников адипоцитов лишь с учетом поверхностных маркеров Sca-1, CD34, CD29 не позволяет судить о реальном происхождении адипоцитов. Обе субпопуляции прогениторов экспрессируют ген PDGFRα (platelet-derived growth factor receptor α, рецептор тромбоцитарного фактора роста α). PDGFRá — поверхностные клеточные рецепторы тирозинкиназы, присутствующие в период развития плода в параксиальной мезодерме, а также во многих мезенхимальных клетках в течение взрослой жизни. Из клеток, экспрессирующих PDGFRα, определенные популяции адипоцитов могут формироваться как в период органогенеза, так и во взрослом возрасте. Клональный анализ показал, что до 80% клеток с фенотипом PDGFRα+, CD31-, CD45- участвуют в адипогенезе in vitro. Выделение предшественников адипоцитов с учетом экспрессии PDGFRα+ является наиболее распространенной методикой идентификации адипогенных клеток. Специфика ниши (микроокружение стволовых и прогениторных клеток, включающее сосуды, нервные волокна, внеклеточный матрикс, клетки иммунной системы, а также зрелые адипоциты) играет важнейшую роль в реализации адипогенеза [13][14]. Современные методы высокоразрешающего имиджинга позволяют получать информацию о распределении клеточных популяций in vivo и отслеживать их изменения в режиме реального времени. Эксперименты на трансгенных животных продемонстрировали, что до 35% адипоцитов подкожной ЖТ берут начало от костномозговых стволовых клеток (как мезенхимальных, так и гемопоэтических). Кроме того, источником новых адипоцитов могут быть перициты, эндотелиальные клетки, фибробласты [4][13]. Исследования с помощью метода РНК-секвенирования единых клеток (single-cell RNA-sequencing, scRNA-sq) позволили обнаружить несколько адипогенных прогениторов даже в пределах единого депо. Так, среди популяции висцеральных клеток, экспрессирующих PDGFRα, были идентифицированы несколько кластеров: клетки-предшественники адипоцитов, коммитированные преадипоциты, фибро-воспалительные прогениторы, мезотелиально-подобные клетки [15]. На основе применения scRNA-sq были открыты новые прогениторные клетки: адипогенез-регуляторные клетки (adipogenesis-regulatory cells, Aregs), ДПП4+-мультипотентные прогениторы (дипептидилпептидаза-4, DPP4+ multipotent progenitors), ассоциированный с СД2 подтип адипогенных прогениторов (type 2 diabetes mellitus-associated adipocyte progenitor subtype) и др. [16]. Общим итогом выполненных на сегодняшний день исследований в области адипогенеза является подтверждение чрезвычайной гетерогенности популяции адипогенных клеток-предшественников, что лежит в основе многообразия функций ЖТ.
В программе адипогенеза задействовано свыше 1200 генов, более 100 транскрипционных факторов, множество сигнальных путей. Транскрипционные факторы определяют выбор пути развития клетки за счет управления экспрессией целого ряда генов [13]. Факторы транскрипции CCAAT-энхансер-связывающие протеины β и δ (CCAAT/enhancer binding proteins β/δ, С/EBP β/δ), факторы KLF (Krüppel-подобные факторы), CREB (белок, связывающий цАМФ-зависимый элемент, cAMP response element-binding protein) первыми реагируют на адипогенные стимулы и запускают адипогенный каскад. Костные морфогенетические протеины (bone morphogenetic proteins, BMPs) — мощные факторы роста, принадлежащие к суперсемейству фактора роста опухоли β. Один из членов семейства BMPs–BMP4 вовлечен в процесс детерминации (коммитирования) плюрипотентных стволовых клеток в адипоцитарную, хондроцитарную либо остеобластную линии. Связываясь со специфическими рецепторами, расположенными на поверхности клеток, BMP4 индуцирует фосфорилирование ряда структурно сходных белков семейства фактора транскрипции SMAD (similar to “Mothers Against Decapentaplegic”). Фосфорилированные SMAD-1, -4, -5, -8 объединяются, данный комплекс транслоцируется в клеточное ядро, что способствует адипогенному коммитированию. Коммитированные преадипоциты экспрессируют цинк-пальцевый белок 423 (zink-finger protein 423, ZFP 423), который является важнейшим детерминатором формирования белых адипоцитов. В фазе дифференциации детерминированные преадипоциты прекращают свой рост и активируют факторы транскрипции PPARγ (рецептор, активируемый пролифератором пероксисом γ, peroxisome proliferator-activated receptor γ) и С/EBPα. Оба эти важнейших регулятора адипогенеза — PPARγ и С/EBPα — индуцируют и поддерживают программу формирования зрелых адипоцитов и экспрессию их ключевых генов (транспортера глюкозы 4 типа — ГЛЮТ4, адипоцит-селективного протеина, связывающего жирные кислоты-2 (adipocyte protein 2, АР2), адипонектина (ADIPOQ) и др.). Целый ряд транскрипционных факторов репрессирует адипогенез, к их числу относятся фактор роста фибробластов-2, активин А, преадипоцитарный фактор 1, ZFP 521, фактор-1 преадипоцитов (preadipocyte factor-1, Pref-1) и др. Гормоны играют важнейшую роль в адипогенезе. Так, инсулин, связываясь со своим рецептором, запускает внутриклеточный сигнальный каскад с участием киназы Akt и транскрипционных факторов семейства FOXO (forkhead box-O), что приводит к адипогенной дифференцировке [17]. Кортизол способствует увеличению содержания центрально расположенных жировых отложений (подкожных и висцеральных). Под влиянием эстрогенов возрастает количество подкожной ЖТ преимущественно в глютеофеморальной области. Гормон роста, напротив, уменьшает объем подкожного депо. Лептин подавляет адипогенез, в то время как адипонектин активирует этот процесс [13][14].
Уникальным свойством белой ЖТ является ее пластичность, которая проявляется не только возможностью многократного изменения объема адипоцитов, но и кардинальным преобразованием их фенотипа и функций путем дедифференциации и трансдифференциации. Как в физиологических условиях, так и при ряде заболеваний зрелые адипоциты способны дедифференцироваться и вновь приобретать свойства преадипоцитов либо плюрипотентных стволовых клеток. Подтверждена роль дедифференцированных адипоцитов в патогенезе липосаркомы. Трансдифференциация — процесс трансформации терминально дифференцированных клеток в принципиально иной тип специализированных клеток. Путем трансдифференциации адипоциты дермы могут преобразовываться в миофибробласты и участвовать в процессах заживления ран. Белые подкожные адипоциты путем трансдифференциации дают начало розовым и бежевым адипоцитам [6][18].
Основные функции
Особенность геометрии белого адипоцита — сферическая форма — обеспечивает ему возможность занимать максимально допустимый объем в сравнительно небольшом пространстве, что подчинено важнейшей функции — эффективному запасанию липидов для энергоснабжения организма. У взрослого человека с нормальной массой тела липидные капли адипоцитов содержат в среднем 500 000 кДЖ энергии, этот ресурс достаточен для пробега 30 марафонов либо поддержания обычного метаболического баланса в течение 2 мес. [6][19]. В процессе липогенеза адипоцит утилизирует свободные жирные кислоты (СЖК), источником которых являются триглицериды (ТГ) кровяного русла. При достаточном поступлении нутриентов синтезированные в печени и кишечнике ТГ поступают в ЖТ в виде липопротеинов и с участием липопротеиновой липазы гидролизуются до СЖК на поверхности эндотелиальных клеток капилляров. В последующем СЖК поступают в просвет сосудов и захватываются адипоцитами с помощью транспортеров жирных кислот (ЖК), таких как ЖК-транспортные протеины, ЖК-связывающие протеины, кавеолины. Помимо экзогенных, адипоциты могут синтезировать эндогенные ЖК, используя для этого поступающую в клетку глюкозу — липогенез de novo. Эндогенные ЖК играют важную роль в регуляции чувствительности к инсулину и энергетического гомеостаза. В конечном итоге под влиянием целого ряда ферментов ЖК эстерифицируются до ТГ и включаются в липидные капли. Инсулин является важнейшим гормоном, стимулирующим липогенез. Липолиз находится под контролем 3 ферментов — адипоцитарной триглицеридлипазы, гормон-чувствительной липазы и моноацилглицерин-липазы. В ходе липолиза происходит гидролизация ТГ до свободного глицерина и 3 молекул ЖК; этот процесс реализуется как в базальных условиях, так и под влиянием гормонов — катехоламинов, глюкагона, кортизола [19][20].
Белая ЖТ является самым большим эндокринным органом, вырабатывая множество адипокинов — биологически активных субстанций, действующих на основе паракринных, аутокринных либо эндокринных механизмов и осуществляющих коммуникации с центральной нервной системой, сердцем, мышечной тканью, сосудами, поджелудочной железой, другими органами и тканями. Адипокины продуцируются не только адипоцитами, но и клетками стромально-сосудистого комплекса: преадипоцитами, эндотелиальными и иммунными клетками, фибробластами. Например, провоспалительный адипокин фактор некроза опухоли α (ФНО-α) преимущественно экспрессируется в моноцитах и макрофагах. Локально, в пределах ЖТ адипокины принимают участие в адипогенезе, ангиогенезе, миграции иммунных клеток и метаболизме. На системном уровне адипокины регулируют энергобаланс, чувствительность тканей к инсулину и его секрецию, а также контролируют функции иммунной, репродуктивной, сердечно-сосудистой, опорно-двигательной систем. Адипокины, содержащие N-терминальный сигнальный пептид (например, лептин и адипонектин), покидают клетку классически с вовлечением эндоплазматического ретикулума и аппарата Гольджи. При отсутствии сигнального пептида адипокины продуцируются альтернативным способом: с помощью транспортер-опосредованного экспорта (например, так поступает в кровоток фактор роста фибробластов-2), микровезикул и экзосом (интерлейкин-1β) и путем селективного посттрансляционного гидролиза с поверхности клетки — «излития» (ФНО-α). К настоящему времени идентифицировано свыше 700 адипокинов, зарегистрированных в специализированной базе данных (http:/www.diabesityprot.org); их количество постоянно возрастает [21][22].
Белая ЖТ осуществляет термальную защиту, а также выполняет роль амортизатора для ряда органов: от наиболее хрупких структур (например, орбита глаз окружена жиром наподобие чашки, обернутой пузырчатой пленкой) до испытывающих постоянный механический стресс отделов тела (пятки и пальцы ног). Белые адипоциты, располагающиеся внутри дермы, отличаются по своему происхождению от подкожных адипоцитов и принимают участие в заживлении ран, поддержании метаболизма волосяных фолликулов и обеспечении резистентности к патогенным микроорганизмам [5].
Влияние ожирения
При ожирении ЖТ подвергается патологическому ремоделированию. Нарушение адипогенеза приводит к формированию гипертрофического ожирения. Гипертрофированные адипоциты вырабатывают большое количество провоспалительных цитокинов, включая ФНО-α, интерлейкин-6, моноцитарный хемо-аттрактантный протеин-1, С-реактивный белок (СРБ) и др. Гипертрофия адипоцитов в сочетании со снижением ангиогенеза способствует развитию выраженной гипоксии, которая является триггером гибели адипоцитов путем ишемического некроза и апоптоза. В свою очередь, это стимулирует инфильтрацию ЖТ активированными макрофагами-рекрутами [5]. Продукция провоспалительных цитокинов резко возрастает, нарушается проведение сигналов инсулина. В зависимости от условий, клетки-предшественники адипоцитов могут менять программу дифференцировки от адипогенеза к фиброгенезу [18]. Пролиферация фибробластов приводит к избыточному накоплению коллагена, что снижает пластичность ЖТ. Экспансия адипоцитов в условиях ригидного микроокружения ассоциирована с развитием механического стресса, способствующего прогрессирующей гиперпродукции провоспалительных цитокинов. Фиброз ВКМ ограничивает возможность адипоцитов накапливать липиды (размер адипоцита обратно пропорционален степени фиброза), начинается эктопия жира в «тощие» ткани [23].
Терапевтический потенциал
Гипертрофическое ожирение, сопровождающееся локальным и системным метавоспалением, предопределяет развитие множества ассоциированных заболеваний. Современные методы лечения ожирения, направленные в конечном итоге на уменьшение объема ЖТ, включают модификацию образа жизни, фармакотерапию, оперативное лечение. Арсенал зарегистрированных фармакологических препаратов на сегодняшний день крайне ограничен. Тем не менее в настоящее время порядка 250 молекул рассматриваются в качестве потенциальных лекарственных средств [24]. На разных этапах клинических исследований проводится оценка эффективности и безопасности агонистов рецепторов глюкагоноподобного пептида-1 (ГПП-1), а также мульти-агонистов рецепторов ГПП-1. Изучаются свойства новых ингибиторов обратного захвата моноаминов, селективных (периферических) антагонистов каннабиноидных рецепторов, агонистов рецепторов меланокортина 4 типа [25]. Разрабатывается таргетная терапия, направленная на моделирование процессов адипогенеза и ангиогенеза, снижение метавоспаления ЖТ; изучаются терапевтические возможности адипокинов. Помимо важнейшего энергетического банка, белая ЖТ служит резервуаром мультипотентных стволовых клеток. Их количество составляет 100 000 на грамм, 17% от общего состава клеток (в костном мозге — лишь 0,01%), таким образом, ЖТ представляет собой своего рода «клеточный супермаркет». Учитывая распространенность липосакций (в среднем в США ежегодно проводится свыше 400 000 вмешательств), в ходе которых удаляется порядка 3 л аспирата, дальнейшее изучение механизмов адипогенеза открывает большие перспективы для развития регенеративной медицины. В частности, изучается возможность применения дедифференцированных белых адипоцитов в качестве источника стволовых клеток для лечения повреждений сердечной ткани и спинного мозга [5][18].
БУРАЯ И БЕЖЕВАЯ ЖИРОВАЯ ТКАНЬ
Открытие бурой ЖТ, состоявшееся в 1551 г., принадлежит шведскому натуралисту Конраду Гесснеру, обнаружившему ее присутствие в межлопаточной области у сурков и описавшему ее структуру как «ни плоть, ни жир, а нечто среднее»; тогда же было высказано предположение о значимости бурой ЖТ для процесса гибернации (зимняя спячка). В последующем выдвигались гипотезы, согласно которым бурая ЖТ представляет собой фрагмент вилочковой железы, либо особую эндокринную железу, участвующую в выработке элементов крови, либо резервуар для хранения пищевых субстратов. Лишь в 1961 г. была окончательно подтверждена важнейшая роль бурой ЖТ в обеспечении несократительного термогенеза [26]. Термогенный эффект бурых адипоцитов реализуется посредством трансмембранного белка UCP-1 (uncouple protein 1, разобщающий протеин 1, термогенин), локализованного во внутренней мембране митохондрий. Митохондрии в большинстве клеток продуцируют АТФ при действии АТФ-синтазы, используя сформированный ею высокий градиент протонов по обе стороны внутренней мембраны клеточных органелл. UCP-1 уменьшает градиент протонов, разобщает физико-химические реакции дыхательных цепей и фосфорилирования, активируя процессы термогенеза [27]. Интерес к бурой ЖТ возрос в начале 2000-х годов после доказательства ее присутствия не только у ребенка, но и у взрослого человека [28]. Позднее был открыт еще один вид термогенных жировых клеток — бежевые адипоциты [29]. В отличие от классических, конститутивных бурых жировых клеток, развивающихся в период эмбриогенеза, бежевые адипоциты определяют как индуцированные, не классические, рекрутируемые. В обычных условиях бежевые адипоциты содержат крайне низкое (сопоставимое с белыми адипоцитами) количество UCP-1. Его экспрессия резко повышается в ответ на адренергические стимулы. Несмотря на морфологическое и функциональное сходство с бурыми адипоцитами, бежевые клетки образуются в процессе особой программы адипогенеза [30].
Структура
До 20–30% объема бурой ЖТ составляют зрелые адипоциты. Стромальная сосудистая фракция представлена преадипоцитами, стволовыми, эндотелиальными, нейрональными и гемопоэтическими клетками. Бурые адипоциты имеют полигональную форму, их размер вдвое меньше размера белых адипоцитов. Округлое ядро, как правило, располагается в центре клетки. Цитоплазматические липиды содержатся в нескольких небольших вакуолях (мультилокулярный адипоцит). Крупные многочисленные митохондрии сферической формы упакованы с образованием пластинчатых крипт, что свидетельствует о мощном энергетическом потенциале. Бурый цвет клеток обусловлен высоким содержанием цитохромов в митохондриях [31][32]. Идентифицированы бурые адипоциты с высокой и низкой экспрессией UCP-1, а также клетки с высокой и низкой экспрессией адипонектина, отличающиеся размерами липидных капель и содержанием митохондрий [32]. Фенотип бежевых адипоцитов определяется их функциональным состоянием. В покое они представляют собой схожие с белыми адипоцитами бледные унилокулярные клетки. При активации их морфология приобретает сходство с бурыми адипоцитами (браунинг, от англ. «browning»), включая обилие митохондрий и мультилокулярный вариант хранения липидов, но липидные капли более мелкие. Двойственные функциональные свойства и морфологические особенности бежевых клеток отражены в их названии. Помимо развитой системы капилляров (до 5 на 1 клетку), бурая и бежевая ЖТ характеризуется большим количеством симпатических нервных волокон [30]. С возрастом морфология термогенной ЖТ меняется. У грудных детей и в первую декаду жизни мультилокулярные адипоциты — преобладающие клетки, у взрослого человека бурая жировая ткань содержит гетерогенную смесь мультилокулярных и унилокулярных клеток с более высоким содержанием липидов [32].
Локализация
Золотым стандартом изучения локализации и содержания бурой ЖТ является позитронно-эмиссионная томография с использованием 18F-флюородеоксиглюкозы в комбинации с компьютерной томографией (18F-ФДГ ПЭТ/КТ). Систематический обзор исследований с использованием 18F-ФДГ ПЭТ/КТ показал, что спонтанно определяемая (в условиях обычной температуры) бурая ЖТ присутствует у 6,8–8,5% взрослых здоровых людей. При воздействии низких температур частота ее выявления составляет от 20 до 100%; объем варьирует от 4 мл до 1400 мл. С учетом максимального потенциала активации и браунинга, объем термогенной ЖТ составляет 510–2358 мл, масса — 459–2122 г [33][34]. Помимо ПЭТ/КТ, исследования проводятся с использованием МР-томографии, спектрометрии, контрастного ультразвука, термографии [35]. Результаты аутопсии и МР-томографии свидетельствуют о постоянном присутствии бурой ЖТ у новорожденных, составляющей до 5% массы тела; в этот период жизни наибольшее количество сосредоточено в межлопаточном пространстве. Активная бурая ЖТ у взрослого человека локализована в 6 основных подкожных депо, в совокупности напоминающих очертания теплового жилета. Они включают надключичные (≈67% от всего объема бурой жировой ткани), шейные, аксиллярные, абдоминальные, медиастинальные и параспинальные регионы. На долю этих депо приходится 1,5% общей массы тела (4,3% общей массы жира). Небольшие скопления висцеральной бурой ЖТ локализованы вблизи сосудов (аорта, общая сонная артерия, брахиоцефальная артерия, паракардиальный жир, эпикардиальная коронарная артерия и сердечные вены, внутренняя грудная артерия, межреберные артерии и вены), вокруг полых мышечных структур (трахея, пищевод, сердце, главные бронхи, диафрагма, мезоколон), вблизи солидных органов (поджелудочная железа, печень, почки, надпочечники, селезенка) [36][37].
Бежевые адипоциты располагаются в белой ЖТ (brite — акроним от «brown in white»), преимущественно в ее подкожных депо. У ряда пациентов с феохромоцитомой значимый захват может отмечаться и в висцеральных белых жировых депо, в данном случае браунинг белых адипоцитов обусловлен длительной стимуляцией эндогенными катехоламинами. После удаления опухоли захват 18F-ФДГ в висцеральных депо уже не прослеживается. Количество термогенных адипоцитов уменьшается в пожилом возрасте, у больных ожирением, у пациентов с СД2 [30][37].
Развитие, адипогенез
У плода человека формирование бурой ЖТ начинается во II триместре беременности. Исходно бурый жир накапливается в области головы и шеи с последующим охватом грудных отделов тела, верхних и нижних конечностей. Предшественники бурых адипоцитов берут начало от мультипотентных прогениторных клеток центрального дермомиотома, экспрессирующих EN1(engrailed 1), PAX3 (pairbox 3), PAX7, MYF5 (myogenic factor 5), Meox1 (mesenchyme homeobox 1). Указанные прогениторы могут также дифференцироваться в клетки скелетных мышц, кожи и ряд белых адипоцитов. Коммитированные предшественники преобразуются в бурые преадипоциты, экспрессирующие EBF2 (early B-cell factor 2). Множество факторов транскрипции описано в качестве ключевых регуляторов развития бурой и бежевой ЖТ, таких как PPARγ, C/EBPs, PPARγ-коактиватор 1α (PPARγ coactivator 1α, PGC-1α), PRDM16 (positive regulatory domain I-binding factor 16), ZFP516, EHMT1 (euchromatic histone-lysine N-methyltrasferase 1), BMP7, некоторые формы микроРНК. PPARγ принимает активное участие в программе дифференцировки не только белых, но и бурых адипоцитов и индуцирует экспрессию UCP-1 в процессе адипогенеза. Важнейшим регулятором дифференциации термогенных адипоцитов является PRDM16, который подавляет экспрессию генов мышечных клеток, фибробластов и белых адипоцитов. Под влиянием PRDM16, тесно взаимодействующего с PPARγ и другими адипогенными факторами транскрипции, бурые преадипоциты трансформируются в классические зрелые бурые жировые клетки, характеризующиеся экспрессией UCP-1, PGC-1α, PRDM16, CIDEA (cell death-inducing DFFA- like effector А) [38][39].
По сравнению с бурыми адипоцитами, бежевые жировые клетки характеризуются более выраженной гетерогенностью. Их подтипы определяются не только локализацией, но и характером активирующих факторов. Бежевые адипоциты формируются при задействовании 3 основных процессов: 1) путем пролиферации и de novo дифференциации из различных пулов предшественников; 2) путем трансдифференциации зрелых белых адипоцитов; 3) путем активации «дремлющих» бежевых клеток [40]. Предшественники бежевых адипоцитов экспрессируют гены SMA (smooth muscle actin), Myh11(myosin heavy chain 11), Pdgfra и Pdgfrb. Кроме того, ряд бежевых клеток-прогениторов характеризуется маркерами Pax3, Myh5, СD81 [39][43]. Зрелые бежевые адипоциты имеют некоторые маркеры, присущие белым и бурым адипоцитам, а также собственные отличительные маркеры, включая CD137, Tbx1 (T-box 1), Tmem 26 (transmembrane protein 26), Cited1 (Cbp/p300-interacting transactivator with Glu/Asp-rich carboxy-terminal domain 1), Shox2 (short stature homeobox 2), Dio2 (iodothyronine deiodinase 2), PGC-1α [39][41][42]. Трансдифференциация белых адипоцитов в бежевые является обратимой. Конверсия бежевого фенотипа в белый (побеление) сопровождается отчетливым сокращением количества митохондрий вследствие митофагии — селективной формы аутофагии в отношении митохондриальной деградации. Блокада аутофагии путем делеции генов Atg5 (autophagy related 5) либо Atg12 предотвращает переход бежевых адипоцитов в белые даже после отмены действия внешних стимулов [43].
Множество внутренних и внешних факторов принимают участие в активации бурых адипоцитов и браунинге белой ЖТ. Низкая температура окружающей среды — классический активатор термогенеза как у животных, так и у человека. Холод стимулирует терморецепторы кожи, что, в свою очередь, активирует нейроны гипоталамических ядер, регулирующие температуру тела. Эфферентные сигналы, поступающие к симпатическим нервным терминалям, являются триггером для выработки норадреналина. Норадреналин связывается с β3-адренергическими рецепторами, расположенными на термогенных адипоцитах, и активирует внутриклеточный сигнальный каскад с участием аденилатциклазы и 3,5-циклического аденозинмонофосфата (цАМФ). Протеинкиназа А (ПКА), активированная цАМФ, инициирует липолиз в бурых адипоцитах путем фосфорилирования гормон-чувствительной липазы, адипоцитарной триглицеридлипазы и перилипина. В результате образуются СЖК, служащие основным субстратом термогенеза. Помимо внутриклеточного пула ТГ, термогенные адипоциты используют в качестве источника энергии циркулирующие в сосудистом русле липиды, аминокислоты, а также глюкозу, на долю которой в качестве энергетического субстрата приходится до 10% [44]. Адренергическая стимуляция с вовлечением цАМФ повышает транскрипцию ГЛЮТ1 и способствует его транслокации к клеточной мембране, в то время как инсулин путем воздействия на фосфатидилинозитол-3-киназу индуцирует транслокацию ГЛЮТ4. При поступлении в термогенный адипоцит до 25% глюкозы подвергается гликолизу, остальное количество используется для липогенеза de novo и реакций окисления жирных кислот [45]. Идентифицирован особый тип бежевых адипоцитов, использующих глюкозу как приоритетный метаболический субстрат (g-beige adipocyte) [39]. Хроническая норадренергическая стимуляция индуцирует не только термогенез, но и процессы тканевого роста (гиперплазию, гипертрофию клеток) и браунинга. Тиреоидные гормоны повышают чувствительность к адренергическим стимулам. Высокая экспрессия дейодиназы 2 типа (Dio2) является одним из характерных свойств бурой ЖТ. Dio2 конвертирует тироксин в трийодтиронин, представляющий критическую значимость для реализации термогенной функции [42].
У животных увеличение количества бежевых адипоцитов отмечается при возрастании физической активности, что обусловлено эффектом ряда миокинов — ирисина, интерлейкина-6 (ИЛ-6), лактата. Убедительных данных о воздействии физической нагрузки на бурые и бежевые адипоциты человека в настоящее время не получено. Прием пищи сопряжен с активацией термогенеза; ряд пищевых компонентов (капсаицин, ресвератрол, куркумин, ментол, катехины, кофеин) оказывает особо отчетливое стимулирующее влияние на термогенные адипоциты. К числу гормональных активаторов термогенеза, помимо тиреоидных гормонов, относятся инсулин, лептин, адипонектин, глюкагоноподобный пептид-1, эстрадиол, натрийуретические пептиды, орексины. Помимо пациентов с феохромоцитомой, активация браунинга отмечается у больных с ожоговой травмой (как результат хронического воздействия норадреналина вследствие перенесенного тяжелого стресса), у пациентов с кахексией на фоне онкопатологии. Активация бурых и бежевых адипоцитов прослеживается под действием адренергических препаратов (эфедрина, мирабегрона), при назначении тиазолидиндионов. Применение неселективного бета-блокатора пропранолола, напротив, снижает захват 18F-ФДГ по данным ПЭТ/КТ [30][39][46]. Помимо основного, UCP-1-зависимого механизма, бежевые адипоциты могут осуществлять термогенез при задействовании альтернативных механизмов — фосфокреатин/креатин-футильного цикла, АТФ-зависимого кальциевого цикла, АМПК-зависимого термогенеза и др. [43].
Браунинг белой ЖТ происходит с участием клеток иммунной системы, в том числе макрофагов. Индукция бежевого адипогенеза начинается с клиренса макрофагами погибших белых адипоцитов, лишь вслед за этим активируется рекрутирование бежевых адипогенных прогениторов. Кроме того, макрофаги, как и нервные волокна, секретируют норадреналин, усиливающий процессы браунинга [39]. В ряде исследований было отмечено, что грудное вскармливание у детей снижает риск развития ожирения. H. Yu и соавт. показали, что к числу активаторов браунинга у младенцев относятся специфические липидные медиаторы алкилглицерины (АКГ), входящие в состав грудного молока. В макрофагах грудного ребенка АКГ метаболизируются в тромбоцит-активирующий фактор (ТАФ), который индуцирует выработку ИЛ-6. В свою очередь, ИЛ-6 активирует JAK/STAT-сигнальные пути (Janus kinase/signal transducers and activators of transcription signaling pathway) в белых адипоцитах и индуцирует браунинг. Дефицит АКГ в раннем детском возрасте приводит к преждевременной потере термогенных адипоцитов, что повышает риск ожирения (рис. 2) [47].
Основные функции
Бурая ЖТ сохранилась в процессе эволюции млекопитающих как надежная защитная система от гипотермии. Она является важнейшим регулятором температуры у детей в период новорожденности, когда мышцы и, соответственно, сократительный термогенез еще недостаточно развиты [48]. У животных также подтверждена отчетливая роль бурой
ЖТ в регуляции температуры тела и энергобаланса. Нокаутирование UCP-1 у мышей сопровождается нарушением индуцированного едой термогенеза, увеличением массы тела. Трансплантация бурых адипоцитов повышает энергозатраты у мышей-реципиентов и устраняет ожирение [49]. Несмотря на отсутствие стандартизированного протокола (температурный режим, питание, выборка без учета сведений о сопутствующей патологии), целый ряд тщательно контролируемых исследований продемонстрировал весомый вклад бурой ЖТ в энергобаланс у взрослого человека при воздействии холодом. Например, по данным V. Ouelett и соавт. (2012), активация бурой ЖТ холодом у молодых людей способна увеличить энергозатраты за счет термогенеза на 80% (нельзя исключить, что столь высокие показатели энергозатрат в большей мере были обусловлены мышечной дрожью, т.е. сократительным термогенезом). Согласно другим расчетам, роль бурой ЖТ в энергобалансе у взрослых людей гораздо более скромная, энергозатраты составляют лишь 7% при массе бурой ЖТ 100 г и 6,3% при массе белой ЖТ 15 кг [51]. Согласно исследованию О. Muzik и соавт. (2012), вклад бурой ЖТ в ежедневные энергозатраты не превышает 15–25 ккал. Это означает, что пациенту с ожирением потребуется 15 лет для снижения массы тела на 20 кг при условии постоянной активности бурого жира. В данной работе существенным ограничением мог быть крайне короткий период стимуляции бурой ЖТ, составивший 30 мин. В исследовании M. Chondronikola и соавт. (2014) с использованием длительного, 5-часового протокола установлено, что у здорового человека 50–100 мл бурой ЖТ увеличивает энергозатраты на 150–300 ккал в сутки. Таким образом, в настоящее время сведения о роли бурой ЖТ в поддержании энергобаланса во взрослой популяции достаточно противоречивы. Тем не менее, следует учесть, что ожирение является результатом длительного положительного энергобаланса. Постоянное превышение должного калоража лишь на 25 ккал в сутки приводит в конечном итоге к увеличению массы тела на 10 кг в течение 10 лет. Соответственно, даже умеренная эпизодическая активность бурой ЖТ может оказывать значимый кумулятивный эффект на энергобаланс и массу тела [51].
Экспериментальные данные у животных убедительно демонстрируют роль термогенных адипоцитов в регуляции углеводного и липидного обменов. Под влиянием низких температур у мышей с ожирением повышается толерантность к глюкозе, бурая ЖТ обеспечивает до 75% общего клиренса глюкозы и до 50% клиренса ТГ в кровяном русле. Трансплантация термогенных адипоцитов улучшает инсулинстимулированный захват глюкозы в бурой и белой ЖТ, а также в миокарде. Уменьшение инсулинорезистентности достигается и благодаря способности термогенных адипоцитов уменьшать фиброз внеклеточного матрикса в белой ЖТ [39]. Блокада браунинга сопровождается развитием тканеспецифичной инсулинорезистентности на уровне печени и белой ЖТ [37]. Исследования у человека также свидетельствуют, что высокая активность термогенных адипоцитов ассоциирована с улучшением контроля гликемии и липидного профиля независимо от возраста, пола и массы тела. Согласно расчетам, 70 мл активированной бурой ЖТ способны утилизировать из сосудистого русла до 20–30 г глюкозы в течение суток. Краткосрочная холодовая акклиматизация повышает чувствительность к инсулину на 43% у больных с СД2 [49]. Важно, что положительное влияние на метаболизм глюкозы у человека прослеживается не только при воздействии холодом, но и в условиях термонейтральности [53].
Бурые и бежевые адипоциты секретируют множество биологически активных веществ (см. рис. 2). По аналогии с адипокинами, вырабатывающимися в белой ЖТ, эти вещества получили название батокины (brown adipose tissue, BAT, — batokines). Ряд батокинов аутокринно либо паракринно влияет на термогенную функцию, активируя либо ингибируя ее. Так, батокин эпендим-связанный протеин-1 (ependymin-related protein 1, EDR1) относится к числу важнейших факторов дифференциации термогенных адипоцитов. Гомолог 2 протеина Slit (Slit homolog protein 2, SLIT2), продуцируемый бурой ЖТ, способствует ее активации c последующим усилением клиренса глюкозы. Сосудистый эндотелиальный фактор роста А (vascular endothelial growth factor А, VEGFА) обеспечивает ангиогенез, а также перфузию, необходимую для доступа термогенных субстратов и рассеивания тепла. Костный морфогенетический протеин BMP8b играет важную роль как в развитии местного сосудистого русла, так и роста нервных волокон [31]. К числу батокинов, повышающих термогенную активность, относятся жирные кислоты, аденозин, оксид азота. Секретируемые эндоканнабиноиды угнетают термогенез. Бурые и бежевые адипоциты секретируют также эндокринные факторы, тем самым оказывая регуляторный контроль над органами и тканями, вовлеченными в метаболический гомеостаз. Например, нейрегулин-4 (neuregulin-4, NRG4) индуцирует рост симпатических аксонов и ангиогенез, а также подавляет в печени липогенез de novo, тем самым снижая инсулинорезистентность и оказывая протективное влияние на развитие жирового стеатоза. Фактор роста фибробластов 21 (fibroblast growth factor 21, FGF21) продуцируется печенью (основной источник), мышечной тканью, поджелудочной железой, белыми и бурыми адипоцитами. FGF21 принимает активное участие в экспрессии термогенных генов, а также в регуляции метаболизма липидов, желчных кислот и глюкозы. Интерлейкин-6 — цитокин, вырабатываемый скелетными мышцами, Т-хелперами, белыми жировыми клетками, а также активированными термогенными адипоцитами. Трансплантация бурой ЖТ у мышей с ожирением, индуцированным приемом высококалорийной пищи, сопровождается устранением гипергликемии, повышением чувствительности к инсулину, снижением массы тела, возрастанием уровня FGF21. Улучшения метаболических показателей не наблюдается при пересадке бурой ЖТ от мышей, нокаутированных по ИЛ-6. В неактивном состоянии бурые адипоциты вырабатывают большое количество миостатина — ключевого фактора мышечного роста, что снижает функциональные возможности скелетной мускулатуры. При активации бурой жировой ткани секреция миостатина, напротив, уменьшается, что сопровождается усилением развития мышечных волокон [31][54]. Обсуждается роль бурой ЖТ в регуляции аппетита. FGF21, помимо активации браунинга и благоприятного влияния на углеводный и жировой обмен, снижает удовольствие от приема особо калорийной, сладкой пищи. Секретин, вырабатываемый в желудке в ответ на прием пищи, поступает в бурые адипоциты из сосудистого русла. Секретин индуцирует прандиальный термогенез и усиливает чувство насыщения на уровне ЦНС через афферентные нервные волокна (рис. 3) [31].

Рисунок 2. Липиды грудного молока алкилглицерины (АКГ) индуцируют браунинг белых адипоцитов у младенцев: а) АКГ грудного молока в макрофагах ребенка метаболизируются в тромбоцит-активирующий фактор (ТАФ); б) активация рецепторов ТАФ (ТАФр) индуцирует выработку интерлейкина-6 (ИЛ-6); в) ИЛ-6 активирует JAK/STAT-сигнальные пути в белых адипоцитах и индуцирует их браунинг; г) влияние АКГ на белую жировую ткань отмечается лишь в раннем детском возрасте, у взрослых людей АКГ-сигналы инактивируются (адаптировано из работы H. Yo и соавт., 2019) [47].
Сокращения: Ucp-1 — uncouple protein-1; Cidea — cell death-inducing DFFA-like effector a); Tmem26 — transmembrane protein 26; Dio2 — iodothyronine deiodinase 2; Ppargc1 — Peroxisome proliferator-activated receptor-g coactivator 1α; JAK/STAT — Janus kinase/signal transducers and activators of transcription.

Рисунок 3. Аутокринные, паракринные и эндокринные эффекты батокинов (адаптировано из работы C. Scheele и соавт., 2020) [31].
Сокращения: EDR1 — ependymin-related protein 1; SLIT-2 — Slit homolog protein 2; IL-6 — интерлейкин-6; FGF21 — fibroblast growth factor 21; NRG4 — neuregulin-4; VEGFА — vascular endothelial growth factor А; BMP8b — bone morphogenetic protein 8b.
По данным сравнительного протеомного анализа белых и бурых адипоцитов человека, секретом бурой ЖТ содержит свыше 100 специфических протеинов, продуцируемых исключительно термогенными адипоцитами [55]. В целом биологические функции термогенных адипоцитов играют важнейшую роль в поддержании метаболического здоровья. T. Becher и соавт. (2021) провели ретроспективную оценку данных 18F-ФДГ ПЭТ/КТ у 52 487 человек, исследования проводились без предварительной активации адипоцитов. У людей с подтвержденным наличием бурой ЖТ констатирована более редкая распространенность сердечно-сосудистых заболеваний (ИБС, артериальной гипертензии, цереброваскулярной патологии, сердечной недостаточности), а также СД2 и дислипидемии. Положительный эффект присутствия бурой ЖТ более отчетливо прослеживался у пациентов с избыточной массой тела и ожирением [56].
Влияние ожирения
Количество термогенных адипоцитов и их активность у больных ожирением снижены, что обусловлено нарушением клеточной пролиферации и дифференциации преадипоцитов, активацией их апоптоза. Предположительно, в основе этих изменений лежат как минимум 4 ключевых механизма: 1) развитие резистентности к катехоламинам, которое характеризуется снижением синтеза норадреналина и β-адренергических рецепторов, а также нарушением проведения внутриклеточных сигналов, задействованных в опосредованной ПКА пролиферации клеток; 2) ожирение приводит к инфильтрации как белой, так и бурой ЖТ М1 макрофагами, участвующими в клиренсе норадреналина и синтезе провоспалительных цитокинов. Транскрипционный фактор NF-κB (Nuclear factor kappa B) подавляет ПКА-опосредованную пролиферацию клеток и их дифференциацию путем блокады экспрессии генов PPARγ и C/EBP (ССAAT-enhancer-binding proteins). Повышение содержания провоспалительного цитокина ФНО-α служит триггером клеточного апоптоза; 3) стресс эндоплазматического ретикулума при выраженном ожирении приводит к гиперактивации системы ответа на мисфолдинг белков UPR (unfolded protein response), что также способствует апоптозу клеток; 4) при ожирении нарушается биогенез митохондрий с последующим накоплением активных форм кислорода, их чрезмерная концентрация приводит к оксидативному стрессу и апоптозу преадипоцитов [26].
Терапевтический потенциал
Термогенные адипоциты играют важнейшую роль в регуляции энергобаланса, углеводного и жирового обмена. В связи с этим их активация представляется чрезвычайно перспективным методом лечения ожирения и СД2. С этой целью за последние годы было изучено множество фармакологических препаратов (селективные β3-адренергические агонисты, тиазолидиндионы, агонисты тиреоидных и глюкокортикоидных рецепторов, экстракты нутриентов и др.), однако реальный успех в клинических исследованиях не был достигнут либо в связи с недостаточным эффектом на метаболизм, либо в связи с нежелательными явлениями [57]. В настоящее время разрабатываются принципиально новые подходы к активации бурых и бежевых адипоцитов. Изучаются сигнальные пути альтернативных, не связанных с UCP-1 механизмов термогенеза. Определяется возможность генетической терапии, позволяющей проводить модификацию адипогенеза бурых адипоцитов. Проводится оценка эффективности применения аналогов батокинов. Разрабатываются системы таргетной доставки активаторов термогенных адипоцитов — функциональные наночастицы и липидные нанотранспортеры. Для успешной разработки эффективных методов лечения необходимы новые методики визуализации и стандартизированные протоколы исследований, позволяющие более точно определять количество, структуру и функции бурой ЖТ [58].
КОСТНО-МОЗГОВАЯ (ЖЕЛТАЯ) ЖИРОВАЯ ТКАНЬ
Костный мозг содержит гемопоэтические и мезенхимальные стволовые клетки, а также их прогениторные клетки, находящиеся на разных стадиях дифференциации и коммитирования. Условно выделяют два вида костного мозга: активно участвующий в гемопоэзе красный мозг и насыщенный адипоцитами желтый мозг [59]. О наличии желтого жира в костях скелета было известно свыше 150 лет назад, первые представления появились в связи с расследованиями случаев отравления мышьяком. Многие годы адипоцитам костного мозга (КМАд) отводилась роль инертных филлеров, заполняющих костные полости при низком содержании костной массы либо нарушении гемопоэза. Учитывая строго изолированную локализацию и мощную иммунную защиту, изучение этого вида адипоцитов сопряжено с объективными трудностями. Кроме того, свойства КМАд во многом определяются их конкретным расположением (позвоночник либо бедренная кость, дистальные либо проксимальные отделы трубчатых костей) [60]. Сведения о взаимосвязи желтой ЖТ с остеопорозом, старением, ожирением, СД2, нервной анорексией, онкологическими заболеваниями и рядом других состояний и заболеваний накопились к началу 70-х годов прошлого столетия. С этого времени в литературных источниках начал использоваться термин «костномозговая жировая ткань» (КМЖТ). На сегодняшний день данный термин является основным для определения функционально интегрированной ткани, сформированной КМАд и их предшественниками [61]. Механизмы адипогенеза и физиологическая значимость КМЖТ стали уточняться лишь в последнее десятилетие. Исследования показали, что КМЖТ играет важную роль в регуляции как локальных процессов — гемопоэза и костного ремоделирования, так и общего гомеостаза [62].
Структура
КМЖТ включает гетерогенную популяцию адипоцитов и их предшественников. Морфологически адипоциты КМЖТ идентичны адипоцитам белой жировой ткани. КМАд представляют собой унилокулярные клетки, желтая окраска обусловлена большим количеством каротиноидов в липидных каплях. КМЖТ состоит из двух подтипов — конститутивного и регулируемого, отличающихся по локализации, составу липидов и генной экспрессии. Регулируемая КМЖТ (рКМЖТ), формирующаяся вскоре после постнатального периода развития, располагается преимущественно в проксимальных отделах скелета в виде небольших вкраплений в зоны активного гемопоэза (красный мозг). По определению, рКМЖТ реагирует на множество факторов окружающей среды, количество и объем адипоцитов уменьшаются либо возрастают в ответ на изменения содержания нутриентов, гормонов, физическую нагрузку и др. Липиды адипоцитов рКМЖТ содержат насыщенные жирные кислоты. Конститутивная КМЖТ (кКМЖТ), появляющаяся на более ранней постнатальной стадии, локализована в дистальных регионах скелета, данный подтип слабо подвержен воздействию окружающих стимулов, в состав липидов входят ненасыщенные жирные кислоты. Клеточный состав дистальных отделов более однородный и представлен преимущественно адипоцитами (желтый мозг) [60][63].
По сравнению с подкожными адипоцитами КМАд характеризуются незначительной липолитической активностью при адренергической стимуляции. Резистентность к β-адренергическим сигналам более отчетлива в дистальных регионах скелета, где располагается кКМЖТ. Эта особенность метаболизма липидов объясняет отсутствие значимого уменьшения количества КМЖТ в ответ на снижение калоража. Кроме того, по сравнению с белыми адипоцитами, желтые адипоциты более активно поглощают глюкозу, оставаясь при этом резистентными к ее инсулинстимулированному захвату [64]. В ряде отделов скелета в небольшом количестве могут присутствовать мультилокулярные адипоциты, не обладающие термогенными свойствами [60][63].
Локализация
КМЖТ располагается в нише костного мозга, которая содержит клетки гемопоэтического и мезенхимного происхождения, находящиеся на разной стадии развития. Гемопоэтические клетки преобладают, они включают эритроциты, нейтрофилы, лейкоциты, тромбоциты и гемопоэтические стволовые клетки (ГСК). ГСК являются мультипотентными клетками, дающими начало миелоидной, лимфоидной и эритроидной линиям. К мезенхимным элементам относятся мезенхимные стволовые клетки (МСК), остеобласты, стромальные фибробласты и адипоциты [7][8]. Наибольшее количество КМЖТ определяется в длинных трубчатых костях; в меньшем количестве она присутствует в позвоночнике, грудине, ребрах, костях таза. В зависимости от объема периферических депо на долю КМЖТ может приходиться от 1 до 30% от всей массы жировой ткани здорового взрослого человека. По данным ПЭТ/КТ, объем КМЖТ в среднем составляет 1142±410 см3, масса — 1,35 кг (от 0,5 до 3 кг) [63].
Развитие, адипогенез
Внутриутробно и у новорожденных костный мозг практически полностью представлен гемопоэтической тканью, характерная красная окраска обусловлена гемоглобином. Постепенное накопление КМЖТ начинается у новорожденных с дистальных фаланг, продолжается в аппендикулярных отделах скелета (от диафизов к дистальным и проксимальным зонам длинных костей) и завершается в его осевых отделах. Уже к 25 годам у человека 70% костного мозга состоит из КМЖТ, по мере старения организма ее количество продолжает возрастать [67]. КМАд берут начало от мозговых скелетных стволовых клеток (МССК), которые также являются предшественниками остеобластов и хондроцитов. Фенотип ранних прогениторов адипоцитов неизвестен; предположительно, это клетки, характеризующиеся экспрессией остерикса (osterix) — фактора транскрипции остеобластогенеза, нестина (nestin) — маркера нейрональных прогениторов, а также рецепторов лептина [68]. С помощью метода scRNA-sq были открыты специфические предшественники костномозговых адипоцитов, получившие название MALPs (marrow adipogenic lineage precursors). Данные клетки не присутствуют в других жировых депо. MALPs формируются на поздних этапах дифференциации и экспрессируют характерные для адипоцитов маркеры, но не содержат липидных капель [10]. Дифференциация МССК в остеобласты и адипоциты регулируется специфическими факторами транскрипции. Детерминирование остеобластной линии на ранней стадии обеспечивают RUNX2 (Runt-related transcription factor 2), остерикс; терминальная дифференцировка находится под контролем коллагена 1 типа, лиганда рецептора активатора ядерного фактора каппа бета RANCL (receptor activator of nuclear factor kappa-B ligand) и остеокальцина. За адипогенную дифференцировку на ранних этапах ответственны PPARγ, CREB, члены семейства C/EBP; терминальная дифференцировка происходит с участием PPARγ, связывающего жирные кислоты протеина-4 (FABP4), перилипина 2 (Plin2), синтазы жирных кислот [60]. Адипогенная либо остеогенная направленность дифференциации МССК контролируется также гормонами, в том числе лептином, эстрогенами, грелином, паратгормоном, гормоном роста. Изменение варианта дифференцировки может происходить под влиянием множества эндогенных и экзогенных факторов, включая нутриенты, физическую нагрузку, медикаменты, заболевания и др. [11]. Зрелые КМАд экспрессируют поздние адипогенные гены AdipoQ, GLUT4, FABP4, LPL, PLIN1, ZFP423. У мышей линии С57BL/6 из костного мозга голеней выделена группа адипоцитов, экспрессирующая гены как белой, так и бурой жировой ткани [4]. Тем не менее данный подтип КМАд не экспрессирует важнейший маркер термогенных адипоцитов UCP-1 как во время дифференциации, так и при адренергической стимуляции; возможности терморегуляции низкие [70].
Основные функции
Ниша костного мозга — анатомическая и функциональная структура, которая интегрирует эндокринные, аутокринные и паракринные сигналы для обеспечения общего гомеостаза и является уникальным домом для множества стволовых клеток. Доступность энергетических субстратов является важнейшим предиктором клеточной пролиферации. Клетки костного мозга тесно взаимодействуют друг с другом, например, остеобласты играют ключевую роль в поддержании гемопоэтической ниши [7]. В течение долгого времени предполагалось, что КМАД является исключительно негативным регулятором остеосинтеза и гемопоэза. Увеличение объема КМЖТ зачастую ассоциировано со снижением минеральной плотности костной ткани и повышением риска переломов у людей пожилого возраста [71]. У животных при ожирении и старении повышение содержания костномозговой жировой ткани сопровождается нарушением функции ГСК и МСК [14]. КМАд и их прогениторы считаются важнейшими медиаторами прогрессии и метастазирования злокачественных новообразований костей и гемобластозов [72]. Концепция метаболической конкуренции недавно была предложена для объяснения механизмов роста злокачественных опухолей. С учетом гиперметаболических свойств, злокачественные клетки в борьбе за метаболические субстраты побеждают другие клетки, располагающиеся в микроокружении опухоли. В конечном итоге это приводит к истощению энергетических резервов регуляторных Т-клеток. Примером может служить множественная миелома, при которой инфильтрация ниши опухолью сопровождается активной утилизацией липидов костномозговых адипоцитов. Более того, клетки миеломы приобретают фенотип адипоцитов, данное преобразование получило название «адипомимикрия». Лишенные необходимых энергетических субстратов остеобласты не могут в должной мере обеспечивать костеобразование, что наблюдается у больных с данным заболеванием [74].
Вполне логично, что в условиях жестко фиксированного пространства костной полости экспансия КМЖТ оставляет меньше места для других клеточных линий, и наоборот. Тем не менее исследования последних лет показали, что взаимоотношения между КМАд и соседними клетками гораздо более сложные и, конечно, не ограничиваются конкурентной борьбой за свободное пространство [59]. Прежде всего, костномозговые адипоциты являются поставщиками энергии для процессов гемопоэза и костного ремоделирования в физиологических условиях, о чем свидетельствует наличие большого запаса ТГ в липидных каплях. Метаболизм липидов в костномозговых адипоцитах изучен недостаточно в связи со сложностями их изоляции и наблюдения in vitro [74]. В работе С. Attane и соавт. (2020) было показано, что КМАд не способны вырабатывать СЖК при адренергической стимуляции, что обусловлено низким содержанием моноацилглицеринлипазы. Эта особенность объясняет отсутствие катаболической реакции КМЖТ в ответ на депривацию нутриентов и предопределяет высокое содержание моноацилглицерина и холестерина в липидных каплях адипоцитов. Тем не менее данные световой микроскопии подтверждают продукцию СЖК костномозговыми адипоцитами и их доставку к трем ключевым зонам: эндотелию, гемопоэтическим и костным клеткам. Учитывая слабую реакцию на адренергические стимулы, липолиз в КМАд может быть индуцирован альтернативным способом. Таким альтернативным активатором липолиза может являться, в частности, паратгормон, рецепторы к которому в большом количестве присутствуют на КМАд. Назначение терипаратида пациентам с остеопорозом сопровождается не только увеличением костной массы, но и снижением содержания общего холестерина, ТГ, а также массы тела. По экспериментальным данным, эти системные эффекты обусловлены прямым влиянием паратгормона на процессы липолиза и утилизации жирных кислот как в периферических жировых депо, так и в КМЖТ [74].
Помимо запасания липидов, КМЖТ осуществляет секрецию гормонов, липидных метаболитов, цитокинов и других биологически активных веществ. Важнейшими адипокинами, вырабатываемыми КМЖТ, являются лептин и адипонектин. К числу других паракринных и эндокринных факторов относятся RANKL, фактор стволовых клеток (ФСК), дипептидилпептидаза-4, интерлейкины ИЛ-3, ИЛ-6, ИЛ-8, цитокин ФНО-α, хемокин (С-Х-С мотив) лиганда 12 (СХСL12) и др. [62]. По данным C. Attane и соавт. (2020), протеомы и секретомы КМЖТ и белой ЖТ практически сопоставимы. Адипокины, вырабатываемые КМАд, оказывают отчетливое влияние на гемопоэз и костное ремоделирование. Кости скелета имеют хорошее кровоснабжение, на его долю приходится до 10% сердечного выброса. Через эндостальные артериолы адипокины КМАд поступают в системный кровоток [59].
Снижение массы тела на фоне ограничения калоража сопровождается повышением уровня адипонектина в крови. Основным источником адипонектина в этот период является КМЖТ. Повышая чувствительность тканей к инсулину, адипонектин влияет на общий гомеостаз организма [76]. На уровне костного мозга адипонектин подавляет дифференциацию адипоцитов и усиливает дифференциацию остеобластов, улучшает выживаемость клеток крови у животных после лучевого воздействия. Лептин регулирует костный метаболизм как минимум на трех уровнях: 1) снижает костеобразование путем активации JAK/STAT сигналов в МСК; 2) усиливает костную резорбцию, повышая симпатическую активность на уровне ствола мозга; 3) уменьшает костную резорбцию путем активации нейронов дугообразных ядер гипоталамуса, вырабатывающих кокаин-амфетамин-регулирующий транскрипт, что приводит к снижению содержания RANKL [77]. КМАд являются важнейшим источником хемокина СХСL12, который участвует в хемотаксисе, хоуминге и выживании ГСК. Вырабатываемый КМАд ФСК индуцирует дифференцировку предшественников лимфоцитов и эритроцитов, кроме того, он обеспечивает регенерацию ГСК и восстановление гемопоэза после лучевой терапии [66, 78]. У трансгенных мышей потеря периферической ЖТ, индуцированная дифтерийным токсином, не сказывается на остеогенезе, в то время как абляция КМЖТ сопровождается значимым увеличением костной массы, активацией рецепторов костного морфогенетического протеина и эпидермального фактора роста [79]. По данным L. Zhong и соавт. (2021), важнейший вклад в регуляцию костного ремоделирования и гемопоэза вносят предшественники костномозговых адипоцитов MALPs. Данные клетки в большом количестве секретируют RANKL и гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМКФ), играющие критическую роль в формировании остеокластов. У экспериментальных мышей, характеризующихся дефицитом RANCL в указанных клетках-предшественниках, наблюдалось увеличение трабекулярной костной массы на 60–100%, снижение количества остеокластов. Авторы пришли к выводу, что именно MALPs являются ключевыми клетками, контролирующими костное ремоделирование как у здорового человека, так и при патологических состояниях. MALPs также подавляют остеогенез, их абляция приводит к снижению содержания в костном мозге антагонистов костных морфогенетических протеинов Grem1 (gremlin 1), Chrdl1 (Chordin Like 1). Кроме того, в объеме, превышающем секреторные возможности любых других мезенхимальных популяций, MALPs вырабатывают важнейшие факторы, регулирующие гемопоэз и ангиогенез, включая СХСL12, ФСК, адипонектин, VEGFА, ангиопоэтин-1 и др. (рис. 4) [80].
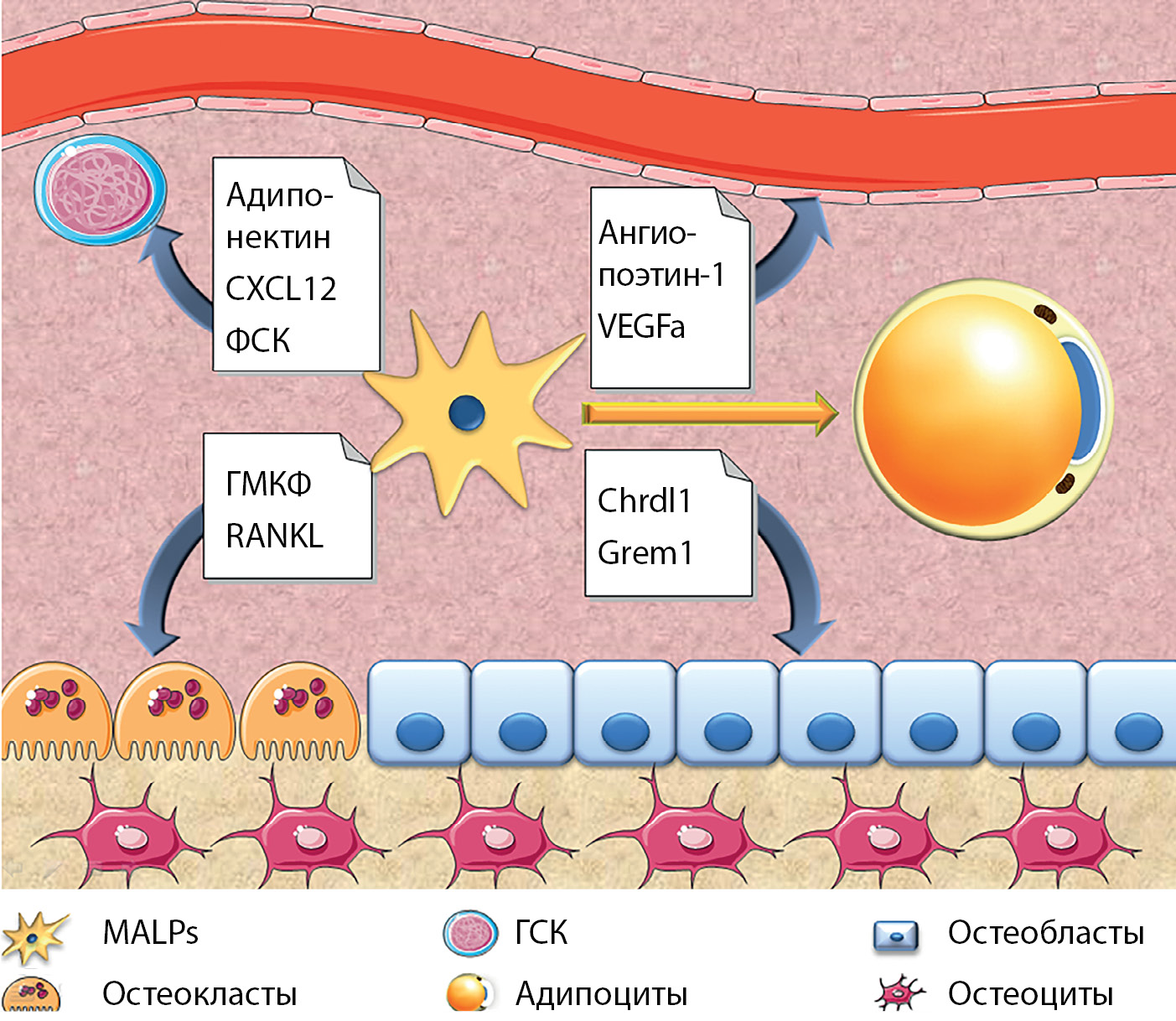
Рисунок 4. Регуляторное влияние предшественников адипоцитов MALPs на клетки костного мозга (адаптировано из работы L. Chong и соавт., 2021) [80].
Сокращения: MALPs — marrow adipogenic lineage precursors; ГСК — гемопоэтические стволовые клетки; ФСК — фактор стволовых клеток; ГМКФ — гранулоцитарно-макрофагальный колониестимулирующий фактор; RANKL — receptor activator of nuclear factor kappa-B ligand, Grem1 — Gremlin 1, Chrdl1 — Chordin Like 1; СХСL12 — хемокин (С-Х-С мотив) лиганда 12.
Влияние ожирения
Результаты экспериментальных и клинических исследований, посвященных влиянию ожирения на КМЖТ, достаточно противоречивы. У животных с ожирением увеличение объема КМЖТ отмечается в подавляющем большинстве работ. Например, у мышей линии С57BL/6, склонных к развитию ожирения и диабета, высококалорийный рацион индуцирует экспансию КМЖТ; переход на стандартный корм сопровождается восстановлением ее обычного содержания. В отличие от подкожной жировой ткани, экспансия КМЖТ на фоне избыточного питания не сопровождается повышением экспрессии провоспалительных генов; инфильтрации макрофагами, развития фиброза и инсулинорезистентности не наблюдается [60][81]. Учитывая инвазивность процедуры костной биопсии, изучение КМЖТ у человека в основном проводится с помощью МРТ, КТ либо ПЭТ/КТ [71]. Оценка взаимосвязи между ИМТ и состоянием КМЖТ у людей началась сравнительно недавно. В некоторых исследованиях указанной взаимосвязи не выявлено [31]. В работе M. A. Bredella и соавт. (2011) отмечена положительная ассоциация между количеством висцерального жира и КМЖТ. У больных СД2 не всегда прослеживается зависимость между состоянием КМЖТ и массой тела, тем не менее, установлена прямая связь с показателями HbA1c. Сахарный диабет приводит к ремоделированию костного мозга — обеднению сети микрососудов, сенсорных нервов, апоптозу гемопоэтических прогениторов, накоплению КМЖТ [83].
У животных и человека резкое ограничение суточного калоража сопровождается парадоксальной гипертрофией и гиперплазией КМАд. У пациенток с нервной анорексией КМЖТ может составлять до 30% от общего объема жировых депо. Экспансия КМЖТ в условиях резкого дефицита питания может быть обусловлена повышением содержания кортизола, грелина, либо гиполептинемией. Гипотетически КМЖТ является стратегическим резервом энергии, обеспечивающим важнейшие функции костного мозга в условиях голода [84]. Экспансия КМЖТ отмечается также при остеопорозе, дефиците эстрогенов, гиперкортицизме, алкогольной зависимости, назначении тиазолидиндионов, глюкокортикоидов, химиотерапии, лучевой терапии. В большинстве случаев это ассоциировано со снижением минеральной плотности кости, умеренными либо выраженными нарушениями гемопоэза. Уменьшение объема КМЖТ наблюдается при физической нагрузке, воздействии низких температур, метформина, паратгормона [85].
Терапевтический потенциал
Многие фармакологические соединения подавляют экспансию КМЖТ, к ним относятся ресвератрол, комбинация витамина D c кверцетином, ранелат стронция, различные оксистеролы и др. Тем не менее дефицит фундаментальных данных о процессах адипогенеза, метаболизме липидов, реальных взаимоотношениях клеток костномозговой ниши не позволяет в настоящее время судить о целесообразности прямого воздействия на адипогенную дифференцировку КМАд. Дальнейшие исследования свойств и функций КМЖТ будут способствовать разработке инновационных методов терапии злокачественных новообразований костей и гемобластозов, остеопороза и других метаболических заболеваний [62][66][83].
ЖИРОВАЯ ТКАНЬ МОЛОЧНОЙ ЖЕЛЕЗЫ И РОЗОВЫЕ АДИПОЦИТЫ
Молочная железа (МЖ) состоит преимущественно из эпителиальных клеток и окружающей ее стромы. Вне лактации белая ЖТ стромы составляет основную массу железы [86]. Дедифференциация, трансдифференциация и репрограммирование — важнейшие звенья тканевого ремоделирования, которое отмечается в МЖ во время лактационного цикла. Основные стадии лактационного цикла включают беременность, лактацию и инволюцию [87]. Розовые адипоциты были идентифицированы в 2004 г. группой итальянских исследователей, возглавляемой S. Cinti [88]. Данные клетки, формирующиеся в ткани МЖ во время беременности и лактации, служат примером уникальной пластичности ЖТ, способной кардинально менять профиль генной экспрессии, свойства и функции в зависимости от метаболических потребностей организма.
Структура
Жировая ткань МЖ в основном представлена белыми адипоцитами, в небольших количествах встречаются бурые и бежевые клетки [86]. Паренхима МЖ имеет структуру альвеолярно-дольчатых комплексов, погруженных в соединительно-тканную строму и окруженных густой сетью миоэпителиальных элементов, кровеносных и лимфатических сосудов, нервных рецепторов. Секреторная ткань каждой железы делится на 15–20 долей, каждая доля имеет свой выводной проток на соске, отделенный от соседних протоков соединительнотканными прослойками и жировой тканью. Тонкостенные протоки альвеол выстланы однослойным плоским эпителием, сходным по строению с железистыми клетками. Снаружи стенку альвеол и выводных протоков окружают миоэпителиальные клетки. Соотношение между железистой, жировой и соединительной тканями в МЖ претерпевает значительные колебания в зависимости от возраста женщины, фазы менструального цикла, стадии лактационного цикла. Молочные железы индивидуально варьируют по величине и массе. У девушек масса каждой железы составляет в среднем 150–250 г, у кормящей матери — 800–900 г, но в ряде случаев может достигать 3–5 кг и более [89]. На долю адипоцитов приходится 56% от количества всех клеток не лактирующей железы и до 35% — в период лактации. Во время беременности количество адипоцитов постепенно уменьшается, что высвобождает пространство для пролиферации эпителиальных клеток протоков и формирования альвеолярных структур. После завершения лактации начинается фаза инволюции, характеризующаяся апоптозом эпителиальных клеток; их место вновь занимают быстро регенерирующие адипоциты [90].
Развитие, адипогенез
В отличие от других органов, молочные железы, закладывающиеся на 6 неделе внутриутробного периода из элементов эктодермиса, завершают свое развитие лишь к пубертату и достигают зрелого функционального состояния во время беременности. Адипоциты МЖ берут начало от периваскулярных мезенхимальных стволовых клеток. Альвеолярный эпителий развивается из взрослых маммарных стволовых клеток (МаСК) [87]. Исследования на трансгенных мышах показали, что в дополнение к МаСК адипоциты МЖ тоже участвуют в формировании альвеолярных клеток путем трансдифференциации. Во время беременности уменьшение количества белых унилокулярных адипоцитов сопровождается появлением мультилокулярных клеток, сходных по морфологии с эпителием (прямая адипоэпителиальная трансдифференциация). Розовая окраска схожих с эпителием адипоцитов отражает особенности цвета молочной железы, насыщенной в этот период кровеносными сосудами. Помимо липидных капель, розовые адипоциты содержат наполненные молоком вакуоли, крупные митохондрии, пероксисомы, гранулярный эндоплазматический ретикулум, цитоплазматические проекции, а также микроворсинки на апикальной поверхности. Розовые адипоциты участвуют в формировании альвеолярного аппарата молочной железы, синтезируют и секретируют компоненты грудного молока, вырабатывают адипокины. Таким образом, гибкая трансформация адипоцитов в эпителиальные клетки необходима для надежного энергетического обеспечения потомства. С прекращением лактации розовые адипоциты приобретают исходный фенотип белых жировых клеток (реверсивная адипоэпителиальная трансдифференциация) [91][92]. Как отмечает S. Cinti (2018), 70% секретирующих молоко эпителиальных клеток образуются путем конверсии адипоцитов, остальные берут начало от МаСК [91]. В работе Q. Wang и соавт. (2018) было определено, что во время лактации адипоциты МЖ дедифференцируются в преадипобласты с последующим редифференцированием в зрелые клетки в период инволюции. В данной работе авторы не обнаружили конверсию адипоцитов в альвеолярные клетки, что, возможно, обусловлено применением другой методики отслеживания клеточных поколений. Тем не менее, в дальнейших исследованиях была продемонстрирована трансдифференциация классических мезенхимальных преадипоцитов, экспрессирующих PDGFRα, в эпителиальные клетки протоков [94]. Кроме того, показана возможность прямой конверсии лобулоальвеолярных эпителиальных клеток в бурые адипоциты [95]. В свою очередь, бурые и бежевые адипоциты МЖ способны трансформироваться в миоэпителиальные клетки [96]. Установлено, что, несмотря на коммитированное состояние, зрелые адипоциты способны сохранять высокий уровень экспрессии генов репрограммирования [92]. Молекулярные механизмы, индуцирующие и контролирующие подобные прямые и обратные клеточные конверсии, в настоящее время не определены. По предварительным данным, в эти кардинальные преобразования генной экспрессии клеток вовлечены гормоны беременности (пролактин, прогестерон, эстрогены), а также паракринные факторы, вырабатываемые железой. Предположительно, весомую роль в процессе конверсии белых адипоцитов в розовые играет остеопонтин (или secreted phosphoprotein 1, Spp1), участвующий в лобуло-альвеолярном развитии и являющийся маркером прогениторных альвеолярных клеток. Экспрессия мРНК Spp1 в жировой ткани МЖ повышается на поздних сроках беременности. Изучается также потенциальный вклад «мастера» регуляции альвеологенеза Elf5 (E74-like factor 5); стабильная эктопическая экспрессия этого транскрипционного фактора выявлена в культуре маммарных адипоцитов. Рассматривается возможный вклад SFRP1 (secreted frizzled related protein 1) в индукцию фазы инволюции. Адипокин SFRP1, вырабатываемый адипоцитами МЖ, участвует в процессах адипогенеза, воспаления и апоптоза. В качестве ключевого фактора трансдифференциации розового адипоцита в белый рассматривается «мастер» регуляции адипогенеза PPARγ (рис. 5) [92, 97].
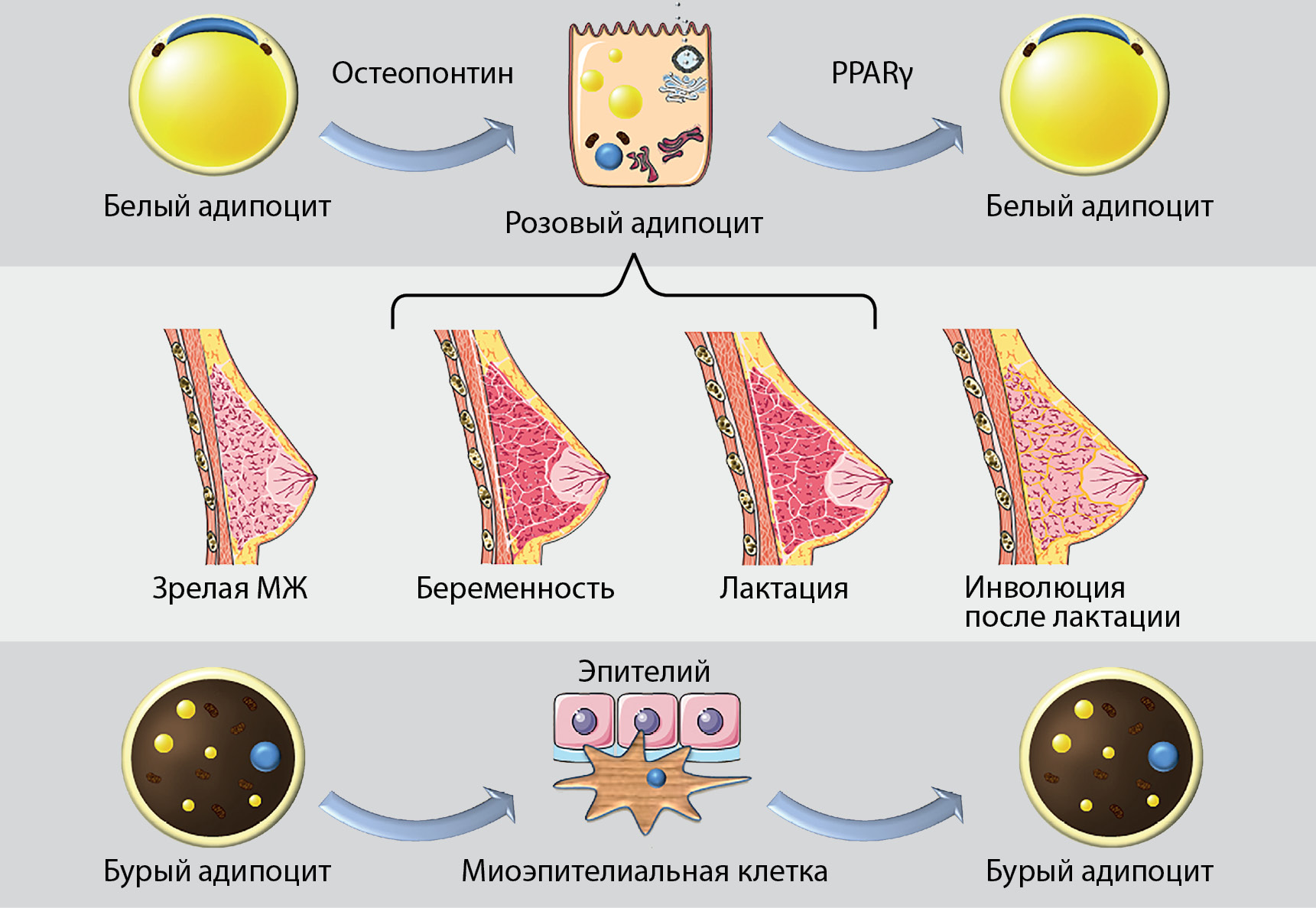
Рисунок 5. Трансдифференциация адипоцитов молочной железы в лактационном цикле (адаптировано из работы C. Kothari и соавт., 2020) [97].
Процесс адипо-эпителиальной трансдифференциации во время лактационного цикла подтвержден и у человека. В среде культивации, содержащей гормоны беременности и регулятор альвеологенеза остеопонтин, адипоциты, дифференцировавшиеся из мультипотентных стромальных стволовых клеток человека, через сутки теряют характерную экспрессию Plin1 и AdipoQ и начинают экспрессировать маркеры альвеологенеза и лактогенеза Elf5, ß-casein, Wap (whey acidic protein). При изучении образцов ткани лактирующей молочной железы, полученных путем биопсии у кормящих женщин, идентифицированы розовые адипоциты, экспрессирующие ген ELF5 [98].
Основные функции
Жировая ткань осуществляет опорную, механическую функцию для МЖ. Помимо этого, адипоциты МЖ играют важнейшую роль в ее развитии в препубертате, пубертатном периоде и взрослом возрасте. Потеря жировой ткани в МЖ у мышей линии A-ZIP приводит к формированию лишь рудиментарных протоков и снижению фертильности [99]. Как и другие жировые депо, адипоциты МЖ синтезируют и секретируют гормоны, ферменты, цитокины, хемокины, факторы роста. Пролактин, рецепторы к которому присутствуют как на адипоцитах, так и на эпителиальных клетках, оказывает многофакторное влияние на процессы маммогенеза, лактогенеза, лактопоэза [89][99]. Внегипофизарный пролактин вырабатывается жировой тканью, в том числе, адипоцитами МЖ [100]. Лептин локально продуцируется белыми и розовыми адипоцитами МЖ. В целом в ходе протеомного анализа идентифицировано свыше 350 адипокинов, вырабатываемых жировой тканью МЖ. Они оказывают как дистантное, эндокринное действие, так паракринные эффекты, направленные на регуляцию развития железы и ее ремоделирование в процессе лактационного цикла. Адипоциты являются основным источником липидов грудного молока. Наряду с другими компонентами, адипокины и липиды, присутствующие в грудном молоке, оказывают регуляторное действие на здоровье потомства [87].
Влияние ожирения
Ожирение у экспериментальных животных сопровождается нарушением маммогенеза и лактогенеза. Ожирение у женщин нередко ассоциировано с укорочением периода лактации, фиброзно-кистозной мастопатией. Ожирение приводит к гипертрофии адипоцитов МЖ, гипоксии, фиброзу, изменению профиля секреции адипокинов [87]. S. Cinti и соавт. определили, что в висцеральной жировой ткани вокруг погибших вследствие гипоксии адипоцитов формируются короноподобные структуры (КПС), образованные макрофагами-рекрутами. КПС продуцируют множество провоспалительных цитокинов, что способствует инсулинорезистентности [101]. Выявлена прямая зависимость между количеством КПС и выраженностью метаболических нарушений. У тучных животных присутствие КПС и, соответственно, метавоспаление отмечены также и в ткани МЖ [87]. Все эти факторы в сочетании с гиперлептинемией и гиперэстрогенией предопределяют высокий риск рака МЖ при ожирении. Изучается роль процессов трансдифференциации и дедифференциации адипоцитов молочной железы в патогенезе ее злокачественных новообразований [97].
Терапевтический потенциал
Адипоциты МЖ обладают уникальными пластичными свойствами, отличающими их от других жировых депо. Коммитирование и дифференциация клеточных поколений традиционно считались однонаправленными и необратимыми процессами. Реверсивная трансдифференциация белых адипоцитов в эпителиальные альвеолярные клетки, наблюдающаяся во время беременности, открывает новый аспект биологии жировой ткани. Аналогичные радикальные преобразования происходят в термогенных адипоцитах, преобразующихся во время лактации в миоэпителиальные клетки. Эта гибкая трансформация свидетельствует о существовании быстрого, безопасного и/или менее энергозатратного механизма изменения структуры и функции клеток, обеспечивающего оптимальную адаптацию к насущным метаболическим потребностям организма. Идентификация молекулярных путей, вовлеченных в процессы трансдифференциации, дедифференциации и репрограммирования жировой ткани, позволит уточнить патогенез и разработать новые подходы к лечению целого ряда заболеваний, в том числе рака МЖ [87][97].
ЗАКЛЮЧЕНИЕ
Жировая ткань — сложный, гетерогенный эндокринный орган. Каждое анатомическое депо отличается по метаболическому и секреторному профилю и реализует особую физиологическую функцию. Гетерогенность анатомических депо обусловлена отличиями по клеточному составу адипоцитов, включая особенности их происхождения, развития, пролиферативной способности, метаболизму глюкозы и липидов, чувствительности к инсулину, гормональному контролю, термогенным возможностям и др. Дополнительными факторами, предопределяющими гетерогенность жировой ткани, являются генетические особенности, пол, возраст, факторы внешней среды. Уникальной особенностью адипоцитов является их способность к гибкой трансформации — трансдифференциации либо дедифференциации в зависимости от потребностей организма. При положительном энергобалансе бежевые адипоциты трансформируются в белые для увеличения возможностей запасания энергии. Низкая температура способствует конверсии белых адипоцитов в бежевые для усиления ее термогенного потенциала. Во время беременности белые адипоциты молочной железы конвертируются в продуцирующий грудное молоко эпителий. Особенности морфологии адипоцитов формируют своего рода «радугу» клеточного состава этого органа и предопределяют широкий спектр функций [5][102]. Дальнейшее изучение биологии жировой ткани будет способствовать уточнению патогенеза множества метаболических заболеваний и разработке персонифицированного подхода к их лечению.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Автор одобрил финальную версию статьи перед публикацией, выразил согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Дедов И.И., Шестакова М.В., Мельниченко Г.А., и др. Междисциплинарные клинические рекомендации «Лечение ожирения и коморбидных заболеваний» // Ожирение и метаболизм. — 2021. — Т. 18. — №1. — С. 5-99.
2. Berry DC, Stenesen D, Zeve D, Graff JM. The developmental origins of adipose tissue. Development. 2013;140(19):3939-3949. doi: https://doi.org/10.1242/dev.080549
3. Lenz M, Arts ICW, Peeters RLM, et al. Adipose tissue in health and disease through the lens of its building blocks. Sci Rep. 2020;10(1):10433. doi: https://doi.org/10.1038/s41598-020-67177-1
4. Schoettl T, Fischer IP, Ussar S. Heterogeneity of adipose tissue in development and metabolic function. J Exp Biol. 2018;221(S1). doi: https://doi.org/10.1242/jeb.162958
5. Rosen ED, Spiegelman BM. What we talk about when we talk about fat. Cell. 2014;156(1-2):20-44. doi: https://doi.org/10.1016/j.cell.2013.12.012
6. Cinti S. Adipose Organ Development and Remodeling. Compr Physiol. 2018;8(4):1357-1431. doi: https://doi.org/10.1002/cphy.c170042
7. Zinngrebe J, Debatin KM, Fischer-Posovszky P. Adipocytes in hematopoiesis and acute leukemia: friends, enemies, or innocent bystanders? Leukemia. 2020;34(9):2305-2316. doi: https://doi.org/10.1038/s41375-020-0886-x
8. Chait A, Hartigh LJ. Adipose tissue distribution, inflammation and its metabolic consequences, including diabetes and cardiovascular disease. Front Cardiovasc Med. 2020;7:22. doi: https://doi.org/10.3389/fcvm.2020.00022
9. Kahn CR, Wang G, Lee KV. Altered adipose tissue and adipocyte function in the pathogenesis of metabolic syndrome. J Clin Invest. 2019;129(10):3990-4000. doi: https://doi.org/10.1172/JCI129187
10. Соркина Е.Л. Синдромы парциальных и тотальных липодистрофий. В кн. Болезни жировой ткани / Под ред. И.И. Дедова. — М.: ГЭОТАР-Медиа; 2020. — С. 191-210.
11. Luong Q, Huang J, Lee KY. Deciphering White Adipose Tissue Heterogeneity. Biology (Basel). 2019;8(2):23. doi: https://doi.org/10.3390/biology8020023
12. Berry DC, Jiang Y, Graff JM. Emerging roles of adipose progenitor cells in tissue development, homeostasis, expansion and thermogenesis. Trends in Endocrinol Metab. 2016;27(8):574-585. doi: https://doi.org/10.1016/j.tem.2016.05.001
13. Ghaben AL, Scherer PE. Adipogenesis and metabolic health. Nat Rev Mol Cell Biol. 2019;20(4):242-258. doi: https://doi.org/10.1038/s41580-018-0093-z
14. Ambele MA, Dhanraj P, Giles R, Pepper MS. Adipogenesis: A Complex Interplay of Multiple Molecular Determinants and Pathways. Int J Mol Sci. 2020;21(12):4283. doi: https://doi.org/10.3390/ijms21124283
15. Hepler C, Shan B, Zhang Q, et al. Identification of functionally distinct fibro-inflammatory and adipogenic stromal subpopulations in visceral adipose tissue of adult mice. Elife. 2018;7(13):4773. doi: https://doi.org/10.7554/eLife.39636
16. Deutsch A, Feng D, Pessin JE, Shinoda K. The Impact of Single-Cell Genomics on Adipose Tissue Research. Int J Mol Sci. 2020;21(13):4773. doi: https://doi.org/10.3390/ijms21134773
17. Егоров А.Д., Пеньков Д.Н., Ткачук В.А. Молекулярные и клеточные механизмы адипогенеза // Сахарный диабет. — 2015. — Т. 18. — №2. — С. 12-19.
18. Bielczyk-Maczynska E. White Adipocyte Plasticity in Physiology and Disease. Cells. 2019;8(12):1507. doi: https://doi.org/10.3390/cells8121507
19. Walther TC, Farese RV Jr. Lipid droplets and cellular lipid metabolism. Annu Rev Biochem. 2012;81:687-714. doi: https://doi.org/10.1146/annurev-biochem-061009-102430
20. Luo L, Liu M. Adipose tissue in control of metabolism. J Endocrinol. 2016;231(3):R77-R99. doi: https://doi.org/10.1530/JOE-16-0211
21. Eckel J. Adipose Tissue. In: The Cellular Secretome and Organ Crosstalk. Vol 18. Elsevier; 2018:9-63. doi: https://doi.org/10.1016/B978-0-12-809518-8.00002-7
22. Zhang Y, Yu M, Dong J, et al. Identification of Novel Adipokines through Proteomic Profiling of Small Extracellular Vesicles Derived from Adipose Tissue. J Proteome Res. 2020;19(8):3130-3142. doi: https://doi.org/10.1021/acs.jproteome.0c00131
23. Hammarstedt A, Gogg S, Hedjazifar S, et al. Impaired Adipogenesis and Dysfunctional Adipose Tissue in Human Hypertrophic Obesity Physiol Rev. 2018;98(4):1911-1941. doi: https://doi.org/10.1152/physrev.00034.2017
24. Kusminski CM, Bickel PE, Scherer PE. Targeting adipose tissue in the treatment of obesity-associated diabetes. Nat Rev Drug Discov. 2016;15(9):639-660. doi: https://doi.org/10.1038/nrd.2016.75
25. Tsilingiris D, Liatis S, Dalamaga M, Kokkinos A. The Fight Against Obesity Escalates: New Drugs on the Horizon and Metabolic Implications. Curr Obes Rep. 2020;9(2):136-149. doi: https://doi.org/10.1007/s13679-020-00378-x
26. Trayhurn P. Brown adipose tissue — a therapeutic target in obesity? Front Physiol. 2018;9:1672. doi: https://doi.org/10.3389/fphys.2018.01672
27. Титов В.Н., Салтыкова М.М. Структурно и функционально разные пулы жировой ткани: инсулиннезависимые висцеральные клетки, инсулинзависимые подкожные адипоциты и бурые клетки термогенеза // Клиническая лабораторная диагностика. — 2017. — Т. 62. — №3. — С. 132-139.
28. Cypess AM, Lehman S, Williams G, et al. Identification and importance of brown adipose tissue in adult humans. N Engl J Med. 2009;360;1509-1517. doi: https://doi.org/10.1056/NEJMoa0810780
29. Petrovic N, Walden TB, Shabalina IG, et al. Chronic peroxisome proliferator-activated receptor γ (PPARγ) activation of epididymally derived white adipocyte cultures reveals a population of thermogenically competent, UCP1-containing adipocytes molecularly distinct from classic brown adipocytes. J Biol Chem. 2010;285;7153-7164. doi: https://doi.org/10.1074/jbc.M109.053942
30. Pfeifer A, Klingespor M, Herzig S. Brown adipose tissue. Handbook of Experimental Pharmacology, Vol. 251. Springer, Cham; 2019. 424 p. doi: https://doi.org/1007/978-3-030-10513-6
31. Scheele C, Wolfrum C. Brown adipose crosstalk in tissue plasticity and human metabolism. Endocr Rev. 2020;41:53-56. doi: https://doi.org/10.1210/endrev/bnz007
32. Oguri Y, Kajimura S. Cellular heterogeneity in brown adipose tissue. J Clin Invest. 2020;130(1):65-67. doi: https://doi.org/10.1172/JCI133786
33. Ong F, Ahmed B, Oreskovich SM et al. Recent advances in the detection of brown adipose tissue in adult humans: a review. Clin Sci. 2018;132:1039-1054. doi: https://doi.org/10.1042/cs20170276
34. Sacks H, Simonds ME. Anatomical locations of human brown adipose tissue: functional relevance and implications in obesity and type 2 diabetes. Diabetes. 2013;62(60):1783-1790. doi: https://doi.org/10.2337/db12-1430
35. Leihner BP, Huang S, Brychta RJ, et al. Mapping of human adipose tissue in lean and obese young men. PNAS. 2017;114(32):8649-8654. doi: https://doi.org/10.107/pnas.1705287114
36. Chondronikola M, Sidossis LS. The Physiological Significance of Brown Adipose Tissue and the Beiging of White Adipose Tissue in People. In: Adipose Tissue Biology. Vol 22. Cham: Springer International Publishing; 2017:201-227. doi: https://doi.org/10.1007/978-3-319-52031-5_6
37. Maliszewska K, Kretowski A. Brown Adipose Tissue and Its Role in Insulin and Glucose Homeostasis. Int J Mol Sci. 2021;22(4):1530. doi: https://doi.org/10.3390/ijms22041530
38. Ladoux A, Peraldi P, Chignon-Sicard B, Dani C. Distinct Shades of Adipocytes Control the Metabolic Roles of Adipose Tissues: From Their Origins to Their Relevance for Medical Applications. Biomedicines. 2021;9(1):40. doi: https://doi.org/10.3390/biomedicines9010040
39. Cohen P, Kajimura S. The cellular and functional complexity of thermogenic fat. Nat Rev Mol Cell Biol. 2021;22(6):393-409. doi: https://doi.org/10.1038/s41580-021-00350-0
40. Rabiee A. Beige Fat Maintenance; Toward a Sustained Metabolic Health. Front Endocrinol (Lausanne). 2020;11. doi: https://doi.org/10.3389/fendo.2020.00634
41. Ruan H-B. Developmental and functional heterogeneity of thermogenic adipose tissue. J Mol Cell Biol. 2021;12(10):775-784. doi: https://doi.org/10.1093/jmcb/mjaa029
42. Lizcano F, Arroyave F. Control of Adipose Cell Browning and Its Therapeutic Potential. Metabolites. 2020;10(11):471. doi: https://doi.org/10.3390/metabo10110471.
43. Ikeda K, Maretich P, Kajimura S. The common and distinct features of brown and beige adipocytes. Trends Endocrinol Metab. 2018;29(3);191-200. doi: https://doi.org/10.1016/j.tem.2018.01.001.
44. Pollard AE, Carling D. Thermogenic adipocytes: lineage, function and therapeutic potential. Biochem J. 2020;477(11):2071-2093. doi: https://doi.org/10.1042/BCJ20200298.
45. Chondronikola М. The role of brown adipose tissue and the thermogenic adipocytes in glucose metabolism: recent advances and open questions. Curr Opin Clin Nutr Metab Care. 2020;23(4):282-287. doi: https://doi.org/10.1097/MCO.0000000000000662
46. Кокшарова Е.О., Майоров А.Ю., Шестакова М.В., Дедов И.И. Метаболические особенности и терапевтический потенциал бурой и бежевой жировой ткани // Сахарный диабет. — 2014. — Т. 17. — №4. — С. 5-15.
47. Yu H, Dilbaz S, Coßmann J, et al. Breast milk alkylglycerols sustain beige adipocytes through adipose tissue macrophages. J Clin Invest. 2019;129(6):2485-2499. doi: https://doi.org/10.1172/JCI125646
48. Sidoss L, Kajimura S. Brown and beige fat in humans: thermogenic adipocytes that control energy and glucose homeostasis. J Clin Invest. 2015;125:478-486. doi: https://doi.org/10.1172/JCI178362
49. Cheng L, Wang J, Dai H, et al. Brown and beige adipose tissue: a novel therapeutic strategy for obesity and type 2 diabetes mellitus. Adypocyte. 2021;10(1):48-65. doi: https://doi.org/10.1080/21623945.2020.1870060
50. Ouellet V, Labbe SM, Blondin DP, et al. Brown adipose tissue oxidative metabolism contributes to energy expenditure during acute cold exposure in humans. J Clin Invest. 2012;122(2):545. doi: https://doi.org/52.10.1172/JCI60433
51. Porter C, Chondronikola M, Sidossis LS. The therapeutic potential of brown adipocytes in human. Front Endocrinol (Lausanne). 2015;6:156. doi: https://doi.org/10.3389/fendo.2015.00156.
52. Muzik O, Mangner TJ, Leonard WR, et al. 15O PET measurement of blood flow and oxygen consumption in cold-activated human brown fat. J Nucl Med. 2013;54(4):523-531. doi: https://doi.org/10.2967/jnumed.112.111336
53. Chondronikola M, Volpi E, Børsheim E, et al. Brown adipose tissue improves whole body glucose homeostasis and insulin sensitivity in humans. Diabetes. 2014;63(12):4089-4099. doi: https://doi.org/10.2337/db14-0746
54. Gavaldà-Navarro A, Villarroya J, Cereijo R, et al. The endocrine role of brown adipose tissue: An update on actors and actions. Rev Endocr Metab Disord. March 2021. doi: https://doi.org/10.1007/s11154-021-09640-6
55. Deshmukh AS, Peijs L, Beaudry JL, et al. Proteomics-based comparative mapping of the secretomes of human brown and white adipocytes reveals EPDR1 as novel batokine. Cell Metab. 2019;30:1-13. doi: https://doi.org/10.1016/j.cmet.2019.10.001
56. Becher T, Palanisamy S, Kramer DJ, et al. Brown adipose tissue is associated with cardiometabolic health. Nat Med. 2021;27:58-65. doi: https://doi.org/10.1038/s41591-020-1126-7
57. Larson CJ. Translation pharmacology and physiology of brown adipose tissue in human disease and treatment. Handb Exp Pharmacol. 2019;251:381-424. doi: https://doi.org/10.1007/164_2018_184
58. Srivastava S, Richard L. Veech RL. Brown and Brite: The Fat Soldiers in the Anti-obesity Fight. Front Physiol. 2019;10:38. doi: https://doi.org/10.3389/fphys.2019.00038
59. Boroumand P, Klip A. Bone marrow adipose cells – cellular interactions and changes with obesity. J Cell Sci. 2020;133(5). doi: https://doi.org/10.1242/jcs.238394
60. De Paula FGA, Rosen CJ. Marrow adipocytes: origin, structure, and function. Annu Rev Physiol. 2020;82:461-484. doi: https://doi.org/10.1146/annurev-physiol-021119-034513
61. Bravenboer N, Bredella MA, Chauveau C, et al. Standardised Nomenclature, Abbreviations, and Units for the Study of Bone Marrow Adiposity: Report of the Nomenclature Working Group of the International Bone Marrow Adiposity Society. Front Endocrinol (Lausanne). 2020;10:923. doi: https://doi.org/10.3389/fendo.2019.00923
62. Tratwal J, Labella R, Bravenboer N, et al. Reporting Guidelines, Review of Methodological Standards, and Challenges Toward Harmonization in Bone Marrow Adiposity Research. Report of the Methodologies Working Group of the International Bone Marrow Adiposity Society. Front Endocrinol (Lausanne). 2020;11:65. doi: https://doi.org/10.3389/fendo.2020.00065
63. Scheller EL, Cawton WP, Burr AA, et al. Marrow adipose tissue: Trimming the fat. Trends Endocrinol Metab. 2016;27(6):392-403. doi: https://doi.org/10.1016/j.tem.2016.03.016
64. Scheller EL, Khandaker S, Learman BS, et al. Bone marrow adipocytes resist lipolysis and remodeling in response to beta-adrenergic stimulation. Bone. 2019;118:32-41. doi: https://doi.org/10.1016/j.bone.2018.01.016
65. Veldhuis-Vlug AG, Rosen CJ. Mechanisms of marrow adiposity and its implications for skeletal health. Metabolism. 2017;67:106-114. doi: https://doi.org/10.1016/j.metabol.2016.11.013
66. Veldhuis-Vlug AG, Rosen CJ. Clinical implication of bone marrow adiposity. J Intern Med. 2018;283(2):121-139. doi: https://doi.org/10.1111/joim.12718
67. Li Z, Hardij J, Bagchi DP, et al. Development, regulation, metabolism and function of bone marrow adipose tissues. Bone. 2018;110:134-140. doi: https://doi.org/10.1016/j.bone.2018.01.008
68. Zhong L, Yao L, Tower RJ, et al. Single cell transcriptomics identifies a unique adipose lineage cell population that regulates bone marrow environment. eLife. 2020;9:e54695. doi: https://doi.org/10.7554/eLife.54695
69. Bukowska J, Frazier T, Smith S, et al. Bone Marrow Adipocyte Developmental Origin and Biology. Curr Osteoporos Rep. 2018;16(3):312-319. doi: https://doi.org/10.1007/s11914-018-0442-z
70. Craft CS, Robles H, Lorenz ML, et al. Bone marrow adipose tissue does not express UCP1 during development or adrenergic-induced remodeling. Sci Rep. 2019;9(1):17427. doi: https://doi.org/10.1038/s41598-019-54036-x
71. Gόmez MPA, Benavent CA, Simoni P, et al. Fat and bone: The multiperspective analysis of a close relationship. Quant Imaging Med Surg. 2020;10:1614-1635. doi: https://doi.org/10.21037/qims.2020.01.11
72. Ambrosi TH, Scialdone A, Graja A, et al. Adipocyte Accumulation in the Bone Marrow during Obesity and Aging Impairs Stem Cell-Based Hematopoietic and Bone Regeneration. Cell Stem Cell. 2017;20(6):771-784.e6. doi: https://doi.org/10.1016/j.stem.2017.02.009
73. Reagan MR, Fairfield H, Rosen CJ. Bone marrow adipocytes: A link between obesity and bone cancer. Cancers. 2021;13:364. doi: https://doi.org/10.3390/cancers13030364
74. Rendina-Ruedy E, Rosen CJ. Lipids in the bone marrow: An evolving perspective. Cell Metab. 2020;31(2):219-231. doi: https://doi.org/10.1016,/j.cmet.2019.09.015
75. Attane C, Esteve D, Chaoui K, et al. Human Bone Marrow Is Comprised of Adipocytes with Specific Lipid Metabolism. Cell Rep. 2020;30:949-958. doi: https://doi.org/10.1016/j.celrep.2019.12.089
76. Cawthorn WP, Scheller EL, Learman BS, et al. Bone marrow adipose tissue is an endocrine organ that contributes to increased circulating adiponectin during caloric restriction. Cell Metab. 2014;20(2):368-375.doi: https://doi.org/10.1016/j.cmet.2014.06.003
77. Li Q, Wu Y, Kang N. Marrow Adipose Tissue: Its Origin, Function, and Regulation in Bone Remodeling and Regeneration. Stem Cells Int. 2018;2018:1-11. doi: https://doi.org/10.1155/2018/7098456
78. Cuminetti V, Arranz L. Bone Marrow Adipocytes: The Enigmatic Components of the Hematopoietic Stem Cell Niche. J Clin Med. 2019;8(5):707. doi: https://doi.org/10.3390/jcm8050707
79. Zou W, Rohatgi N, Brestoff JR, et al. Ablation of Fat Cells in Adult Mice Induces Massive Bone Gain. Cell Metab. 2020;32(5):801-813. doi: https://doi.org/10.1016/j.cmet.2020.09.011
80. Zhong L, Yao L, Seale P, Qin L. Marrow adipogenic lineage precursor: A new cellular component of marrow adipose tissue. Best Pract Res Clin Endocrinol Metab. 2021:101518. doi: https://doi.org/10.1016/j.beem.2021.101518
81. Tencerova M, Figeac F, Ditzel N, et al. High-Fat Diet-Induced Obesity Promotes Expansion of Bone Marrow Adipose Tissue and Impairs Skeletal Stem Cell Functions in Mice. J Bone Miner Res. 2018;33(6):1154-1165. doi: https://doi.org/10.1002/jbmr.3408
82. Bredella MA, Torriani M, Ghomi RH, et al. Vertebral bone marrow fat is positively associated with visceral fat and inversely associated with IGF-1 in obese women. Obesity (Silver Spring). 2011;19(1):49-53. doi: https://doi.org/10.1038/oby.2010.106
83. Santopaolo M, Gu Y, Spinetti G, Madeddu P. Bone marrow fat: friend or foe in people with diabetes mellitus? Clin Sci (Lond). 2020;134(8):1031-1048. doi: https://doi.org/10.1042/CS20200220
84. Fazeli PK, Klibanski A. The paradox of marrow adipose tissue in anorexia nervosa. Bone. 2019;118:47-52. doi: https://doi.org/10.1016/j.bone.2018.02.013
85. Li Y, Meng Y, Yu X. The Unique Metabolic Characteristics of Bone Marrow Adipose Tissue. Front Endocrinol (Lausanne). 2019;10:69. doi: https://doi.org/10.3389/fendo.2019.00069
86. Wang QA, Scherer PE. Remodeling of Murine Mammary Adipose Tissue during Pregnancy, Lactation, and Involution. J Mammary Gland Biol Neoplasia. 2019;24(3):207-212. doi: https://doi.org/10.1007/s10911-019-09434-2
87. Colleluori G, Perugini J, Barbatelli G, Cinti S. Mammary gland adipocytes in lactation cycle, obesity and breast cancer. Rev Endocr Metab Disord. 2021;22(2):241-255. doi: https://doi.org/10.1007/s11154-021-09633-5
88. Morroni M, Giordano A, Zingaretti MC, et al. Reversible transdifferentiation of secretory epithelial cells into adipocytes in the mammary gland. Proc Natl Acad Sci USA. 2004;101(48):16801–16806. doi: https://doi.org/10.1073/pnas.04076 47101
89. Дедов И.И., Мельниченко Г.А., Романцова Т.И. Синдром гиперпролактинемии. — М.: Триада; 2004. — 304 с.
90. Song T, Kuang S. Adipocyte dedifferentiation in health and diseases. Clin Sci (Lond). 2019;133(20):2107-2119. doi: https://doi.org/10.1042/CS20190128
91. Cinti S. Pink Adipocytes. Trends Endocrinol Metab. 2018;29(9):651-666. doi: https://doi.org/10.1016/j.tem.2018.05.007
92. Prokesch A, Smorlesi A, Perugini J, et al. Molecular aspects of adipo-epithelial transdifferentiation in mouse mammary gland. Stem Cells. 2014;32(10):2756-2766. doi: https://doi.org/10.1002/stem.1756
93. Wang QA, Song A, Chen W, et al. Reversible De-differentiation of Mature White Adipocytes into Preadipocyte-like Precursors during Lactation. Cell Metab. 2018;28(2):282-288. doi: https://doi.org/10.1016/j.cmet.2018.05.022
94. Wang W, Ishibashi J, Trefely S, et al. A PRDM16-Driven Metabolic Signal from Adipocytes Regulates Precursor Cell Fate. Cell Metab. 2019;30(1):174-189. doi. https://doi.org/10.1016/j.cmet.2019.05.005
95. Giordano A, Perugini J, Kristensen DM, et al. Mammary alveolar epithelial cells convert to brown adipocytes in post-lactating mice. J Cell Physiol. 2017;232(11):2923-2928. doi. https://doi.org/10.1002/jcp.25858
96. Li L, Li B, Li M, et al. Brown adipocytes can display a mammary basal myoepithelial cell phenotype in vivo. Mol Metab. 2017;6(10):1198-1211. doi: https://doi.org/10.1016/j.molmet.2017.07.015
97. Kothari C, Diorio C, Durocher F. The Importance of Breast Adipose Tissue in Breast Cancer. Int J Mol Sci. 2020;21(16):5760. doi: https://doi.org/10.3390/ijms21165760
98. Colleluori G, Perugini J, Di Mercurio E, et al. Mammary gland adipo-epithelial remodelling during the lactation cycle. Obes Rev. 2020;21(S1):A201-202. doi: https://doi.org/10.1111/obr.13115
99. Zwick R, Guerrero-Juarez CF, Horsley V, Plikus MV. Anatomical, physiological and functional diversity of adipose tissue. Cell Metab. 2018;27(1):68-83. doi: https://doi.org/10.1016/j.cmet.2017.12.002
100. Ben-Jonathan N, Hugo E. Prolactin (PRL) in adipose tissue: regulation and functions. Adv Exp Med Biol. 2015;846:1-35. doi: https://doi.org/10.1007/978-3-319-12114-7_1
101. Cinti S, Mitchell G, Barbatelli G, et al. Adipocyte death defines macrophage localization and function in adipose tissue of obese mice and humans. J Lipid Res. 2005;46(11):2347-2355. doi. https://doi.org/10.1194/jlr.M5002 94-JLR200
102. Cinti S. White, brown, beige and pink: A rainbow in the adipose organ. Curr Opin Endocr Metab Res. 2019;4:29-36. doi: https://doi.org/10.1016/j.coemr.2018.07.003
Об авторе
Т. И. РоманцоваРоссия
Романцова Татьяна Ивановна, д.м.н., профессор; eLibrary SPIN: 3855-5410
Россия, 119991, ул. Б. Пироговская, д. 2, стр. 4
Дополнительные файлы
|
|
1. Рисунок 1. Фенотипические и функциональные свойства белых, бурых, бежевых, желтых, розовых адипоцитов (адаптировано из работы J. Zinngrebe и соавт., 2020) [7]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(503KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Липиды грудного молока алкилглицерины (АКГ) индуцируют браунинг белых адипоцитов у младенцев (адаптировано из работы H. Yo и соавт., 2019) [47]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(228KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Аутокринные, паракринные и эндокринные эффекты батокинов (адаптировано из работы C. Scheele и соавт., 2020) [31]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(397KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Регуляторное влияние предшественников адипоцитов MALPs на клетки костного мозга (адаптировано из работы L. Chong и соавт., 2021) [80]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(383KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Трансдифференциация адипоцитов молочной железы в лактационном цикле (адаптировано из работы C. Kothari и соавт., 2020) [97]. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(342KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Романцова Т.И. Жировая ткань: цвета, депо и функции. Ожирение и метаболизм. 2021;18(3):282-301. https://doi.org/10.14341/omet12748
For citation:
Romantsova T.I. Adipose tissue: colors, depots and functions. Obesity and metabolism. 2021;18(3):282-301. (In Russ.) https://doi.org/10.14341/omet12748

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).










































