Перейти к:
Изменения антропометрических характеристик, уровня андрогенов и эстрогенов при коррекции мужского гипогонадизма препаратами тестостерона или хорионического гонадотропина: результаты ретроспективного сравнительного исследования
https://doi.org/10.14341/omet12733
Аннотация
Обоснование. Использование тестостеронзаместительной терапии (ТЗТ) широко распространено. Несмотря на положительные изменения, такие как увеличение уровня тестостерона, улучшение эректильной функции и рост либидо, возможно развитие негативного проявления — гиперэстрогении. На сегодняшний день отсутствуют исследования, оценивающие распространенность развития гиперэстрогении на фоне ТЗТ.
Цель. Изучить достоверность повышения уровней общего тестостерона и эстрадиола и изменения общего веса, индекса массы тела (ИМТ), длин окружности талии (ОТ) и бедер (ОБ) в зависимости от вида ТЗТ и терапии хорионическим гонадотропином человека (ХГЧ).
Материалы и методы. Для ретроспективного анализа были отобраны истории болезни пациентов с исходным дефицитом тестостерона и нормальным уровнем эстрадиола, которым была назначена ТЗТ или ХГ-терапия.
Уровни тестостерона, эстрадиола, глобулина, связывающего половые гормоны (ГСПГ), вес, ОТ, ОБ, ИМТ в каждой группе оценивали 2 раза — перед назначением лечения и в разные периоды лечения, например, через 3–6–9 и 12 мес. Большинство пациентов имели период контроля данных параметров до назначения ТЗТ или ХГ-терапии и через 6 мес.
Результаты. В исследование было включено 60 историй болезни пациентов с исходным дефицитом тестостерона и нормальным уровнем эстрадиола и избыточной массой тела или ожирением. Повышение уровней общего тестостерона и эстрадиола на фоне ТЗТ в общей выборке составило 109,6 и 111,3% соответственно.
В каждой группе повышение уровней общего тестостерона и эстрадиола было достоверным, p≤0,001. Уровень общего тестостерона до физиологических значений повысился только во 2-й группе — достигая средне-нормальных, рекомендованных уровней, с 8,7±0,5 (2,5) и до 16±2 (10) нмоль/л. Максимальные подъемы общего тестостерона, как и эстрадиола, были отмечены в 1-й группе, с 9,5±0,72 (3) до 24,9±2,7 нмоль/л (11,62) нмоль/л и с 24,19±2 (8,5) до 58,1±4 (18,1) нмоль/л соответственно. ТЗТ, как и ХГ-терапия, способствует росту уровня эстрадиола, что было продемонстрировано во всех группах, а не только 1-й группе: во 2-й группе с 28,1±2,3 (11,3) до 55±4 (20) нмоль/л и в 3-й группе с 27,1±2,5 (10,5) до 55,8±4,6 (19,6) нмоль/л. В среднем по всей выборке — с 26,6±1,32 (10,2) до 56,2±2,5 (19) нмоль/л. Снижение веса на ТЗТ достоверным оказалось только во 2-й группе, причем по всем параметрам — весу, ИМТ, длинам ОТ и ОБ. В 3-й группе также незначительно уменьшились ИМТ, величины ОТ и ОБ. В 1-й группе общий вес незначительно увеличился, при этом ИМТ не изменился, как и величина ОБ, а величина ОТ незначительно уменьшилась.
Заключение. ТЗТ достоверно повышает уровни общего тестостерона и эстрадиола, способствуя нормализации уровня тестостерона, как во 2-й группе, или развитию супрафизиологических уровней общего тестостерона и гиперэстрогении, как в 1-й и 3-й группах. Учитывая, что сформировалось стойкое убеждение, что ТЗТ приводит к значительному снижению веса, наше исследование подтвердило это заявление только во 2-й группе.
Для цитирования:
Павлова З.Ш., Голодников И.И., Орлова Я.А., Камалов А.А. Изменения антропометрических характеристик, уровня андрогенов и эстрогенов при коррекции мужского гипогонадизма препаратами тестостерона или хорионического гонадотропина: результаты ретроспективного сравнительного исследования. Ожирение и метаболизм. 2021;18(3):268-275. https://doi.org/10.14341/omet12733
For citation:
Pavlova Z.S., Golodnikov I.I., Orlova Y.A., Kamalov A.A. Changes in anthropometric characteristics, androgen and estrogen levels during correction of male hypogonadism with testosterone or hCG: results of a retrospective comparative study. Obesity and metabolism. 2021;18(3):268-275. (In Russ.) https://doi.org/10.14341/omet12733
ОБОСНОВАНИЕ
Медицинский прогресс позволил человеку доживать до периода, когда его эндокринные железы, в том числе и половые, истощаются, например, с последующим развитием дефицита общего тестостерона у мужчин. Количество мужчин, достигших возраста старше 85 лет, за последний век стало в 31 раз больше [1]. Но нынешний тренд — это дефицит общего тестостерона у достаточно молодых мужчин и снижение среднего уровня тестостерона у молодых мужчин в сравнении с предыдущими годами, примерно с 18,5 нмоль/л до 14,5 нмоль/л [2][3]. Напомним, что «пороговым значением, позволяющим разграничить нормальное состояние и потенциальный дефицит тестостерона, следует считать 12,1 нмоль/л для общего тестостерона сыворотки крови (уровень 2b, степень A)» [4][5].
В течение последних 5 десятилетий прогрессивно распространяется ожирение [6]. Именно оно зачастую и сопровождает молодых и мужчин среднего возраста с андрогенным дефицитом и является патогенетической основой для его развития. Выраженно разнятся эпидемиологические данные относительно андрогенного дефицита. По данным одних авторов, распространенность дефицита тестостерона среди мужчин европейцев и американцев, среднего и пожилого возраста варьировала от 2,1% до 12,8%, увеличиваясь у мужчин с избыточной массой тела или ожирением, сахарным диабетом 2 типа (СД2) и другими сопутствующими заболеваниями [7]. Вариабельность распространенности дефицита тестостерона от 10 до 40% у мужчин старше 45 лет, по данным российских ученых, вызывает большой интерес и желание получить более точные данные [8]. Результаты Балтиморского исследования старения мужчин показывают, что каждый десяток лет увеличивается количество мужчин с андрогенным дефицитом, начиная от 20% среди мужчин старше 60 и заканчивая 50% среди мужчин старше 80 лет [9–12].
Carruthers M., назвав адипоцит «осью зла», обосновал развитие метаболического синдрома, СД2, андрогенного дефицита и прочих коморбидных ожирению состояний изначальным развитием воспаления в избыточно развитой жировой ткани [13]. В 2010 г. Всемирным эндокринологическим обществом и в 2013 г. МЗ РФ были даны рекомендации о необходимости контроля общего тестостерона у пациентов с ожирением и СД2, что повышает частоту выявления андрогенного дефицита, соответственно, компенсацию этого дефицита и эффективность проводимого лечения в целом [14–23]. Именно от воспаления жировой ткани у мужчин с избыточной массой тела и/или ожирением, активизации в этих условиях фермента ароматазы и проистекает замаскированный под абсолютный андрогенный дефицит процесс избыточной конвертации тестостерона в эстрадиол [24–27]. Так как определение эстрадиола не рекомендовано, то, не имея объективной информации по распространенности гиперэстрогении, ее как бы не существует, и никто не может оценить ее наличия и масштабов. Однако проблема гиперэстрогении очень актуальна во всем мире, и одна из последних работ, опубликованная в мае 2020 г., в полной мере отражает высокий интерес специалистов, использующих тестостеронзаместительную терапию (ТЗТ) [28].
Актуальность нашей работы заключается в том, что сегодня практически нет эпидемиологических данных о выраженности гиперэстрогении у мужчин с нарушенным составом тела на фоне ТЗТ.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Целью ретроспективного одноцентрового когортного исследования (анализа медицинской документации пациентов с исходным дефицитом тестостерона и использованием у них ТЗТ и ХГ-терапии) являлось изучение достоверности повышения уровней общего тестостерона и эстрадиола, изменения общего веса, индекса массы тела (ИМТ), длин окружности талии (ОТ) и окружности бедер (ОБ) на фоне ТЗТ в зависимости от вида ТЗТ.
МАТЕРИАЛЫ И МЕТОДЫ
Место и время проведения исследования
Место проведения. Работа выполнена на базе Университетской клиники МНОЦ МГУ им. М.В. Ломоносова.
Время исследования. Были отобраны истории болезней пациентов, проходивших лечение в период с февраля 2015 по апрель 2020 гг. Данные каждого конкретного пациента оценивались за период лечения в полгода от начала использования ТЗТ или хорионического гонадотропина человека (ХГЧ).
Изучаемые популяции (одна или несколько)
Изучалась одна популяция.
Критерии включения: мужской пол, возраст от 18 лет и до 75 лет включительно, исходный дефицит тестостерона, нормальный уровень эстрадиола, с избыточной массой тела или ожирением.
Критерии исключения: в исследование не включали пациентов с доброкачественной гиперплазией предстательной железы, с тяжелым течением СД2 в стадии декомпенсации, с кризовым течением гипертонической болезни, в возрасте до 18 лет, дефицитом массы тела, с повышенными или пониженными уровнями лютеинизирующего (ЛГ) и фолликулостимулирующего гормонов (ФСГ), гиперпролактинемией (пролактин выше 475 мМе/л), повышенным уровнем тиреотропного гормона (ТТГ), более 4 мкМЕ/мл.
Способ формирования выборки из изучаемой популяции (или нескольких выборок из нескольких изучаемых популяций)
Выборка была создана произвольным образом, исходя из необходимости наличия полноты исходных данных в историях болезни.
Дизайн исследования
Одноцентровое обсервационное ретроспективное когортное одновыборочное исследование.
Методы
Эндокринные и патологии внутренних органов мы могли определить и в последующем исключить таких пациентов из анализа по имеющимся в их историях болезни результатам обследования. Например, при повышенном уровне ТТГ или повышенных печеночных трансаминазах, имеющихся УЗ-исследованиях мы делали соответствующие выводы и обозначали это в критериях исключения.
Пациенты были разделены на группы по используемому препарату тестостерона, а именно:
- 1-я группа — пациенты, которым производили внутримышечные инъекции тестостерона ундеканоата 25% (1000 мг в 4 мл масляного раствора, в среднем 1 раз в 8–10 недель);
- 2-я группа — пациенты, которым назначили 1% гель 5 мл, содержащий тестостерон (50 мг тестостерона, 1 раз в день);
- 3-я группа — пациенты, которым производили внутримышечные инъекции хорионического гонадотропина человека в форме лиофилизата или готового раствора (в среднем 2000 МЕ, 2 раза в неделю).
Использование тех или иных форм тестостерона, как мы предполагаем, не основывалось на финансовых возможностях пациентов, в том числе и потому, что средняя стоимость в пересчете на стоимость одного дня тестостерона ундеканоата и гелевой формы тестостерона примерно одинаковая. Выяснить все детали, используя ретроспективно данные историй болезни, не всегда представляется возможным, но при подборе пациентов учитывалась сравнимость их исходных состояний. Выбор в пользу ХГЧ, как и должно, производился у пациентов с репродуктивными планами в ближайшей перспективе, что всегда выясняется до начала лечения пациентов с гипогонадизмом.
Уровень тестостерона, эстрадиола, глобулина, связывающего половые гормоны (ГСПГ), вес, ОТ, ОБ, ИМТ в каждой группе оценивали 2 раза — перед назначением лечения и в разные периоды лечения, например, через 3–6–9 и 12 мес. Большинство пациентов имели период контроля данных параметров до назначения ТЗТ или ХГ-терапии и через 6 мес.
Для определения тех или иных параметров в сыворотке крови использовались следующие лабораторные методы.
Эстрадиол определяли автоматизированным способом при помощи хемилюминесцентного анализа и реагента Access Sensitive Estradiol на аппарате Beckman Coulter UniCell DxI 800. Использовалась сыворотка крови.
ГСПГ (SHBG) определяли автоматическим образом на аппарате Beckman Coulter UniCell DxI 800 с использованием реагента Access SHBG, с использованием хемилюминесцентного анализа. Использовалась сыворотка крови.
Тестостерон определяли автоматизированной системой аппарата Beckman Coulter UniCell DxI 800 методом хемилюминесцентного анализа Access Testosterone, Total, с использованием реагента Beckman Coulter UniCell DxI 800. Использовалась сыворотка крови.
Клинический осмотр и оценка антропометрических параметров.
Всем пациентам проводилось общеклиническое обследование, включавшее сбор анамнеза, жалоб, физикальный осмотр, оценку физического и полового развития. Оценка физического развития осуществлялась на основании антропометрических показателей — роста и массы тела. Рост измерялся при помощи механического ростомера (Harpenter stadiometr, Holtain Ltd, UK) с точностью до 1 мм. Масса тела измерялась на электронных напольных весах.
Измерение ОТ производится на середине расстояния между краем последнего ребра и гребнем подвздошной кости (crista iliaca), в положении стоя в конце выдоха, с использованием специальной сантиметровой ленты с регулятором натяжения. ОБ — окружность бедер определяется накладыванием сантиметровой ленты на наиболее выступающие назад точки ягодичной области, а сбоку и впереди лента располагается строго горизонтально. Определение соотношения ОТ к ОБ или индекс талия/бедра (аббревиатуры СТБ, ИТБ или WHR — от англ. waist-hip-ratio) определяется простым делением значения ОТ на ОБ.
При использовании ТЗТ большинством научных школ рекомендовано облегчение симптомов гипогонадизма путем восстановления сывороточных уровней тестостерона до нормальных физиологических значений, на уровне 14–17,5 нмоль/л [ 4,29–30 ]. Превышение этих значений рассматривается как супрафизиологические концентрации тестостерона. Каждая лаборатория устанавливает свои пороговые значения, но ученые, как и клиницисты, ориентируются на экспертное мнение мировых школ.
К сожалению, нет единого мнения по поводу референсных значений эстрадиола в крови у мужчин. Американская авторитетная клиника Mayo Clinic рекомендует пороговое значение от 10 до 40 пг/мл [31]. В европейских странах пороговым уровнем эстрадиола у мужчин принято считать от 12 до 37,4 пг/мл [32]. В Индии и странах Юго-Восточной Азии эти цифры иные — от 11,6 до 41,2 [33]. В нашей стране, так же как и во всем мире, нет единого диапазона, и от лаборатории к лаборатории можно встретить существенно отличающиеся значения. Наиболее распространенным значением в референсных диапазонах для эстрадиола у мужчин является показатель <47 пг/мл, или в среднем 40–161 пмоль/л. Мы проводили расчеты исходя из двух значений — среднего и наиболее высокого, 11,6–41,2 и <47 пг/мл соответственно.
Статистический анализ
Для каждой характеристики и критерия были определены следующие статистические параметры: среднее, стандартное отклонение, стандартная ошибка. Для проверки распределений на нормальность использовался одновыборочный критерий Колмогорова–Смирнова, уровень значимости — 0,05. Для проверки различия значений выборок использовался критерий Вилкоксона, уровень значимости — 0,05. Расчет производили в программе IBM SPSS 23.0
Этическая экспертиза
Исследование одобрено ЛЭК МНОЦ МГУ им. М.В. Ломоносова, прошедшего 20 сентября 2021 г., протокол под номером 6/21.
РЕЗУЛЬТАТЫ
Всего в анализ вошли 60 пациентов, которые были разделены на 3 группы по используемому препарату тестостерона, а именно:
- 1-я группа — 18 человек;
- 2-я группа — 24 человека;
- 3-я группа — 18 человек.
Забегая вперед, демонстрируем повышение уровней тестостерона и эстрадиола на фоне ТЗТ в общей выборке, которое составило 109,6% и 111,3% соответственно от исходного уровня. Общая характеристика всех пациентов представлена в таблице 1.
В каждой группе повышение уровней общего тестостерона и эстрадиола было достоверным (рис. 1, 2). Минимально уровень тестостерона повысился во 2-й группе. Максимальные подъемы тестостерона, как и эстрадиола, были отмечены в 1-й группе, при том, что минимальное значение исходного уровня эстрадиола было именно в этой группе.
Снижение общего веса на ТЗТ достоверным оказалось только во 2-й группе, причем по всем изученным параметрам: общему весу, ИМТ, величинам ОТ и ОБ (рис. 3, 4, 5,6). Также произошло повышение уровня ГСПГ во всех исследуемых группах, но достоверным оно оказалось только в 1-й и во 2-й группах (рис. 7).
Нежелательные явления зафиксированы не были. Мы не нашли их отражения ни в опросе пациентов при проведении контрольных приемов, ни в результатах контрольных лабораторных данных.
Таблица 1. Клинико-антропометрические данные пациентов, вошедших в ретроспективный анализ исследования.
Группа | Тестостерона ундеканоат 25% (18 человек) | Гель тестостерона 1% 50 мг (24 человека) | ХГЧ (2000 МЕ 2 раза в неделю) (18 человек) | Вся выборка (всего 60 человек) |
Возраст, лет | 52±2,3 (10) | 51±2,6 (13) | 47±3 (12) | 49±1,5 (11,8) |
Рост, см | 179±1,3 (5,4) | 177±1,3 (6,3) | 183±1,5 (6,5) | 179,3±0,8 (6,5) |
Вес 1 (до терапии), кг | 95,1±1,3 (5,4) | 102,8±4,2 (20,7) | 96,5±3,2 (13,6) | 98,6±2,3 (18) |
Вес 2 (после терапии), кг | 95,2±4,4 (19) | 99,5±3,6 (18)* | 95,7±3 (13) | 97,1±2,1 (16,6) |
ИМТ 1 (до терапии), кг/м2 | 28,35 (25,38; 32,5) | 32,6 (27; 39,5) | 28,85 (26,5; 32,1) | 28,9 (26,65; 32,8) |
ИМТ 2 (после терапии), кг/м2 | 28,1 (26; 31,5) | 31,9 (27,1; 37,85)* | 28,4 (26,8; 31,33) | 29,55 (26,9; 32,8) |
ОТ 1, см (до терапии), см | 99,6±2,8 (12) | 107,5±3 (14,6) | 95,7±2,2 (9,3) | 101,6±1,7 (13,3) |
ОТ 2, см (после терапии), см | 99,4±3,1 (13) | 103±2,5 (12,4)* | 94,5±2 (8,4) | 99,4±1,5 (12) |
ОБ 1, см (до терапии), см | 101,8±2,2 (9,3) | 108,4±2,2 (11) | 103,9±1,8 (7,5) | 105±1,3 (9,8) |
ОБ 2, см (после терапии), см | 101,8±2 (8,5) | 106±1,5 (7,6)* | 102,3±1,5 (6,1) | 103,9±1 (7,6) |
Т1 (исходный уровень тестостерона), нмоль/л | 9,5±0,72 (3) | 8,7±0,5 (2,5) | 9,96±0,5 (2,1) | 9,4±0,3 (2,6) |
Т2 (уровень тестостерона на фоне ТЗТ), нмоль/л | 24,9±2,7 (11,62)* | 16±2 (10)* | 19,5±2,5 (11)* | 19,7±1,4 (11,2) |
Э1 (исходный уровень эстрадиола), пг/мл | 23,05 (20,03; 29,1) | 26,4 (20; 34,93) | 26 (20,78; 31,6) | 24 (20,33; 32) |
Э2 (уровень эстрадиола на фоне ТЗТ), пг/мл | 51,58 (45,48; 66,05)* | 54,27 (43,65; 65,93)* | 50 (44,6; 65,3)* | 51,2 (44,8; 65,23) |
ГСПГ 1 (исходный уровень ГСПГ), нмоль/л | 28±2,7 (11,5) | 26,4±2,3 (11) | 29,5±3,7 (15,6) | 27,8±1,6 (12,6) |
ГСПГ 2 (уровень ГСПГ на фоне ТЗТ), нмоль/л | 36,4±3,7 (15,8)* | 30,7±2,8 (14)* | 31,4±3,6 (15,4) | 32,6±2 (15) |
*разница достоверна, р<0,05. Значения указаны согласно следующему формату — среднее ± стандартная ошибка (стандартное отклонение) (для параметров, распределенных нормально) или медианы и 25% и 75% процентиля (для параметров, распределенных ненормально).
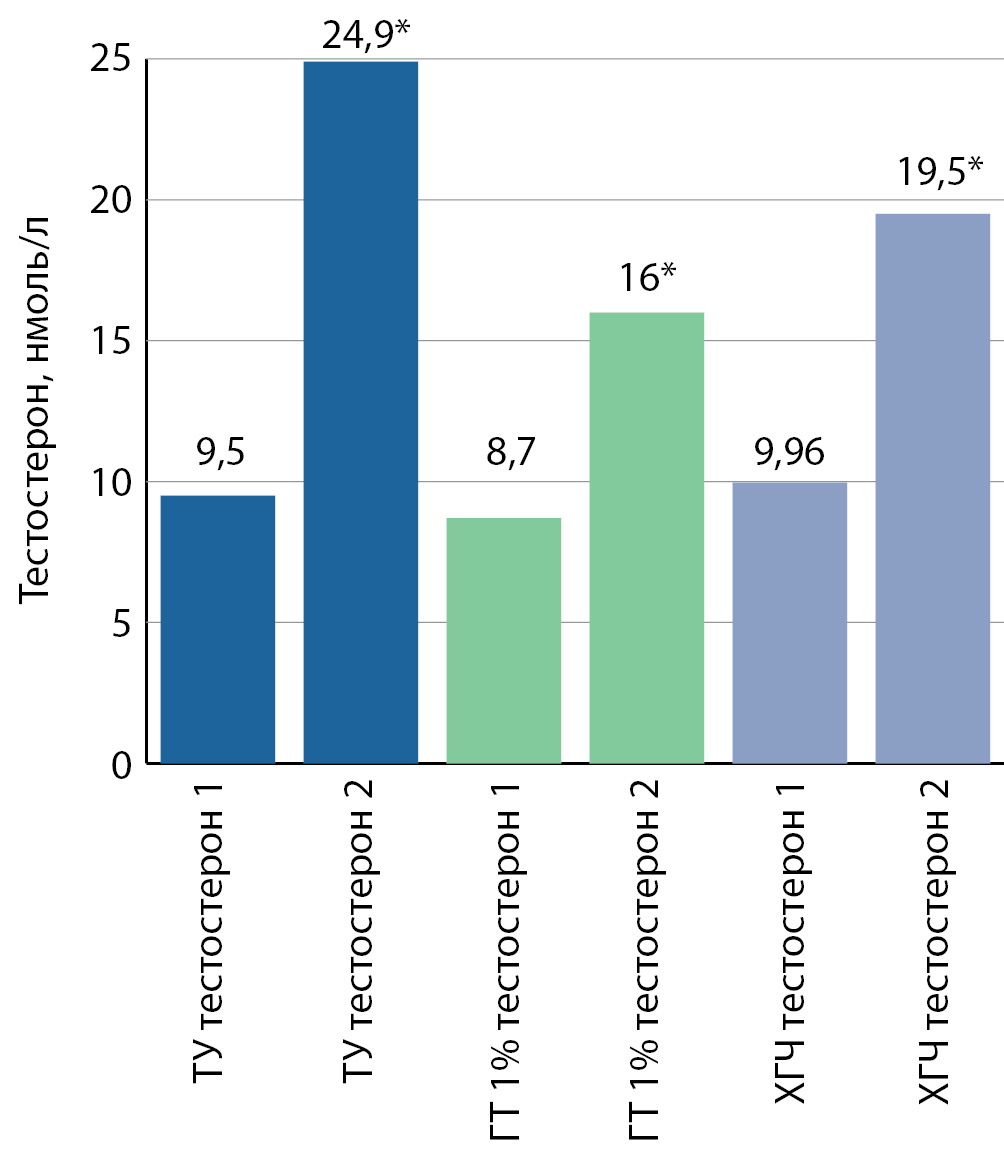
Рисунок 1. Уровень тестостерона до и на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. Данные представлены в виде средних значений в полученных группа. На рисунках 1–7: ТУ — тестостерона ундеканоат; ГТ — гель тестостерона; ХГЧ — хорионический гонадотропин человека. Использован статистический метод – критерий Вилкоксона; уровень статистической значимости 0,05, звездочкой помечены статистически значимые различия.
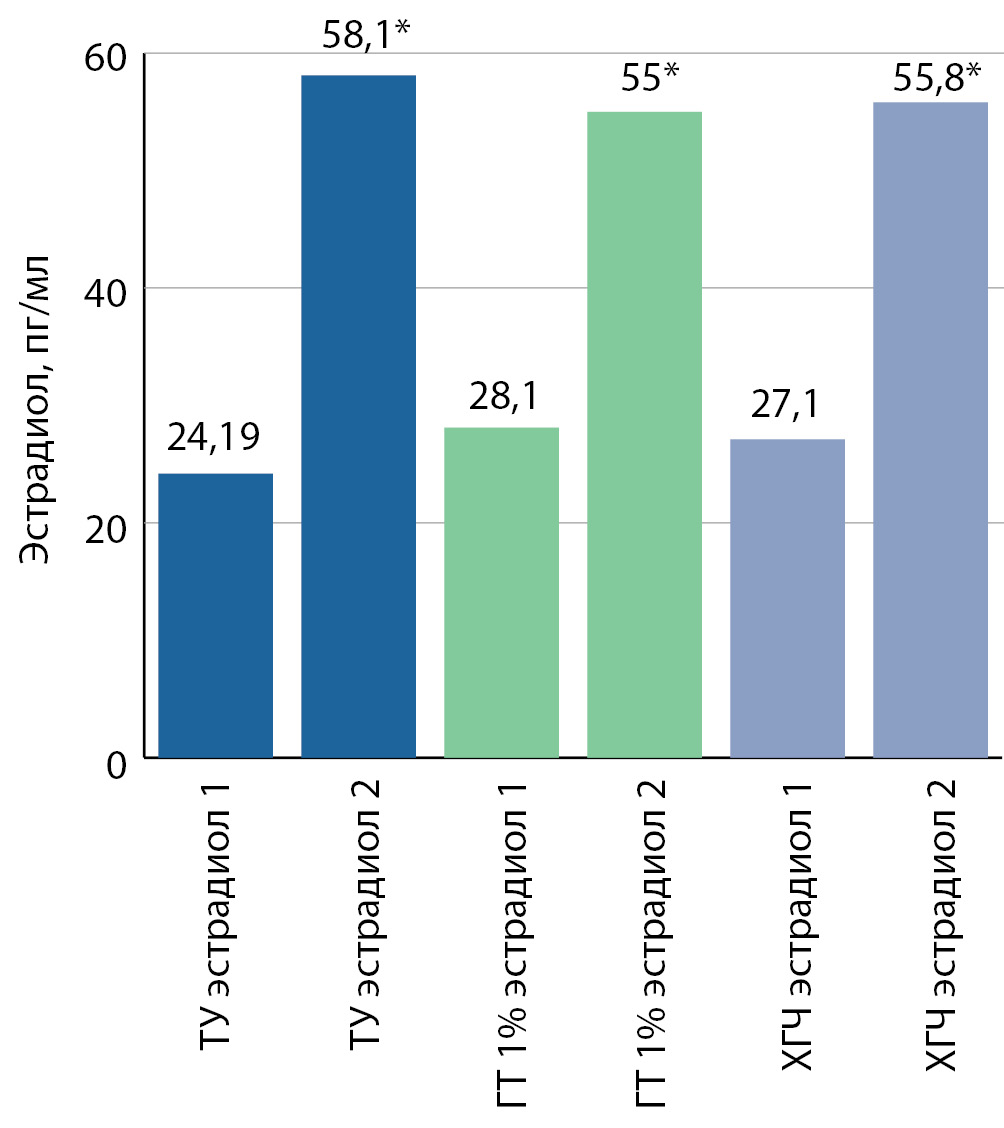
Рисунок 2. Уровень эстрадиола до и на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. Данные представлены в виде средних значений в полученных группах.

Рисунок 3. Изменение веса в кг на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. Данные представлены в виде средних значений в полученных группах.
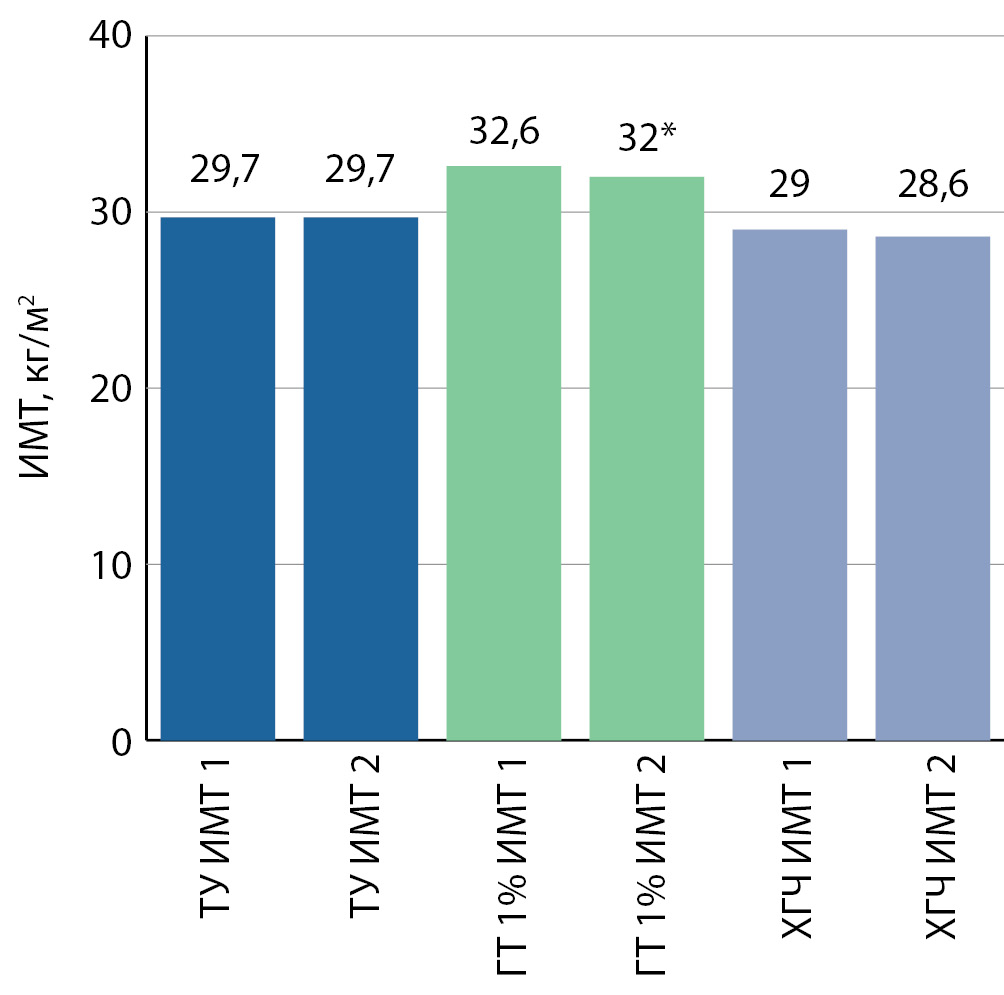
Рисунок 4. Изменение индекса массы тела, кг/м2, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. Данные представлены в виде средних значений в полученных группах.
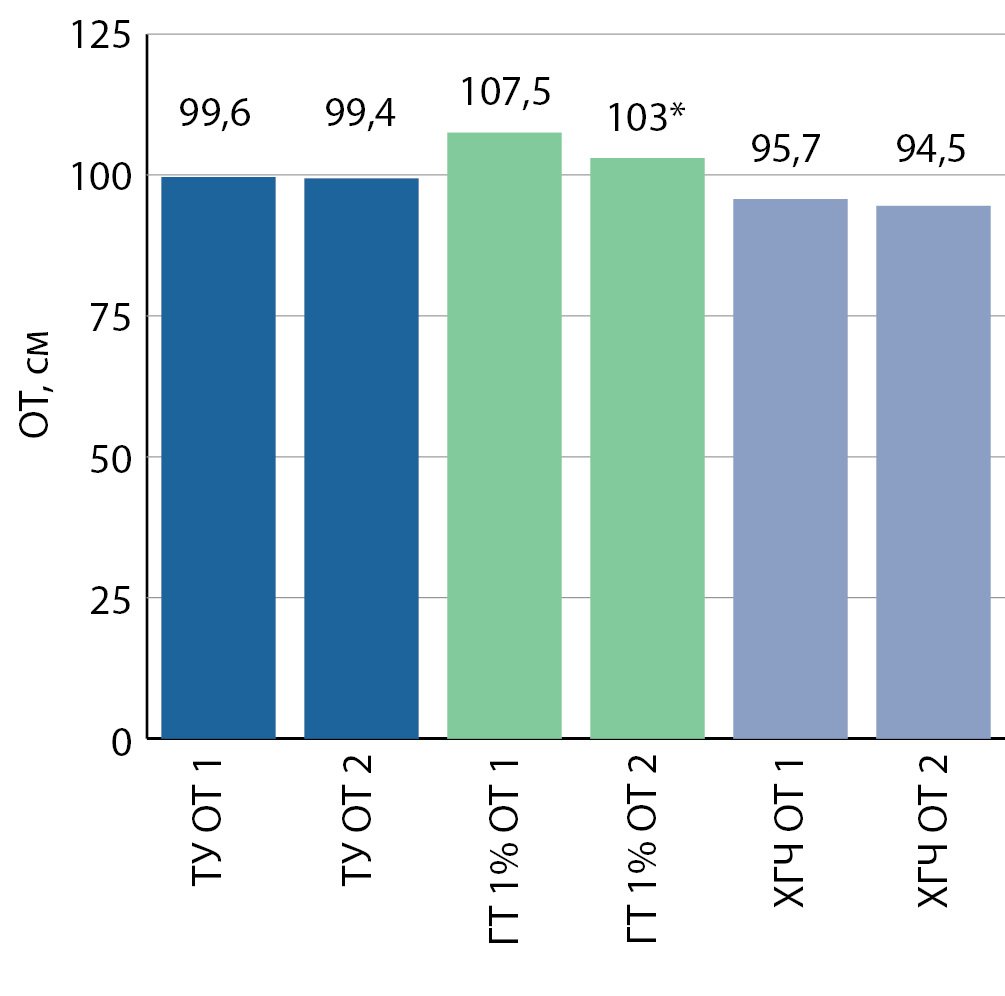
Рисунок 5. Изменение окружности талии, см, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. Данные представлены в виде средних значений в полученных группах.
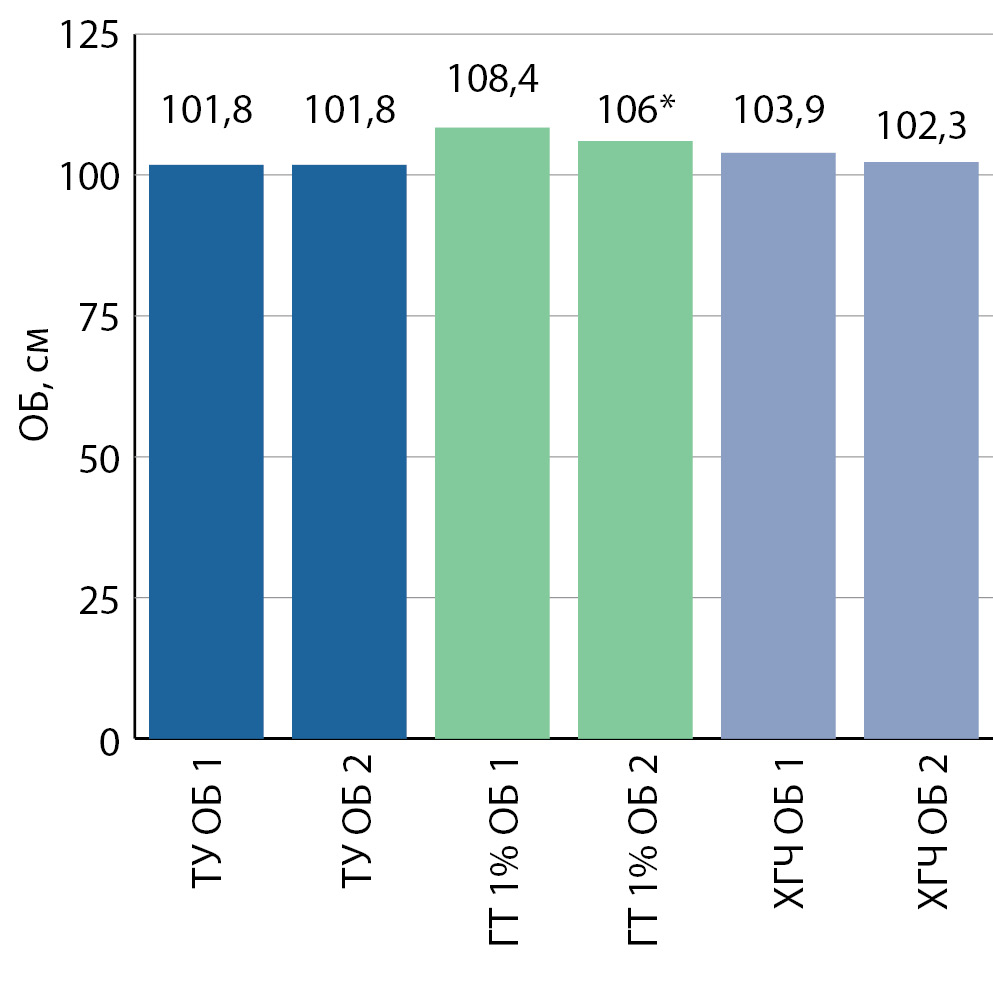
Рисунок 6. Изменение окружности бедер, см, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. Данные представлены в виде средних значений в полученных группах.
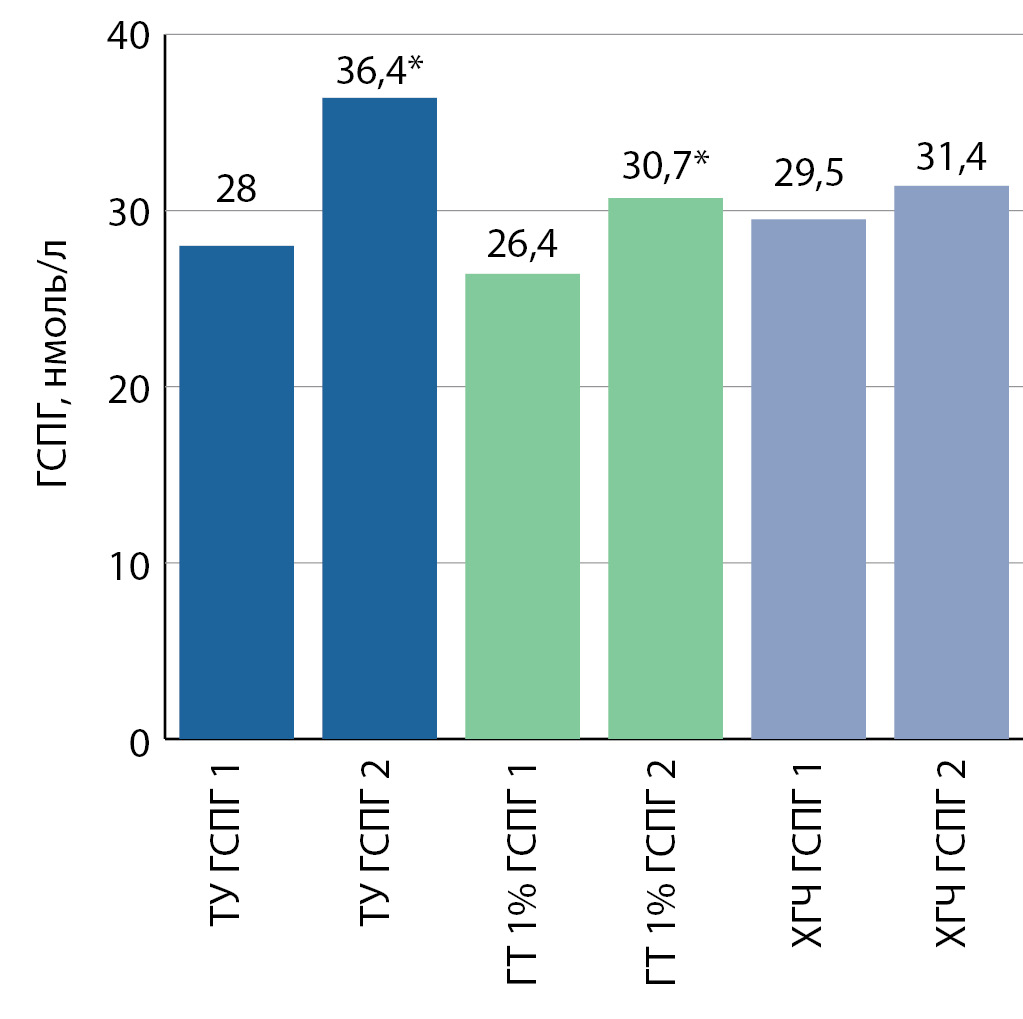
Рисунок 7. Изменение уровней глобулина, связывающего половые гормоны, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. Данные представлены в виде средних значений в полученных группах.
ОБСУЖДЕНИЕ
Репрезентативность выборок
Формируя выборочную совокупность, мы старались учесть особенности генеральной выборки, а именно мужчин с аналогичным возрастом и весом как базовыми пунктами для нашего исследования. Исследование проводилось на базе федерального учреждения (клиники), закрепленного и входящего в состав научно-образовательного кластера, соответственно, практически у всех пациентов (точные данные не собирались) имеется высшее образование и профессиональная реализация. Данный факт, теоретически, влияет на лучшую приверженность к терапии, чем в генеральной совокупности, тем самым моделируя идеальные условия, когда пациент не пропускает дни использования лекарственного средства и не нарушает режим дозирования.
Сопоставление с другими публикациями
Тема гиперэстрогении у мужчин становится актуальнее год от года, в том числе и в связи с растущим количеством исследований, содержащих противоречивые данные в отношении положительных или отрицательных последствий для мужчин [32–34]. При противоречивости одних данных другие данные, такие как распространенность гиперэстрогении у мужчин или повышение уровней общего тестостерона и эстрадиола на фоне ТЗТ, практически отсутствуют. Именно поэтому и возникла потребность в исследовании, которое было нами проведено. Полученные нами результаты показали, что ТЗТ в любых ее формах достоверно повышает уровень эстрадиола, до 111,3% в общей выборке по сравнению с исходным уровнем. Кроме того, в двух группах, в 1-й и в 3-й, достигались супрафизиологические уровни общего тестостерона до 109,6% в общей выборке. Во 2-й группе уровень тестостерона также повышался достоверно, но оставался в пределах нормальных рекомендованных значений. Несмотря на то что сформировалось стойкое убеждение, что ТЗТ приводит к значительному снижению веса, наше исследование подтвердило это заявление только во 2-й группе.
Мы не можем оценить долгосрочные эффекты гиперэстрогении у этих пациентов, так как это ретроспективный анализ. Но полученные данные демонстрируют достоверное развитие гиперэстрогении и должны подстегнуть интерес ученых и клиницистов к этой теме.
Клиническая значимость результатов
Клиническая значимость данного исследования заключается в том, что полученные данные демонстрируют положительные и отрицательные эффекты разных вариантов ТЗТ и ХГ-терапии, которые не представлены широко в мировой литературе, и это может способствовать более оправданному и индивидуально обоснованному выбору тактики лечения клиницистами.
Ограничения исследования
Мы проводили ретроспективный анализ медицинских документов только одного учреждения. Также ограничением нашей работы является относительно небольшой размер выборки.
Направления дальнейших исследований
Выявленные нами тенденции требуют дальнейшего изучения в проспективном, желательно мультицентровом исследовании на значительно большем количестве участников и с большим периодом наблюдения для получения максимально объективных данных.
ЗАКЛЮЧЕНИЕ
ТЗТ ожидаемо повышает уровни общего тестостерона во всех группах. В зависимости от формы препарата эти уровни будут существенно отличаться: максимально уровень тестостерона повышался в 1-й группе — с 9,5±0,72 нмоль/л (3) до 24,9±2,7 нмоль/л (11,62), до супрафизиологических значений, минимальное повышение отмечено во 2-й группе (с 8,7±0,5 (2,5) и до 16±2 (10) нмоль/л), до средне-нормальных значений. В среднем по выборке — с 9,4±0,3 (2,6) до 19,7±1,4 (11,2) нмоль/л. Повышение уровня общего тестостерона сопровождается и ростом уровня эстрадиола, что было продемонстрировано во всех группах ТЗТ: в 1-й группе с 24,19±2 (8,5) до 58,1±4 (18,1) нмоль/л, во 2-й группе — с 28,1±2,3 (11,3) до 55±4 (20) нмоль/л и в 3-й группе — с 27,1±2,5 (10,5) до 55,8±4,6 (19,6) нмоль/л. В среднем по всей выборке — с 26,6±1,32 (10,2) до 56,2±2,5 (19) нмоль/л. Максимально выраженно уровень эстрадиола ожидаемо повышался в 1-й группе, так как именно в этой группе были достигнуты максимальные уровни супрафизиологических значений общего тестостерона, при том, что исходный уровень эстрадиола был минимальным в этой группе. Существующее мнение о том, что более высокие уровни общего тестостерона способствуют более выраженному улучшению состава тела, не нашло подтверждения в нашем исследовании. Достоверным улучшение состава тела оказалось только во 2-й группе, причем по всем контролируемым параметрам, а именно: общему весу, ИМТ, величинам ОТ и ОБ. В 3-й группе также незначительно уменьшился ИМТ, величины ОТ и ОБ. В 1-й группе общий вес незначительно увеличился, при этом ИМТ не изменился, как и величина ОБ, а величина ОТ незначительно уменьшилась.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена в рамках Государственного задания МНОЦ МГУ им. М.В. Ломоносова «Разработка, апробация и внедрение методов профилактики, диагностики и лечения возраст-ассоциированных заболеваний» (регистрационный номер: 121061800145-1).
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Павлова З.Ш. — разработка дизайна исследования, написание статьи; Голодников И.И. — получение, анализ данных, интерпретация результатов, написание статьи; Орлова Я.А. — разработка концепции исследования, внесение существенной правки в текст с целью повышения научной ценности статьи. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. Аметов А.С., Пашкова Е.Ю. Эволюция тестостеронозаместительной терапии. Новые формы — новые возможности // Эндокринология: новости, мнения, обучение. — 2017. — №2. — С. 55-65.
2. Peterson MD, Belakovskiy A, McGrath R, Yarrow JF. Testosterone Deficiency, Weakness, and Multimorbidity in Men. Sci Rep. 2018;8(1):5897. doi: https://doi.org/10.1038/s41598-018-24347-6
3. Travison T, et al. Harmonized Reference Ranges for Circulating Testosterone Levels in Men of Four Cohort Studies in the USA and Europe. J. Clin. Endocrinol. Metab. 2017;102:1161–1173. doi: https://doi.org/ 10.1210/jc.2016-2935.
4. Дедов И.И., Мельниченко Г.А., Шестакова М.В., и др. Рекомендации по диагностике и лечению дефицита тестостерона (гипогонадизма) у мужчин с сахарным диабетом // Ожирение и метаболизм. — 2017. — Т. 14. — №4. — С. 83-92.
5. Dohle GR, Arver S, Bettocchi C, et al. EAU 2014 guideline on male hypogonadism. European Association of Urology; 2014. Available from: http://www.uroweb.org/gls/pdf/16_Male_Hypogonadism_LR%20II.pdf [cited 8 Dec 2014].
6. Trends in adult body-mass index in 200 countries from 1975 to 2014: a pooled analysis of 1698 population-based measurement studies with 19-2 million participants. The Lancet. 2016. doi: https://doi.org/10.1016/S0140-6736(16)30054-X.
7. Zarotsky V, Huang M-Y, Carman W, et al. Systematic Literature Review of the Epidemiology of Nongenetic Forms of Hypogonadism in Adult Males. Journal of Hormones. 2014;214:1-17. doi: https://doi.org/10.1155/2014/190347.
8. Галимов Ш.Н., Божедомов В.А., Галимова Э.Ф., и др. Мужское бесплодие. Молекулярные и иммунологические аспекты. — М.: ГЭОТАР-Медиа; 2020.
9. Пашкова Е.Ю., Рождественская О.А. Возрастной андрогенный дефицит у мужчин: этиология, клиника, диагностика, лечение // Андрология и генитальная хирургия. — 2015. — Т. 16. — №1 — С. 95-101.
10. Feldman HA, Longcope C, Derby CA, et al. Age trends in the level of serum testosterone and other hormones in middle-aged men: longitudinal results from the Massachusetts male aging study. The Journal of clinical endocrinology and metabolism. 2002;87(2):589-598. doi: https://doi.org/10.1210/jcem.87.2.8201
11. Bhasin S, Buckwalter JG. Testosterone supplementation in older men: A rational idea whose time has not yet come. J Androl. 2001;22(5):718-731. doi: https://doi.org/10.1002/j.1939-4640.2001.tb02570.x
12. Harman SM, Metter EJ, Tobin JD, et al. Longitudinal effects of aging on serum total and free testosterone levels in healthy men. Baltimore Longitudinal Study of Aging. The Journal of clinical endocrinology and metabolism. 2001;86(2):724-731. doi: https://doi.org/10.1210/jcem.86.2.7219
13. Carruthers M, Trinick TR, Jankowska E, et al. Are the adverse effects of glitazones linked to induced testosterone deficiency? Cardiovascular diabetology. 2008;7:30. doi: https://doi.org/10.1186/1475-2840-7-30
14. Савельева Л.В., Роживанов Р.В., Шурдумова Б.О., и др. Нормогонадотропный гипогонадизм у мужчин с ожирением // Ожирение и метаболизм. — 2009. — Т. 6. — №3. — С. 39-42.
15. Laaksonen DE, Niskanen L, Punnonen K, et al. Testosterone and sex hormone-binding globulin predict the metabolic syndrome and diabetes in middle-aged men. Diabetes care. 2004;27(5):1036-1041. doi: https://doi.org/10.2337/diacare.27.5.1036
16. Antonio L, Wu FC, O’Neill TW, et al. Associations between sex steroids and the development of metabolic syndrome: a longitudinal study in European men. The Journal of clinical endocrinology and metabolism. 2015;100(4):1396-1404. doi: https://doi.org/10.1210/jc.2014-4184
17. Ohlsson C, Barrett-Connor E, Bhasin S, et al. High serum testosterone is associated with reduced risk of cardiovascular events in elderly men. The MrOS (Osteoporotic Fractures in Men) study in Sweden. Journal of the American College of Cardiology. 2011;58(16):1674-1681. doi: https://doi.org/10.1016/j.jacc.2011.07.019
18. Bhasin S, Cunningham GR, Hayes FJ, et al. Testosterone therapy in men with androgen deficiency syndromes: an Endocrine Society clinical practice guideline. The Journal of clinical endocrinology and metabolism. 2010;95(6):2536-2559. doi: https://doi.org/10.1210/jc.2009-2354
19. Traish AM, Saad F, Guay A. The Dark Side of Testosterone Deficiency: II. Type 2 Diabetes and Insulin Resistance. Journal of Andrology. 2009;30(1):23-32. doi: https://doi.org/10.2164/jandrol.108.005751
20. Grossmann M, Thomas MC, Panagiotopoulos S, et al. Low Testosterone Levels Are Common and Associated with Insulin Resistance in Men with Diabetes. The Journal of Clinical Endocrinology & Metabolism. 2008;93(5):1834-1840. doi: https://doi.org/10.1210/jc.2007-2177
21. Rhoden EL, Ribeiro EP, Teloken C, et al. Diabetes mellitus is associated with subnormal serum levels of free testosterone in men. BJU international. 2005;96(6):867-870. doi: https://doi.org/10.1111/j.1464-410X.2005.05728.x
22. Dhindsa S, Prabhakar S, Sethi M, et al. Frequent Occurrence of Hypogonadotropic Hypogonadism in Type 2 Diabetes. The Journal of Clinical Endocrinology & Metabolism. 2004;89(11):5462-5468. doi: https://doi.org/10.1210/jc.2004-0804
23. Ding EL, Song Y, Malik VS, et al. Sex differences of endogenous sex hormones and risk of type 2 diabetes: a systematic review and meta-analysis. JAMA. 2006;295(11):1288-1299. doi: https://doi.org/10.1001/jama.295.11.1288
24. MacDonald AA, Herbison GP, Showell M, et al. The impact of body mass index on semen parameters and reproductive hormones in human males: a systematic review with meta-analysis. Human reproduction update. 2010;16(3):293-311. doi: https://doi.org/10.1093/humupd/dmp047
25. Schneider G, Kirschner MA, Berkowitz R, Ertel NH. Increased Estrogen Production in Obese Men*. J Clin Endocrinol Metab. 1979;48(4):633-638. doi: https://doi.org/10.1210/jcem-48-4-633
26. Cutolo M. Estrogen metabolites: increasing evidence for their role in rheumatoid arthritis and systemic lupus erythematosus. The Journal of rheumatology. 2004;31(3):419-421
27. Castagnetta LA, Carruba G, Granata OM, et al. Increased estrogen formation and estrogen to androgen ratio in the synovial fluid of patients with rheumatoid arthritis. The Journal of rheumatology. 2003;30(12):2597-2605
28. Butaney M, Thirumavalavan N, Balasubramanian A, et al. Treatment of Estrogen Levels in the Management of Hypogonadism: An Anonymous Survey of ISSM Members. Urology. 2020;139:104-109. doi: https://doi.org/10.1016/j.urology.2020.01.032
29. Bhasin S, Cunningham GR, Hayes FJ, et al. Testosterone Therapy in Men with Androgen Deficiency Syndromes: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2010;95(6):2536-2559. doi: https://doi.org/10.1210/jc.2009-2354
30. Alvaro M., Bebb RA, Manjo P. et al, Diagnosis and management of testosterone deficiency syndrome in men: clinical practice guideline. CMAJ; 2015;187(18):1369-1377. doi: https://doi.org/10.1503/cmaj.150033
31. Estradiol, serum; Available from: https://www.mayocliniclabs.com/test-catalog/Clinical+and+Interpretive/81816. [cited 03.10.2020]
32. Jankowska EA, Rozentryt P, Ponikowska B, et al. Circulating estradiol and mortality in men with systolic chronic heart failure. Jama. 2009;301(18):1892-1901. doi: https://doi.org/10.1001/jama.2009.639
33. Basu A, Seth S, Arora K, et al. Evaluating estradiol levels in male patients with colorectal carcinoma. Journal of clinical and diagnostic research : JCDR. 2015;9(1):8-10. doi: https://doi.org/10.7860/jcdr/2015/10508.5397
34. Rubinow KB. Estrogens and Body Weight Regulation in Men. Advances in experimental medicine and biology. 2017;1043:285-313. doi: https://doi.org/10.1007/978-3-319-70178-3_14
Об авторах
З. Ш. ПавловаРоссия
Павлова Зухра Шариповна, к.м.н.; eLibrary SPIN: 9329-7628
Россия, 119991, Москва, ул. Ленинские горы, д. 1
И. И. Голодников
Россия
Голодников Иван Иванович, ординатор; eLibrary SPIN: 3213-0916
Москва
Я. А. Орлова
Россия
Орлова Яна Артуровна, д.м.н.; eLibrary SPIN: 3153-8373
Москва
А. А. Камалов
Россия
Камалов Армаис Альбертович, д.м.н., профессор; eLibrary SPIN: 6609-5468
Москва
Дополнительные файлы
|
|
1. Рисунок 1. Уровень тестостерона до и на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(118KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Уровень эстрадиола до и на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(116KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Изменение веса в кг на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(97KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Изменение индекса массы тела, кг/м2, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(97KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Изменение окружности талии, см, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(97KB)
|
Метаданные ▾ | |
|
|
6. Рисунок 6. Изменение окружности бедер, см, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(100KB)
|
Метаданные ▾ | |
|
|
7. Рисунок 7. Изменение уровней глобулина, связывающего половые гормоны, на фоне тестостеронзаместительной терапии, в 1-й (ТУ), во 2-й (ГТ) и в 3-й (ХГЧ) группах. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(100KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Павлова З.Ш., Голодников И.И., Орлова Я.А., Камалов А.А. Изменения антропометрических характеристик, уровня андрогенов и эстрогенов при коррекции мужского гипогонадизма препаратами тестостерона или хорионического гонадотропина: результаты ретроспективного сравнительного исследования. Ожирение и метаболизм. 2021;18(3):268-275. https://doi.org/10.14341/omet12733
For citation:
Pavlova Z.S., Golodnikov I.I., Orlova Y.A., Kamalov A.A. Changes in anthropometric characteristics, androgen and estrogen levels during correction of male hypogonadism with testosterone or hCG: results of a retrospective comparative study. Obesity and metabolism. 2021;18(3):268-275. (In Russ.) https://doi.org/10.14341/omet12733

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).










































