Перейти к:
Характеристика уровня артериального давления у детей с различной массой тела
https://doi.org/10.14341/omet12721
Аннотация
Обоснование. Эссенциальная артериальная гипертензия (АГ) чаще развивается у детей при наличии факторов риска — ожирения и избыточной массы тела, отягощенной наследственности и генетической предрасположенности.
Цель. Изучение особенностей клинического течения АГ у подростков с нормальной массой тела, избытком массы тела и ожирением.
Материалы и методы. Исследование проводилось у детей с диагнозом АГ, находившихся на лечении в двух детских больницах г. Воронежа в 2016–2020 гг. Проводился ретроспективный анализ историй болезни детей, учитывались данные анамнеза, клинико-лабораторного и инструментального обследования. У части детей проведено генетическое тестирование методом полимеразной цепной реакции для определения патологических аллелей генов, регулирующих артериальное давление (АД).
Результаты. В исследовании приняли участие 96 пациентов в возрасте от 9 до 17 лет. В группу детей с нормальной массой тела включены 38 пациентов (39,6%), медиана возраста 16,4 года (10,7; 17,9), с избытком массы тела — 33 человека (34,4%), медиана возраста 15,2 года (12,0; 17,9), с ожирением — 25 детей (26,0%), медиана возраста 14,5 года (9,2; 17,9). Дети с ожирением развивали АГ в более раннем возрасте (р=0,023). По данным суточного мониторирования АД (СМАД) патологические значения систолического АД (САД) днем (выше значения 95-го перцентиля) среди детей с нормальной массой тела наблюдались у 17 пациентов (44,7%), среди детей с избытком массы тела — у 14 человек (42,4%), среди детей с ожирением — у 16 человек (64%), p=0,031. Получены достоверные различия между группами по значениям индекса времени (ИВ) САД ночью (p=0,006). ИВ диастолического АД днем >50% был отмечен только в группе детей с ожирением — 4 человека (16%) (p=0,042). При проведении генетического исследования у отдельных пациентов наиболее часто выявлялись патологические аллели гена ангиотензиногена (AGT: 704 T>C), гена альдостеронсинтазы (CYP11B2: -344 C>T) и эндотелиальной синтазы азота 3 типа (NOS3: -786 T>C).
Заключение. Дети с ожирением раньше развивали АГ по сравнению со своими сверстниками с нормальной массой тела и чаще имели неблагоприятный профиль течения АГ по данным СМАД. Данные результаты могут использоваться для подбора персонализированной терапии, а также формирования настороженности в поражении определенных органов-мишеней.
Для цитирования:
Чубаров Т.В., Петеркова В.А., Батищева Г.А., Жданова О.А., Шаршова О.Г., Артющенко А.И., Бессонова А.В. Характеристика уровня артериального давления у детей с различной массой тела. Ожирение и метаболизм. 2022;19(1):27-34. https://doi.org/10.14341/omet12721
For citation:
Chubarov T.V., Peterkova V.A., Batischeva G.A., Zhdanova O.A., Sharshova O.G., Artyushchenko A.I., Bessonova A.V. Characteristics of blood pressure level in children with different body weight. Obesity and metabolism. 2022;19(1):27-34. (In Russ.) https://doi.org/10.14341/omet12721
ОБОСНОВАНИЕ
Истоки первичной артериальной гипертензии (АГ) закладываются в детском и подростковом возрасте, когда формируются нейрогенные и гуморальные механизмы регуляции деятельности сердечно-сосудистой системы и артериального давления (АД) [1]. В настоящее время АГ встречается у 6,8–18% подростков, имеющих хронические заболевания, и по распространенности уступает только астме и ожирению [2]. АГ у детей и подростков является фактором риска атеросклероза, ишемической болезни сердца, цереброваскулярных осложнений, сердечной недостаточности, хронической болезни почек, которые могут возникнуть во взрослом возрасте [3][4].
Эссенциальная АГ чаще развивается у детей при наличии факторов риска — ожирения и избыточной массы тела, отягощенной наследственности и генетической предрасположенности [1]. Ожирение относится к наиболее значимой медико-социальной проблеме, стоящей перед здравоохранением большинства стран мира. Распространенность ожирения среди детей в возрасте от 6 до 11 лет за последние 20 лет увеличилась почти в 2 раза (с 7 до 13%), а среди подростков в возрасте от 12 до 19 лет — практически в 3 раза (с 5 до 14%) [2]. Распространенность АГ среди детской популяции составляет в настоящее время от 2,2 до 22,0% [5]. Ожирение связано с АГ и ухудшает ее прогноз. По данным отечественных и зарубежных исследователей, избыток массы тела коррелирует с уровнем артериального давления [3][4][6]. По данным Flynn J.T. et al. (2017), распространенность АГ у подростков с избыточной массой тела и ожирением составляет до 24,8% [4].
ЦЕЛЬ ИССЛЕДОВАНИЯ
Изучение особенностей клинического течения АГ у подростков с нормальной массой тела, избытком массы тела и ожирением.
МАТЕРИАЛЫ И МЕТОДЫ
Место и время проведения исследования
Место проведения. Воронежская детская клиническая больница ФГБОУ ВО «ВГМУ им. Н.Н. Бурденко» Минздрава России, БУЗ ВО «Воронежская областная детская клиническая больница №1».
Время исследования. Исследование включало ретроспективный анализ историй болезни пациентов, находившихся на стационарном лечении в период с января 2016 г. по декабрь 2020 г.
Изучаемые популяции (одна или несколько)
Изучалась одна популяция, которую составили дети с первичной АГ.
Критерии включения: дети (мальчики и девочки), которые проходили обследование по поводу АГ в условиях стационара.
Критерий исключения: наличие симптоматической АГ.
Способ формирования выборки из изучаемой популяции (или нескольких выборок из нескольких изучаемых популяций)
Сплошной.
Дизайн исследования
Проводилось многоцентровое наблюдательное одномоментное ретроспективное одновыборочное неконтролируемое исследование.
Описание медицинского вмешательства (для интервенционных исследований)
Проводился ретроспективный анализ историй болезни детей, учитывались данные анамнеза, клинико-лабораторного, инструментального обследования и проводимая фармакотерапия. В интересах исследования части детей было проведено генетическое тестирование методом полимеразной цепной реакции (ПЦР) для определения патологических аллелей генов, регулирующих АД.
Методы
АГ диагностировалась в соответствии с российскими Клиническими рекомендациями по диагностике и лечению артериальной гипертензии у детей и подростков [1]. К АГ относили состояние, при котором средний уровень систолического артериального давления (САД) и/или диастолического артериального давления (ДАД), рассчитанный на основании 3 отдельных измерений, более или равен значению 95-го перцентиля АД в популяции для соответствующего возраста, пола и роста. Физическое развитие детей оценивалось согласно рекомендациям Всемирной организации здравоохранения (ВОЗ) [2] с использованием программы WHO AnthroPlus. Избыток массы тела диагностировали при значениях индекса массы тела (ИМТ) для соответствующего возраста и пола ребенка более 1 и менее 2 стандартных отклонений (standard deviation score, SDS), ожирение — более 2 SDS ИМТ [2].
Оценивалась характеристика состояния сердечно-сосудистой системы, наличие поражения органов-мишеней, особенности течения АГ у подростков с избытком массы тела и ожирением. Проводилась оценка фармакотерапии у пациентов с АГ с учетом наличия или отсутствия избытка массы тела и ожирения.
Данные наследственной отягощенности по сердечно-сосудистым заболеваниям формировались на основании данных анамнеза и опроса родителей пациентов, оценивались показатели физического развития (длина тела, масса тела, ИМТ), АД (результаты мониторирования АД по дневникам наблюдений), инструментальных исследований (электрокардиография (ЭКГ), эхокардиография (ЭхоКГ), суточного мониторирования артериального давления (СМАД)).
У части пациентов проводилось исследование в крови генетических маркеров АГ методом ПЦР: гена AGTR1 (кодирует ангиотензиновый рецептор 1), гена AGTR2 (кодирует ангиотензиновый рецептор-2), генов ангиотензиногена (AGT C521T и AGT T704C), генов ангиотензиновых рецепторов (AGTR1 (А1166С) и AGTR2 (G1675A)), гена альдостерон-синтазы CYP11B2 (C(-344)T), гена ADD1 (G1378T), кодирующего белок альфа-аддуцин, гена GNB3, кодирующего G-белок, и гена NOS3 (эндотелиальной синтазы азота).
Статистический анализ
Размер выборки предварительно не рассчитывался.
Методы статистического анализа данных:
а)анализ данных проводился с использованием пакета статистической обработки Statistica 6.1 и программы Biostat (версия 4.03);
б)качественные показатели представлены в виде абсолютных значений и процентов, количественные — в виде медианы и максимальных и минимальных значений;
в)для анализа различий в группах использовали однофакторный дисперсионный анализ. Для сравнения качественных показателей использовали критерий χ2. Достоверность различий определяли при значениях р<0,05.
Этическая экспертиза
Все стадии исследования соответствовали законодательству Российской Федерации, международным этическим нормам, одобрены Этическим комитетом ГБОУ ВПО «ВГМУ им. Н.Н. Бурденко» Минздрава России (протокол № 2 от 26.05.2016 г.). От всех пациентов или их законных представителей получено информированное согласие.
РЕЗУЛЬТАТЫ
В исследование включены дети, которые находились на лечении в кардиологическом отделении с диагнозом АГ.
Выборку составили 96 пациентов в возрасте от 9 до 17 лет, средний возраст — 15,9 года (14,1; 16,8). Мальчиков было 70 (72,9%), девочек — 26 (27,1%). Жители города Воронежа — 46 (47,9%), районов области — 50 детей (52,1%).
В группу детей с нормальной массой тела включены 38 пациентов (39,6%), медиана возраста 16,4 года (10,7; 17,9), с избытком массы тела — 33 человека (34,4%), медиана возраста 15,2 года (12,0; 17,9), с ожирением — 25 детей (26,0%), медиана возраста 14,8 года (9,2; 17,9). Среди наших пациентов не было детей с недостатком массы тела. На основании проведенных наблюдений дети с ожирением развивали АГ в более раннем возрасте (р=0,029) (рис. 1).
По данным СМАД патологический уровень САД днем (среднее значение выше 95-го перцентиля) среди детей с нормальной массой тела наблюдался у 17 пациентов (44,7%), среди детей с избытком массы тела данный показатель встречался у 14 человек (42,4%), среди детей с ожирением — 16 человек (64%). Полученные различия достоверны, p=0,031. Данные наглядно представлены на рис. 2.
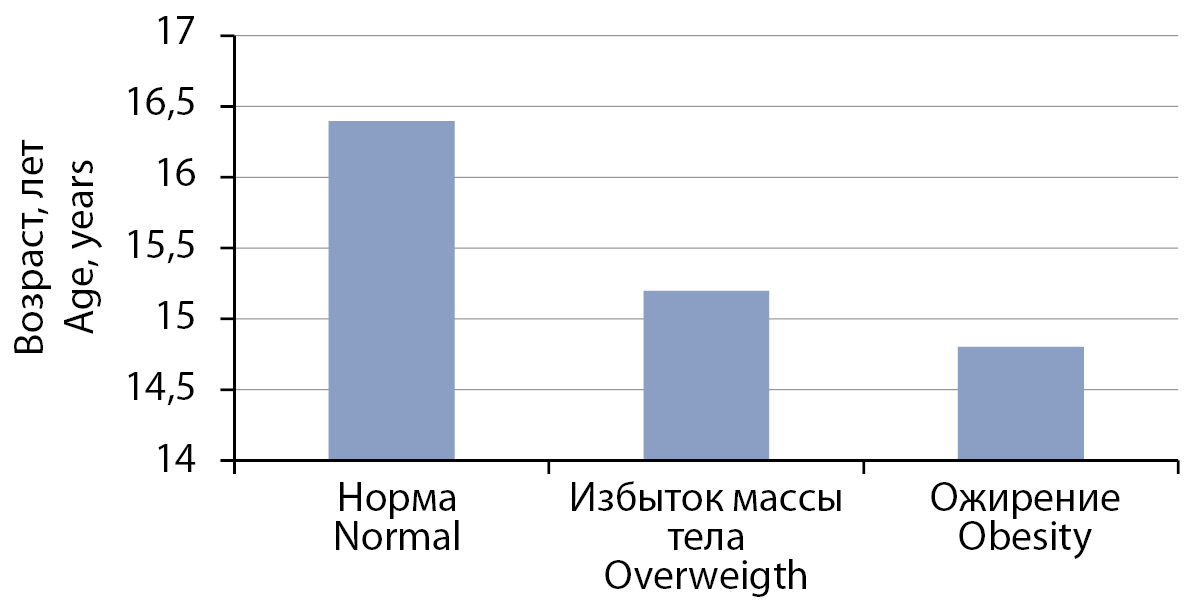
Рисунок 1. Медиана возраста пациентов с артериальной гипертензией и различными значениями индекса массы тела.
Figure 1. Median age of patients with arterial hypertension and different values of body mass index.
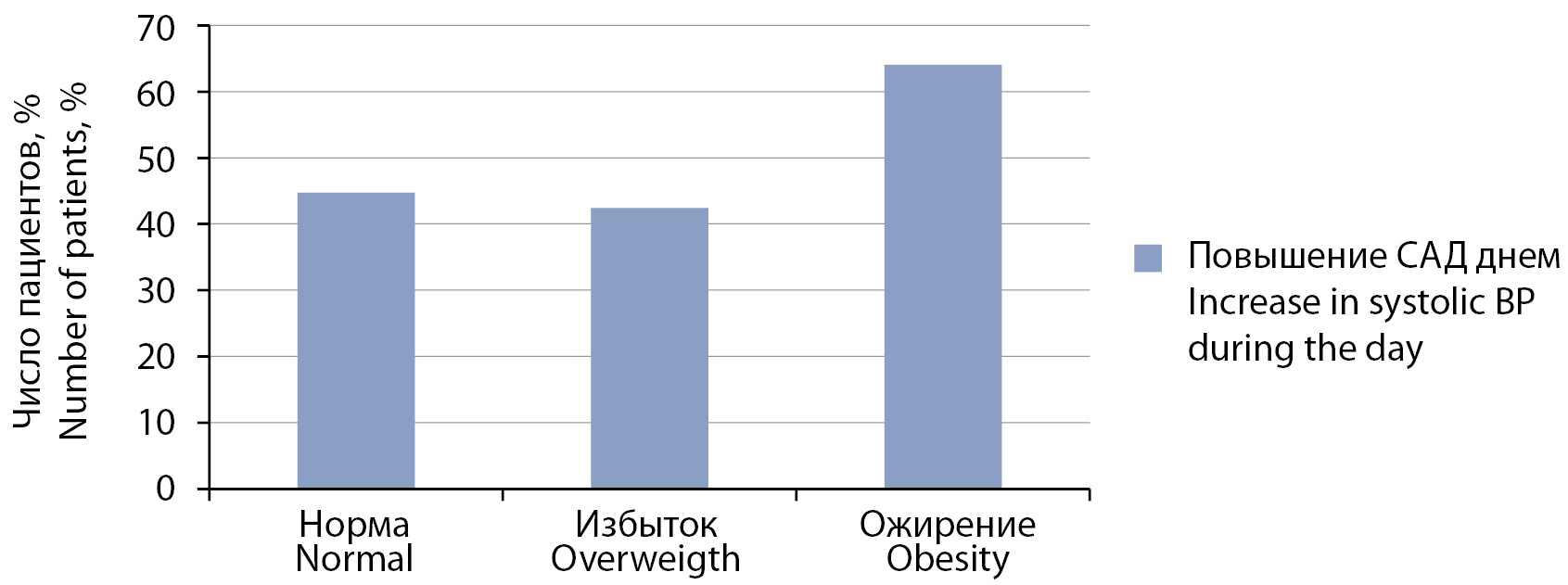
Рисунок 2. Частота встречаемости патологических значений среднего систолического артериального давления днем у пациентов с различной массой тела.
Figure 2. The frequency of pathological values of mean systolic BP during the day in patients with different body weight.
Высокое среднее САД ночью отмечалось у 12 детей с нормальной массой (31,5%), с избытком массы тела — у 9 детей (27,2%), среди пациентов с ожирением — у 14 человек (56%). Достоверных различий между группами не получено, p=0,130.
Анализ стойкости АГ проводился с помощью величины индекса времени (ИВ). При ИВ 25–50% течение АГ расценивалось как лабильное, значение ИВ более 50% свидетельствовало о стабильной АГ. Так, в группе детей с нормальной массой тела ИВ САД днем >50% наблюдался у 15 детей (39,5%), ночью — у 11 детей (28,9%), в группе детей с избытком массой тела — днем у 7 человек (26,3%), ночью патологических показателей не было зафиксировано, в группе детей с ожирением — у 14 человек (56%) днем, ночью — у 11 человек (44%). Получены достоверные различия между группами по значениям ИВ САД ночью (p=0,006).
ИВ ДАД днем >50% был отмечен только в группе детей с ожирением — 4 человека (16%) (p=0,042), ночью наблюдался у 3 детей (7,9%) с нормальной массой тела, в группе детей с избытком массой тела не был зафиксирован, в группе детей с ожирением — у 3 человек (12%), достоверных различий среди сравниваемых групп не получено (p=0,250).
Для определения адекватности снижения АД ночью использовался суточный индекс (СИ), который в норме составлял 10–20% по сравнению с дневными показателями. СИ САД менее 10%, который свидетельствует о недостаточном снижении ночного АД [1], в группе детей с нормальной массой наблюдался у 9 человек (23,6%), среди детей с избытком массы — у 6 человек (18,2%), среди детей с ожирением — у 8 человек (32%). Низкое значение СИ ассоциировано с поражением органов-мишеней. СИ САД более 20% (повышенная степень снижения АД ночью) в группе детей с нормальной массой наблюдался у 1 ребенка (2,6%), с избытком массы тела — также у 1 человека (3%), среди детей с ожирением не наблюдалось, p=0,670. СИ ДАД более 20% (повышенная степень снижения АД ночью) в группе детей с нормальной массой наблюдался у 9 человек (23,7%), среди детей с избытком массы — у 8 человек (24,2%), среди детей с ожирением — у 4 человек (16%), p=0,630. СИ ДАД менее 10% (недостаточное снижение АД ночью) в группе детей с нормальной массой наблюдался у 5 человек (13,1%), среди детей с избытком массы — у 7 человек (21,2%), среди детей с ожирением — у 5 человек (20%), p=0,612. У одного ребенка (3%) из группы с избытком массы тела отмечался СИ ДАД ночью менее 0%, что говорит об устойчивом ночном повышении ДАД.
По результатам эхокардиографии утолщение межжелудочковой перегородки было выявлено у 3 детей с нормальной массой тела (7,8%), у 4 детей с избытком массы тела (12,1%), у 2 детей с ожирением (8%), признаки концентрической гипертрофии миокарда левого желудочка отмечены у одного ребенка с избытком массы тела (3%). Достоверных различий между группами не получено (p=0,678). Все дети с изменениями по данным ультразвукового исследования сердца имели стойкую систоло-диастолическую АГ.
Среди пациентов 1-й группы у 7 человек (18,4%) имелся отягощенный наследственный анамнез (хотя бы один из родителей страдал АГ), во 2-й группе выявлены 8 детей (24,2%), которые имели отягощенную наследственность по гипертензии среди родственников 1-й линии, в 3-й группе — 7 детей (28%), p=0,322. Отягощенный наследственный анамнез по ожирению, согласно данным, полученным из медицинской документации, отмечался у 2 (6,1%) детей из группы с избытком массы тела, 5 (20%) детей из группы ожирения, не отягощен у детей из группы с нормальной массой тела. Данные значения могут быть связаны с дефектами сбора наследственного анамнеза.
Трем пациентам из группы с избытком массы тела и 3 детям с ожирением было проведено генетическое тестирование методом ПЦР для выявления патологических аллелей генов АГ. Оценивались варианты кодирующего альфа-аддуцин гена ADD1: 1378 G>T, гена ангиотензиногена AGT: 521 C>T и AGT: 704 T>C, генов, кодирующих рецепторы к ангиотензину 1 и 2, AGTR1: 1166 A>C и AGTR2: 1675 C>A, гена альдостерон-синтазы CYP11B2: -344 C>T, эндотелиальной синтазы азота 3 типа NOS3: -786 T>CNOS3: 894 G>T. Результаты представлены на рис. 4. Генетическое исследование в группе детей с нормальной массой тела авторами планируется провести в ходе дальнейших исследований.
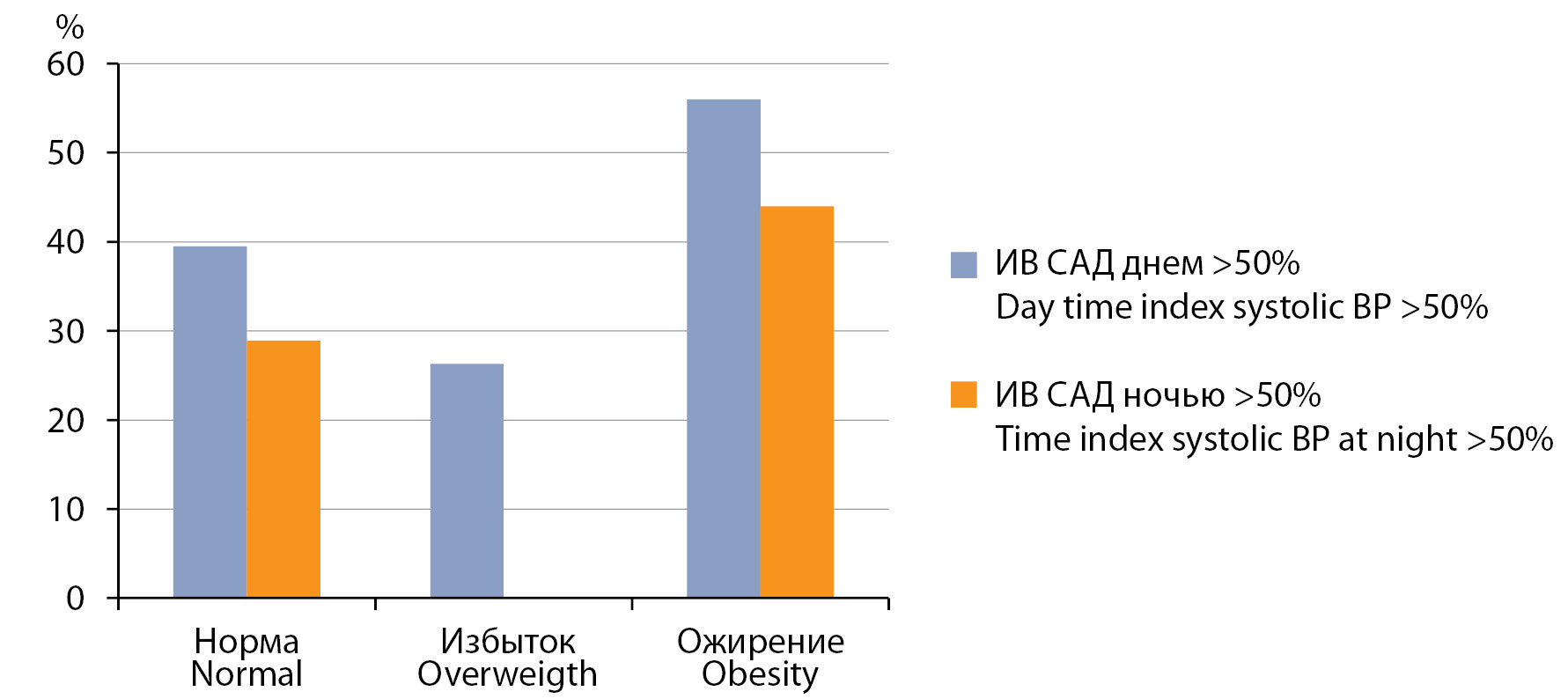
Рисунок 3. Частота встречаемости патологических значений индекса времени систолического артериального давления у пациентов с различными значениями индекса массы тела.
Figure 3. Frequency of pathological values of the systolic blood pressure time index in patients with different body mass index values.
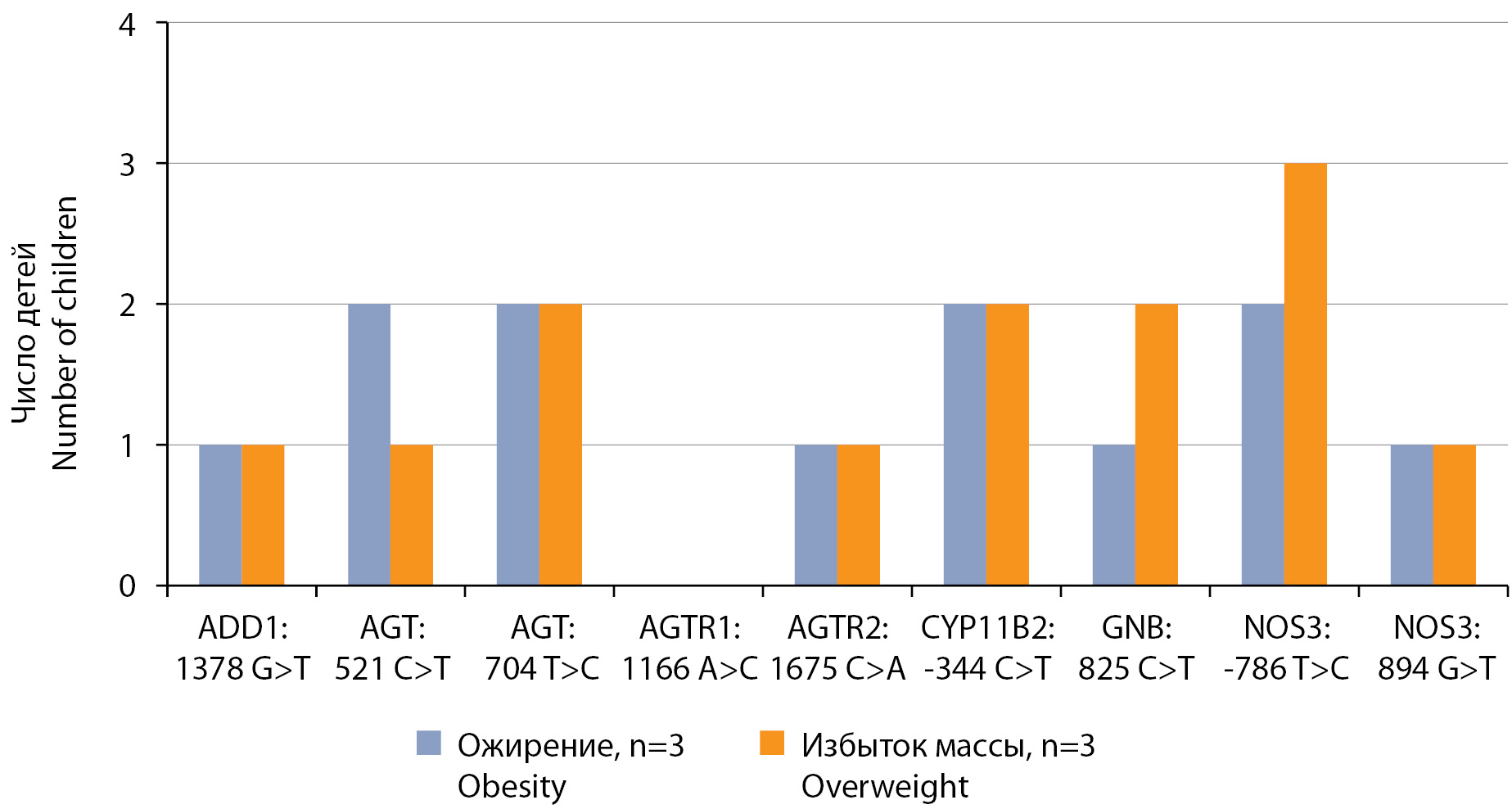
Рисунок 4. Частота встречаемости патологических аллелей генов, ассоциированных с артериальной гипертензией, среди детей с различными значениями индекса массы тела.
Figure 4. The frequency of pathological alleles of genes associated with hypertension among children with different body mass index values.
У всех пациентов выявлялись патологические аллели генов, ассоциированных с АГ. Двое детей с избытком массы тела имели изменения генов ангиотензиногена, что может приводить к повышению уровня ангиотензиногена в крови, гена альдостерон-синтазы и эндотелиальной синтазы азота. Реже у детей с избытком массы тела выявлялись изменения генов белка альфа-аддуцина, участвующего в транспорте ионов натрия в клетках почечных канальцев, гена ангиотензинового рецептора 2, гена, кодирующего активность G-белка.
Все дети с ожирением имели патологические аллели гена NOS3, у большинства были изменены гены ангиотензина, альдостерон-синтазы, G-белка. Не было выявлено патологических аллелей гена AGTR1.
Нежелательных явлений в ходе исследования выявлено не было.
ОБСУЖДЕНИЕ
Репрезентативность выборок
На репрезентативность выборки могли оказать влияние внешние факторы. В частности, популяцию составили дети с более тяжелым течением заболевания, нуждавшиеся в лечении в условиях стационара. Возможным остается влияние социального фактора — большинство детей относились к городскому населению. Вероятно, в популяции детей с ожирением имеется достаточное количество невыявленных случаев АГ, что связано с низкой настороженностью среди родителей и врачей первичного звена.
Сопоставление с другими публикациями
Дети с ожирением, по нашим данным, развивали АГ в более раннем возрасте (медиана 14,5 года), чем дети с нормальной массой тела и избытком массы тела. Изучение распространенности АГ среди детей Санкт-Петербурга, проведенное Н.Б. Куприенко и Н.Н. Смирновой (2020), выявило высокую распространенность АГ среди детей с избыточной массой тела и ожирением — до 6,5% по сравнению с 0,6% среди детей с нормальной массой тела [8]. Практически в любом возрасте динамика АД зависит от динамики ИМТ. Об этом свидетельствуют и данные, опубликованные Американской академией педиатрии: повышенный ИМТ даже в раннем детском возрасте ассоциирован с более высоким АД в будущем [4]. Вероятно, риск развития АГ возрастает с увеличением степени ожирения. Полученные нами данные свидетельствуют о более неблагоприятном течении АГ у детей с ожирением, что, вероятно, способствует раннему поражению органов-мишеней и развитию осложнений во взрослом возрасте [7]. По нашим данным, патологические значения САД днем (выше значения 95-го перцентиля) достоверно чаще встречались среди детей с ожирением (64,0%) по сравнению с пациентами с нормальной массой тела (42,4%), p=0,031. Дети с ожирением имели более высокие значения индекса времени САД ночью и индекса времени ДАД ночью (р=0,006 и 0,042 соответственно). Изменения миокарда по данным ультразвукового исследования сердца выявлены у пациентов со стойкой систоло-диастолической гипертензией. О неблагоприятном течении и прогнозе АГ у детей с ожирением свидетельствуют многочисленные литературные источники [8–10]. Греков И.С. и соавт. (2020), проведя обзор литературных данных, указывают, что ожирение рассматривается как один из факторов риска развития эссенциальной АГ. У детей с метаболическим синдромом и АГ увеличивается риск развития ишемической болезни сердца уже в молодом возрасте [8].
АГ является полиэтиологическим и многофакторным заболеванием. В настоящее время выделяют несколько патофизиологических механизмов формирования АГ у детей с нарушениями питания. Возникающая при ожирении инсулинорезистентность приводит к повышению активности симпатической нервной системы, что вызывает активацию юкстагломерулярного аппарата почки и ренин-ангиотензин-альдостероновой системы, в результате чего повышается реабсорбция натрия и воды, повышается общее периферическое сосудистое сопротивление. Другим механизмом является развитие эндотелиальной дисфункции — в частности, выработка активных форм кислорода запускает процессы перекисного окисления, в результате чего снижается продукция вазодилататоров — оксида азота, брадикинина, простациклина. Помимо этого, с ожирением ассоциирована выработка ряда сосудосуживающих веществ, таких как эндотелин и ангиотензин II [11].
Среди детей с ожирением в нашем исследовании достоверно чаще выявлялась стабильная АГ по данным СМАД, что соответствует данным других публикаций. Стойкая систолическая гипертензия днем у 56% детей с ожирением против 39,5% среди детей с нормальной массой тела и 26,3% детей с избытком массы, ночью — 44% детей с ожирением, 28,9% детей с нормальной массой, показатели ДАД днем были достоверно выше в группе детей с ожирением, ночью достоверных различий между группами не получено. В исследовании, проведенном на базе Федерального центра сердца, крови и эндокринологии им. Алмазова, которое включало 410 детей, стабильная АГ по данным СМАД отмечалась у 60% больных с ожирением, в группе детей с избыточной массой тела — у 36% и в группе детей с нормальной массой тела — в 27% случаев (p=0,01) [12]. Высокий уровень АД в течение суток указывал на избыточную активацию симпатической нервной системы.
Согласно полученным данным, дети с ожирением чаще имели наследственную отягощенность по АГ в сравнении с детьми с нормальной массой тела и избытком массы, но достоверные различия по данному признаку в нашем исследовании не выявлены. В работе О.Ю. Халидуллиной и соавт. (2019) наличие у родителей ожирения, гипертонической болезни способствовало более ранней манифестации высокого АД [13]. Авторы включали в исследование детей с ожирением абдоминального и равномерного типа 1-й степени и выше. Помимо этого, по некоторым данным, у детей с наследственной отягощенностью по АГ в семье незначительное повышение АД способствовало выраженной гипертрофии миокарда и ригидности сосудистой стенки в результате нарушения взаимодействия клеточных мембран с ионами кальция [8].
Продолжают изучаться различные генетические варианты, ассоциированные с АГ [14, 15]. Наличие генетического маркера гена ангиотензиногена (AGT C521T, AGT T704C) ассоциировано с риском развития поражений органов-мишеней: гипертрофией левого желудочка, изменением эластичности сонных артерий. Патологические аллели генов, кодирующих рецепторы к ангиотензину 1 и 2 (AGRTR1, AGTR2), активируют ренин-ангиотензин-альдостероновую систему, что приводит к увеличению общего периферического сосудистого сопротивления, гипертрофии левого желудочка. Вариант гена альдостерон-синтазы CYP11B2 (C(-344)T) увеличивает базальную секрецию альдостерона и ассоциирован с увеличением массы миокарда и расширением полости левого желудочка, а также, по некоторым данным, связан с развитием «сольчувствительной» формы АГ [15]. Маркер гена альфа-аддуцина ADD1 (G1378T) регулирует транспорт ионов натрия в канальцах почки, приводя к задержке жидкости и гиперволемии. Гуанин-связывающий протеин GNB3 повышает сосудистый тонус, а патологический аллель маркера эндотелиальной синтазы азота 3 типа (NOS3) приводит к дисфункции эндотелия путем снижения выработки оксида азота и повышает риск тромбоза. В нашем исследовании среди отдельных пациентов наиболее часто встречались патологические варианты AGT: 704 T>C, CYP11B2: -344 C>T, NOS3: -786 T>C.
По данным ряда авторов [15–17], течение АГ у взрослых и детей с генетическим полиморфизмом характеризуется манифестацией в более раннем возрасте, быстрыми темпами прогрессирования и высокой частотой развития осложнений. Поэтому фармакогенетическое тестирование, позволяющее помочь в подборе персонализированной терапии, в настоящее время является перспективным направлением для изучения и применения в клинической практике.
Клиническая значимость результатов
Таким образом, дети с ожирением раньше развивали АГ по сравнению со своими сверстниками с нормальной массой тела, чаще имели неблагоприятный профиль течения АГ по данным СМАД (среднее САД днем, стойкое повышение САД ночью) и чаще нуждались в назначении антигипертензивных препаратов. Полученные данные свидетельствуют о том, что ожирение является фактором риска развития и прогрессирования АГ. Следовательно, детей с ожирением следует рассматривать как группу риска АГ, необходимо своевременно обследовать и выявлять данное заболевание для его коррекции и предотвращения поражения органов-мишеней у пациентов в дальнейшем.
Дети с избытком массы тела имели более лабильное течение АГ по сравнению с пациентами с нормальной массой тела. Это может быть связано с большей частотой наследственной предрасположенности к АГ в группе детей с нормальной массой тела. Изучение генетической предрасположенности к АГ у детей с нормальной массой тела планируется провести в дальнейших исследованиях.
Ограничения исследования
Исследование было ограничено объемом выборки пациентов, а также вероятно более тяжелым течением заболевания, что могло отличать пациентов от общей популяции детей с АГ.
Направления дальнейших исследований
По нашему мнению, перспективным является изучение генетических факторов развития АГ для персонализированного подбора терапии и прогнозирования поражения органов-мишеней.
ЗАКЛЮЧЕНИЕ
АГ у детей с ожирением имеет более раннее начало и неблагоприятный профиль по данным СМАД. Для детей с АГ вне зависимости от состояния питания характерна отягощенная наследственность по гипертонии, что может быть обусловлено генетической предрасположенностью. При проведении генетического исследования у отдельных пациентов наиболее часто выявлялись патологические аллели AGT: 704 T>C, CYP11B2: -344 C>T, NOS3: -786 T>C. Данные результаты могут использоваться для подбора персонализированной терапии, а также формирования настороженности в поражении определенных органов-мишеней.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Чубаров Т.В., Батищева Г.А. — концепция и дизайн исследования; Жданова О.А., Бессонова А.В. — статистическая обработка данных; Жданова О.А., Артющенко А.И., Шаршова О.Г. — написание текста; Петеркова В.А. — редактирование.
Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Благодарности. Авторы выносят благодарность Гусаревой А.А. за помощь в наборе клинического материала.
Список литературы
1. Александров А.А., Кисляк О.А., Леонтьева И.В., и др. Российское медицинское общество по артериальной гипертонии. Ассоциация детских кардиологов России. Клинические рекомендации. Диагностика, лечение и профилактика артериальной гипертензии у детей и подростков // Системные гипертензии. — 2020. — Т. 17. — №2. — С.7-35. doi: https://doi.org/10.26442/2075082X.2020.2.200126
2. World Health Organization. [Internet]. Available from: https://www.who.int/dietphysicalactivity/childhood/ru/
3. Новиков С.Ю., Шестопалов А.В., Шумилов П.В., и др. Сравнительный анализ липидного и углеводного обмена у подростков с артериальной гипертензией и ожирением // Вопросы детской диетологии (Педиатрическое питание). — 2019. — Т. 17. — №3. — С. 18-27. doi: https://doi.org/10.20953/1727-5784-2019-3-18-27
4. Flynn JT, Kaelber DC, Baker-Smith CM, et al. Subcommittee on screening and management of high blood pressure in children. Clinical Practice Guideline for Screening and Management of High Blood Pressure in Children and Adolescents. Pediatrics. 2017;140(3):e20171904. doi: https://doi.org/10.1542/peds.2017-3035
5. Максимович Н.А., Лукша А.В., Кизелевич А.И. Артериальная гипертензия у детей: современная эпидемиологическая ситуация // Modern science. — 2020. — T. 5. — №3. — С. 450-454.
6. Bigazzi R, Zagato L, Lanzani C, et al. Hypertension in High School Students: Genetic and Environmental Factors: The HYGEF Study. Hypertension. 2020;75(1):71-78 doi: https://doi.org/10.1161/HYPERTENSIONAHA.119.13818
7. Wójtowicz J, Łempicka A, Łuczyński W, et al. Central aortic pressure, arterial stiffness and echocardiographic parameters of children with overweight/obesity and arterial hypertension. Adv Clin Exp Med. 2017;26(9):1399-1404. doi: https://doi.org/10.17219/acem/65485.
8. Греков И.С., Налетов А.В., Чалая Л.Ф. Клинико-диагностические аспекты артериальной гипертензии у детей и подростков (обзор литературы) // Медико-социальные проблемы семьи. — 2020. — Т. 25. — №2. — С. 96-104.
9. Куприенко Н.Б., Смирнова Н.Н. Распространенность артериальной гипертензии у детей школьного возраста с избыточной массой тела и ожирением // Профилактическая и клиническая медицина. — 2020. — Т. 75. — № 2. — C. 64-69.
10. Wühl E. Hypertension in childhood obesity. Acta Paediatr. 2019;108(1):37-43. doi: https://doi.org/10.1111/apa.14551
11. Кобалава Ж.Д., Конради А.О., Недогода С.В. Артериальная гипертензия у взрослых. Клинические рекомендации 2020 // Российский кардиологический журнал. — 2020. — Т. 25. — №3. — С. 149-218. doi: https://doi.org/10.15829/1560-4071-2020-3-3786
12. Образцова Г.И., Гуркина Е.Ю. Артериальная гипертензия у детей с ожирением // Бюллетень Федерального Центра сердца, крови и эндокринологии им. В.А. Алмазова. — 2012. — №1. — С.32-38.
13. Халидуллина О.Ю., Ушакова С.А., Петрушина А.Д., и др. Особенности наследственной отягощенности у детей с артериальной гипертензией и избыточной массой тела // Университетская медицина Урала. — 2019. — T. 5. — №3. — С. 5-9.
14. Oliveira-Paula GH, Pereira SC, Tanus-Santos JE, Lacchini R. Pharmacogenomics And Hypertension: Current Insights. Pharmgenomics Pers Med. 2019;12:341-359. doi: https://doi.org/10.2147/PGPM.S230201
15. Хохлов А.Л., Сироткина А.М., Воронина Е.А., и др. Клиникогенетические ассоциации у больных артериальной гипертензией // Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова. — 2012. — Т. 4. — №2. — С. 80-85.
16. Игнатенко Г.А., Дубовая А.В., Науменко Ю.В., и др. Особенности течения артериальной гипертензии у взрослых и детей с генетическим полиморфизмом // Российский кардиологический журнал. — 2020. — Т. 25, дополнительный выпуск (октябрь). — С. 12-13.
17. Сафроненко А.В. Генеалогические и молекулярно-генетические аспекты артериальной гипертензии // Современные проблемы науки и образования. — 2012. — Т. 4. — №1. — С. 80-86.
Об авторах
Т. В. ЧубаровРоссия
Чубаров Тимофей Валерьевич, кандидат медицинских наук
394018 г. Воронеж, пер. Здоровья, д. 16
eLibrary SPIN: 6559-1476
В. А. Петеркова
Россия
Петеркова Валентина Александровна, доктор медицинских наук, профессор
Москва
eLibrary SPIN: 4009-2463
Г. А. Батищева
Россия
Батищева Галина Александровна, доктор медицинских наук, профессор
Воронеж
Researcher ID: AAD-8203-2019;
Scopus Author ID: 6507913282;
eLibrary SPIN: 2285-1917
О. А. Жданова
Россия
Жданова Ольга Александровна, доктор медицинских наук
Воронеж
Researcher ID: А-9510-2018;
Scopus Author ID: 6602466689;
eLibrary SPIN: 1235-9770
О. Г. Шаршова
Россия
Шаршова Ольга Геннадьевна
Воронеж
А. И. Артющенко
Россия
Артющенко Анна Ивановна, врач - кардиолог
Воронеж
eLibrary SPIN: 4811-1900
А. В. Бессонова
Россия
Бессонова Анна Владимировна
Москва
Дополнительные файлы
|
|
1. Рисунок 1. Медиана возраста пациентов с артериальной гипертензией и различными значениями индекса массы тела. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(76KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Частота встречаемости патологических значений среднего систолического артериального давления днем у пациентов с различной массой тела. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(110KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Частота встречаемости патологических значений индекса времени систолического артериального давления у пациентов с различными значениями индекса массы тела. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(126KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Частота встречаемости патологических аллелей генов, ассоциированных с артериальной гипертензией, среди детей с различными значениями индекса массы тела. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(170KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Чубаров Т.В., Петеркова В.А., Батищева Г.А., Жданова О.А., Шаршова О.Г., Артющенко А.И., Бессонова А.В. Характеристика уровня артериального давления у детей с различной массой тела. Ожирение и метаболизм. 2022;19(1):27-34. https://doi.org/10.14341/omet12721
For citation:
Chubarov T.V., Peterkova V.A., Batischeva G.A., Zhdanova O.A., Sharshova O.G., Artyushchenko A.I., Bessonova A.V. Characteristics of blood pressure level in children with different body weight. Obesity and metabolism. 2022;19(1):27-34. (In Russ.) https://doi.org/10.14341/omet12721

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).










































